Clear Sky Science · zh
一种能降解 HER2 和 EGFR 的药物消除了 p95HER2,并在 HER2 阳性乳腺癌中显示出强效抗肿瘤活性
此项研究为何重要
对于患有一种称为 HER2 阳性、侵袭性强的乳腺癌的人来说,现代药物已将这种曾经致命的诊断转变为可治疗的疾病。然而,仍有部分肿瘤能够找到逃避治疗并继续生长的途径。本研究聚焦于一个尤其棘手的元凶——一种被截短的 HER2 蛋白形式,称为 p95HER2——并介绍了一种实验性药物 PEPDG278D,研究显示它似乎能抹去这一逃逸通路,使即便是高度耐药的肿瘤在小鼠中也进入持久缓解。
难治的乳腺癌亚型
大约五分之一的乳腺癌携带名为 HER2 的基因拷贝过多,这会使细胞比正常更快地生长和分裂。已有多种成功药物针对 HER2,包括像曲妥珠单抗这样的抗体以及称为酪氨酸激酶抑制剂的小分子口服药。然而,许多肿瘤最终会产生耐药性。一个主要原因是 p95HER2 的出现——这是一段被截短但持续活跃的片段,即使在 HER2 外部区域被切除后仍锚定于细胞膜。该片段缺乏抗体药物通常结合的位点,助长肿瘤侵袭与转移,并与患者预后不良相关。
现有药物及其局限
作者首先在一系列体外培养的人乳腺癌细胞系中比较了标准的 HER2 靶向药物——曲妥珠单抗、帕妥珠单抗、图卡替尼和拉帕替尼。这些细胞系过表达全长 HER2,并产生不同量的 p95HER2。尽管获批药物在某些细胞中能减缓生长,但效果有限且不稳定,尤其是在伴有生长信号通路突变等额外耐药因素的模型中。重要的是,这些药物均未明显降低细胞内实际的 HER2 或 p95HER2 蛋白含量;至多它们削弱了一些活性,在某些情况下甚至提高了令人头疼的 p95HER2 片段水平。
一种新策略:让受体消失
PEPDG278D 采取了不同的策略。它不是单纯阻断 HER2 的活性,而是一种工程化的人源蛋白,能结合 HER2 和相关生长受体 EGFR 的外部结构,并触发它们在细胞内被清除和分解。在多种 HER2 阳性乳腺癌细胞系中,极低剂量的 PEPDG278D 即显著抑制细胞生长。详尽的蛋白分析显示,它几乎完全消除了 HER2、EGFR 和 p95HER2,以及驱动增殖和生存的关键信号开关(如 AKT 与 ERK 的磷酸化)。值得注意的是,PEPDG278D 并未改变这些基因的转录活性——它通过降解既有蛋白起作用——且对缺乏 HER2 或 EGFR 的细胞无明显毒性,提示其具有一定选择性。
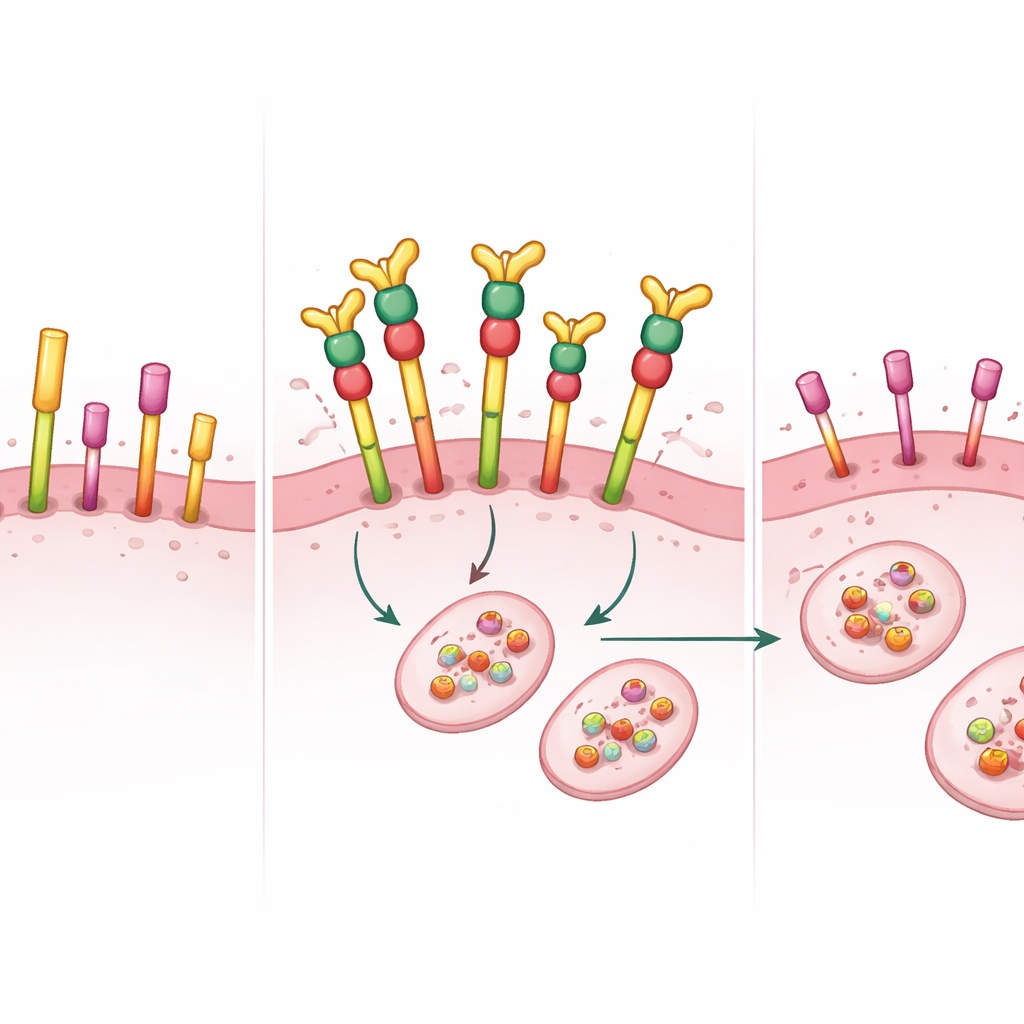
在小鼠肿瘤模型中的强大效果
研究团队随后转向更具真实感的模型:在小鼠乳腺组织内生长的肿瘤。在一项细胞系异种移植模型和一项携带扩增的 HER2 与 EGFR 且对曲妥珠单抗与图卡替尼耐药的患者来源肿瘤模型中,标准药物未能阻止肿瘤生长。形成鲜明对比的是,PEPDG278D 与一种用于稳定其在血液中避免迅速降解的抗体联合给药,导致肿瘤快速且常为完全的退缩。在患者来源模型中,所有肿瘤在约两周内消失,并在停药后 72 天的随访期内未复发。肿瘤样本显示,HER2、p95HER2、EGFR 及其下游信号通路蛋白在蛋白水平上基本被关闭。
这对患者意味着什么
这些发现表明,即便产生 p95HER2 并对现有药物耐药,HER2 阳性乳腺癌仍然在很大程度上依赖 HER2 与 EGFR 蛋白的存在。通过物理移除这两种受体,PEPDG278D 同时关闭了多条生长通路并消除了麻烦的 p95HER2 片段。尽管这些工作在细胞与小鼠中完成,尚需在人类中验证安全性与有效性,但该策略指向了一个有前景的新治疗思路:与其仅阻断致癌蛋白,不如让它们彻底消失。
引用: Yang, L., Bhattacharya, A., Li, Y. et al. A degrader of HER2 and EGFR abolishes p95HER2 and shows robust antitumor efficacy in HER2-positive breast cancer. Sci Rep 16, 12890 (2026). https://doi.org/10.1038/s41598-026-47444-3
关键词: HER2 阳性乳腺癌, p95HER2, 蛋白质降解疗法, EGFR, 耐药