Clear Sky Science · ar
مُحلِّل لبروتينَي HER2 وEGFR يقضي على p95HER2 ويُظهر فعالية قوية مضادة للأورام في سرطان الثدي الإيجابي لـ HER2
لماذا هذا البحث مهم
بالنسبة لكثير من الأشخاص الذين يعانون من شكل عدواني من سرطان الثدي يُسمى المرض الإيجابي لـ HER2، حوّلت الأدوية الحديثة تشخيصًا كان مميتًا إلى حالة قابلة للعلاج. ومع ذلك لا تزال بعض الأورام تجد طرقًا للهروب من العلاج والاستمرار في النمو. يركّز هذا البحث على مُذنِبٍ عنيد بشكل خاص — شكل مُقصّر من بروتين HER2 يُدعى p95HER2 — ويقدّم دواءً تجريبيًا، PEPDG278D، يبدو أنه يُقضي على هذا طريق الهروب ويدفع حتى الأورام شديدة المقاومة إلى نقاهة مستديمة في الفئران.
شكل صعب العلاج من سرطان الثدي
حوالي واحدة من كل خمس حالات سرطان ثدي تحمل نسخًا مفرطة من جين يُدعى HER2، ما يجعل الخلايا تنمو وتتكرر أسرع مما ينبغي. تستهدف عدة أدوية ناجحة HER2 بالفعل، بما في ذلك الأجسام المضادة مثل التراستوزوماب وحبوب صغيرة الجزيء المعروفة بمثبطات التيروزين كيناز. مع ذلك، تصبح العديد من الأورام مقاومة في نهاية المطاف. سبب رئيسي لذلك هو ظهور p95HER2، وهو مقطع مُقصّر ونشط باستمرار يبقى مثبتًا في غشاء الخلية حتى بعد قطع الجزء الخارجي من HER2. يفتقر هذا المقطع إلى مواقع الارتباط المعتادة لأدوية الأجسام المضادة، ويساعد الأورام على الغزو والانتشار، وقد رُبط بسوء البقاء لدى المرضى.
الأدوية الحالية وحدودها
قارن الباحثون أولًا الأدوية القياسية المستهدفة لـ HER2 — التراستوزوماب، البرتوزوماب، توكاتينيب، واللباتينيب — في مجموعة من خطوط خلايا سرطان الثدي البشري المزروعة في المختبر. كانت هذه الخلايا تُعبر عن كمية زائدة من HER2 الكامل الطول وتنتج أيضًا كميات متفاوتة من p95HER2. بينما استطاعت الأدوية المعتمدة إبطاء النمو في بعض الخلايا، كانت تأثيراتها متواضعة وغير متسقة، لا سيما في النماذج التي تحمل عوامل مقاومة إضافية مثل طفرات في مسارات إشارات النمو. والأهم أن أياً من هذه الأدوية لم تُقلل بشكل جوهري من كمية بروتين HER2 أو p95HER2؛ في أفضل الأحوال خفّفت بعض النشاط، وفي بعض الحالات زادت حتى مستويات المقطع المزعج p95HER2.
استراتيجية جديدة: اجعل المستقبلات تختفي
يتبع PEPDG278D نهجًا مختلفًا. بدلًا من حجب نشاط HER2 فحسب، يرتبط هذا البروتين البشري المصمم بالجزء الخارجي لكل من HER2 ومستقبل النمو القريب EGFR، ويُطلق آلية لإزالتهما وتحللّهما داخل الخلية. في عدة خطوط خلايا سرطان ثدي إيجابية لـ HER2، قلّلت جرعات منخفضة جدًا من PEPDG278D النمو الخلوي بشكل حاد. أظهرت تحليلات البروتين التفصيلية أنه قضى تقريبًا كليًا على HER2 وEGFR وp95HER2، إلى جانب مفاتيح الإشارة الأساسية (مثل فسفرة AKT وERK) التي تدفع التكاثر والبقاء. ومن الجدير بالملاحظة أن PEPDG278D لم يغيّر نشاط الجينات — بل عمل عبر تحليل البروتينات الموجودة — ولم يؤذِ الخلايا التي تفتقر إلى HER2 أو EGFR، مما يشير إلى درجة من الانتقائية.
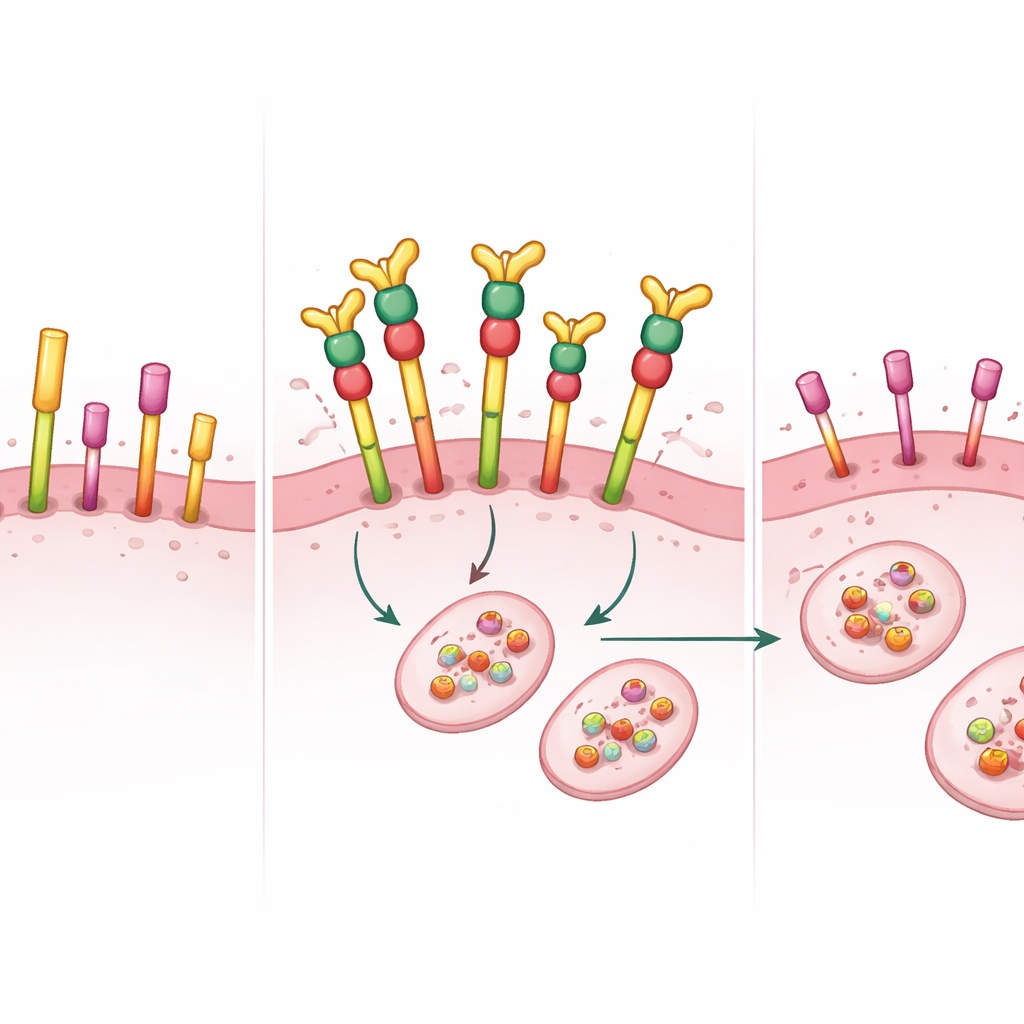
تأثيرات قوية في نماذج أورام الفئران
ثم انتقل الفريق إلى نماذج أكثر واقعية: أورام تنمو في غدد الثدي لدى الفئران. في نموذج زرع خلايا ونموذج مستمد من مريض يحمل تضخمًا في HER2 وEGFR وكان مقاومًا للتراستوزوماب والتوكاتينيب، فشلت الأدوية القياسية في إيقاف نمو الورم. وعلى النقيض اللافت، تسبب PEPDG278D، المُعطى مع جسم مضاد مُثبِّت يمنعه من التحلل السريع في الدم، في تراجع سريع وغالبًا كامل للأورام. في النموذج المستمد من المريض، اختفت جميع الأورام خلال حوالي أسبوعين ولم تعد تظهر خلال 72 يومًا من المتابعة بعد توقف العلاج. أظهرت عينات الأورام أن HER2 وp95HER2 وEGFR وشركاء إشاراتهم السفليين قد تم إيقاف تشغيلهم جوهريًا على مستوى البروتين.
ماذا قد يعني هذا للمرضى
تشير هذه النتائج إلى أن سرطانات الثدي الإيجابية لـ HER2، حتى عندما تُنتج p95HER2 وتقاوم الأدوية الحالية، تعتمد كثيرًا على وجود بروتينات HER2 وEGFR. من خلال إزالة المستقبلَين فعليًا، يوقف PEPDG278D عدة مسارات نمو مرة واحدة ويقضي على المقطع المزعج p95HER2. وبينما أُجريت هذه الدراسة في خلايا وفئران، ولا تزال السلامة والفعالية في البشر بحاجة إلى اختبار، فإنها تشير إلى استراتيجية علاجية واعدة جديدة: بدلاً من حجب البروتينات المسببة للسرطان فحسب، اجعلها تختفي تمامًا.
الاستشهاد: Yang, L., Bhattacharya, A., Li, Y. et al. A degrader of HER2 and EGFR abolishes p95HER2 and shows robust antitumor efficacy in HER2-positive breast cancer. Sci Rep 16, 12890 (2026). https://doi.org/10.1038/s41598-026-47444-3
الكلمات المفتاحية: سرطان الثدي الإيجابي لـ HER2, p95HER2, علاج تحلل البروتين, EGFR, مقاومة الدواء