Clear Sky Science · zh
一种用于评估跨内皮细胞迁移性能的深度学习方法
观察免疫细胞穿越边界
我们的身体依赖能离开血流、挤过血管内皮细胞并进入组织以抵御感染和肿瘤的游走免疫细胞。这种越境行为在实验室中很难捕捉到,尤其是在真实血流条件下。文章提出了一种新的方法,能够细致观察这一过程,并利用人工智能(AI)快速评分免疫细胞通过的情况,旨在理解胰腺癌和与年龄相关的免疫功能下降等疾病。
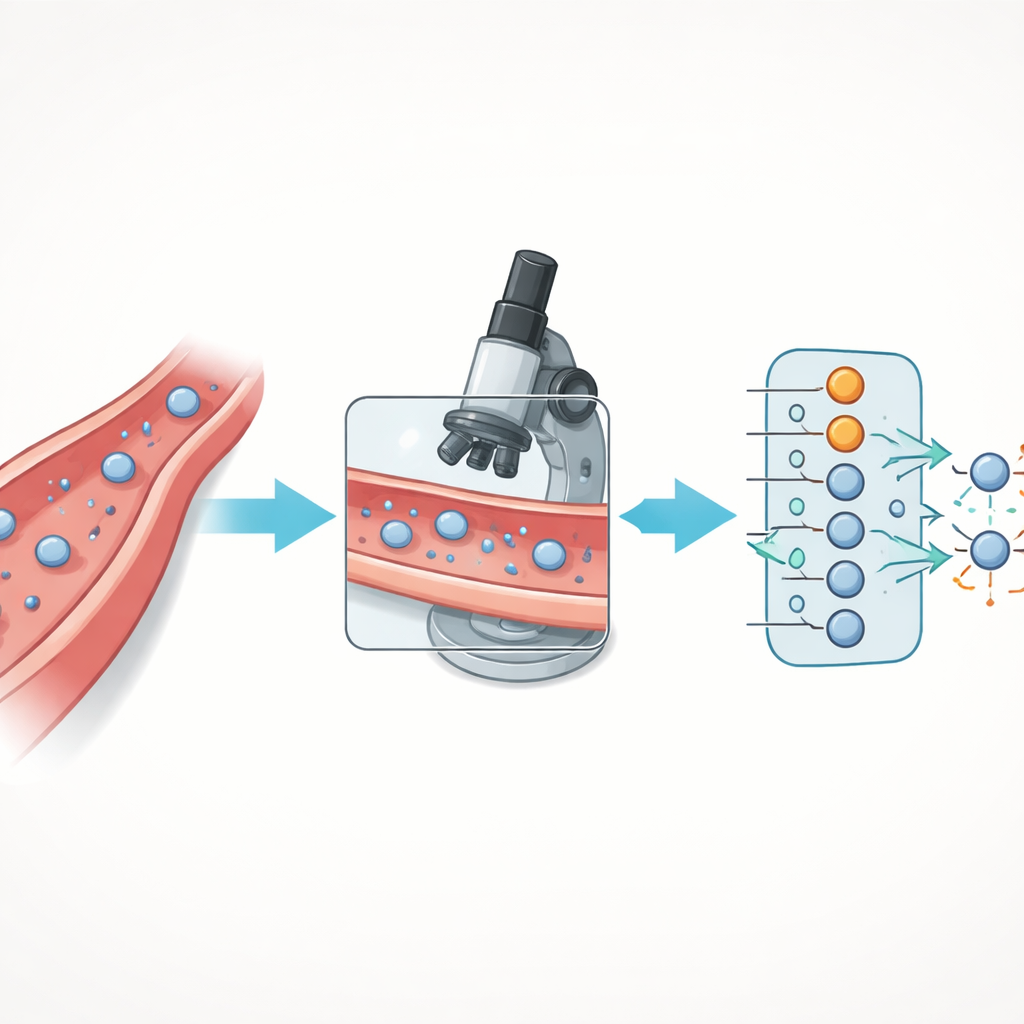
细胞如何从血管中溜出去
免疫细胞并不是随意从血管中滑出。它们遵循一系列精心编排的步骤:首先被血管壁捕获,然后沿血管壁滚动、停下、爬行,最后在内皮细胞之间或穿过内皮进入组织。这个多步骤过程称为跨内皮迁移,依赖于免疫细胞和内皮细胞表面的黏附分子和信号分子网络。当这一序列被打乱时,免疫防御可能受损,肿瘤可能能逃避免疫攻击,或过度的细胞进入会导致慢性炎症和自身免疫病。
传统实验为何不足以胜任
用于评估细胞迁移的常规实验很少能复制细胞在真实血管内遇到的力学与结构。简单的滤膜系统可以让研究者计数穿过膜的细胞数量,但这些系统主要依赖重力,无法模拟持续的血流剪切力,也无法揭示穿越序列的每一步。动物模型虽能捕捉更多复杂性,但与人类生物学不同且成本高、耗时长。更现实的方法称为基于流动的粘附测定,允许研究者在狭窄通道内培养人源内皮细胞,并在受控流动下将免疫细胞泵送经过它们。直到现在,该方法一直受限于需要对数千个细胞逐帧进行耗时且依赖操作员的人工评分。
用AI将细胞电影转化为数据
作者改进了流动测定并将其与深度学习模型配对以实现自动化分析。他们在微流控载玻片内培养人内皮细胞,刺激它们展示恰当的黏附分子,然后在活体屏障上流动荧光标记的T细胞,同时用共聚焦显微镜记录高分辨率图像。图像处理步骤去除背景噪声并分离单个T细胞,允许测量诸如细胞面积、拉长程度和轮廓圆度等简单形态特征。团队没有要求AI区分旅程中的每一个细微阶段,而是将细胞分为两个关键状态:仍在血管壁上或内嵌其中的细胞,以及已完全穿越到远侧的细胞。
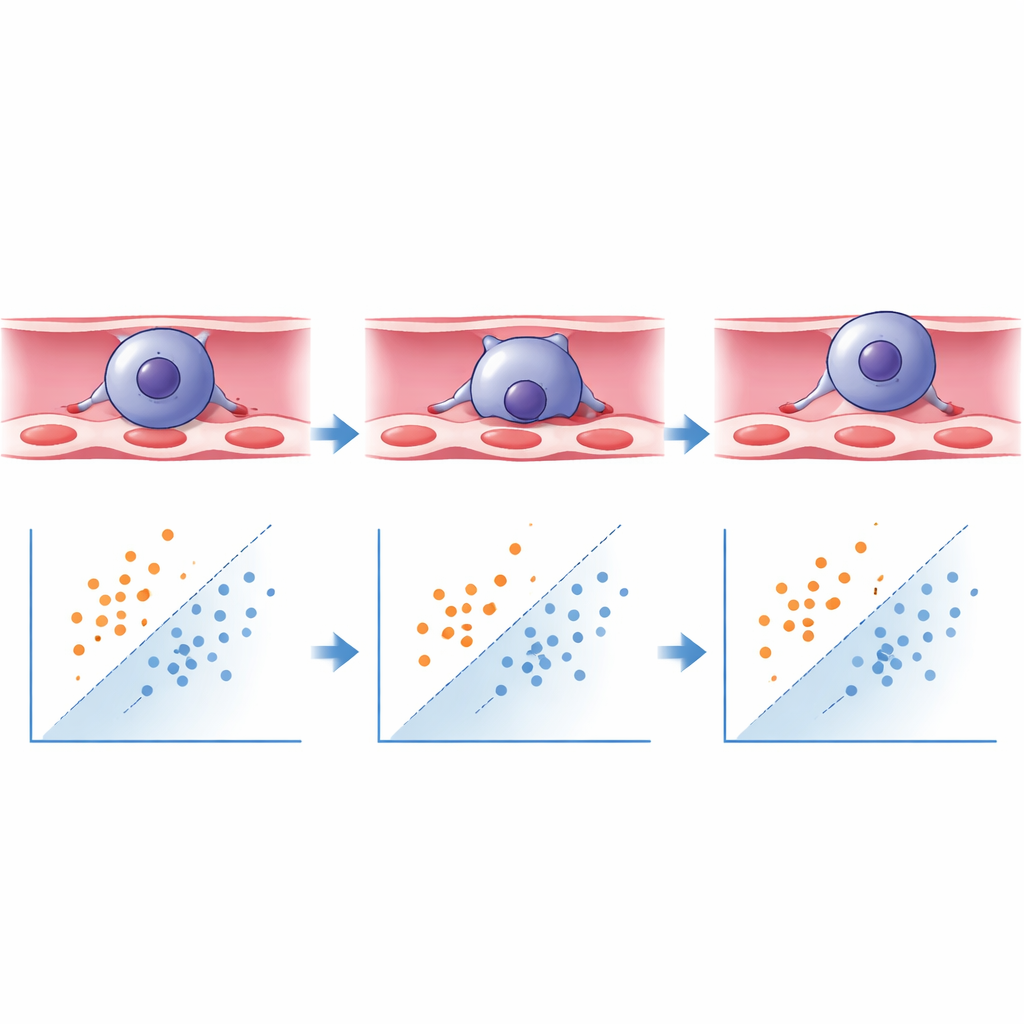
神经网络学到了什么
研究人员使用Keras/TensorFlow框架训练了一个深度学习模型,根据这些形态特征将每个分割出的细胞分类为“已穿越”或“尚未穿越”。模型学会了拉长且高纵横比的细胞更可能处于穿越过程中或已完成穿越,而更圆的细胞则倾向于仍附着在血液一侧。在对以前未见过的新图像进行测试时,该系统对已穿越细胞的识别正确率超过93%,对未穿越细胞的识别正确率约为88%,明显超出常见的可靠自动分类基准。原本需要两位盲法专家约十小时的细致人工评分现在可在数分钟内完成,且一致性更好、几乎没有操作员偏差。
测试来自健康人和癌症患者的免疫细胞
为证明该方法可应对真实世界的变异性,团队将其AI辅助测定应用于来自不同年龄和性别的健康供体的T细胞,以及来自胰腺导管腺癌患者的T细胞——该癌症以肿瘤微环境高度抑制、免疫浸润差著称。健康供体在穿越性能上未显示出明显的年龄或性别差异。相比之下,胰腺癌患者的T细胞在完成穿越内皮的能力上明显不如健康者,无论肿瘤是否携带常见的KRAS突变或患者是否接受过化疗。这些探索性结果提示,肿瘤微环境可能对免疫细胞留下持久影响,削弱其有效迁移的能力。
研究和定制免疫流动的新工具
通过将现实的基于流动的测定与深度学习结合,作者创建了一个实用平台,能够将复杂的图像序列转化为快速、标准化的细胞跨血管壁能力测量。该方法具有足够的灵活性,可重新训练以适应其他免疫细胞、肿瘤细胞或器官特异性的内皮层,并可望在未来扩展到更复杂的三维血管模型。对非专业读者来说,关键信息是:观察和评分免疫细胞迁移不再需要缓慢的人工操作;借助AI,它可以成为一种强健的、高通量的工具,帮助科学家探究某些免疫反应失败的原因以及新疗法如何恢复细胞到达所需组织的能力。
引用: Schumacher, T.M., Gottloeber, E.M., Koziel, E. et al. A deep learning approach to assess transendothelial cell trafficking performance. Sci Rep 16, 11602 (2026). https://doi.org/10.1038/s41598-026-46045-4
关键词: 免疫细胞迁移, 跨内皮迁移, 深度学习显微镜, 基于流动的粘附测定, 胰腺癌免疫