Clear Sky Science · de
Ein Deep‑Learning‑Ansatz zur Bewertung der transendothelialen Zellmigration
Beobachtung, wie Immunzellen die Grenze überschreiten
Unser Körper ist auf wandernde Immunzellen angewiesen, die den Blutkreislauf verlassen, sich zwischen die Gefäßwandzellen zwängen und ins Gewebe eindringen, um Infektionen und Tumore zu bekämpfen. Dieses Grenzüberqueren ist im Labor schwer zu erfassen, besonders unter realistischen Blutflussbedingungen. Der Artikel beschreibt eine neue Methode, diese Reise detailliert zu beobachten und dann künstliche Intelligenz (KI) schnell bewerten zu lassen, wie gut Immunzellen die Barriere überwinden — mit Blick auf Erkrankungen wie Bauchspeicheldrüsenkrebs und altersbedingten Immunabbau.
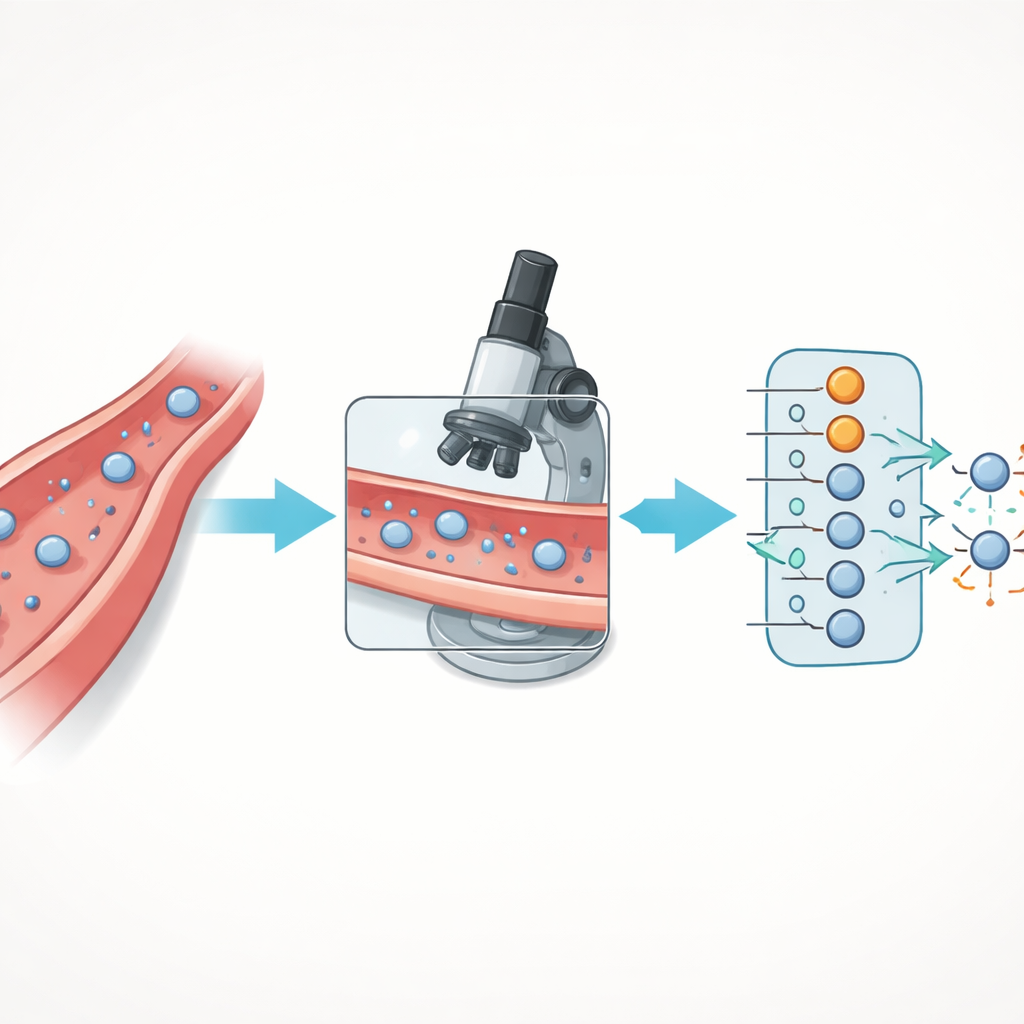
Wie Zellen aus Blutgefäßen entwischen
Immunzellen entkommen Blutgefäßen nicht zufällig. Sie folgen einer sorgfältig choreografierten Abfolge von Schritten: Zuerst werden sie an der Gefäßwand eingefangen, dann rollen sie entlang, halten an, kriechen und drücken sich schließlich zwischen oder durch die Endothelzellen, um das Gewebe dahinter zu erreichen. Diese mehrstufige Reise, transendotheliale Migration genannt, beruht auf einem Geflecht von Oberflächenverbindungen und Signalmolekülen sowohl an den Immunzellen als auch an den Gefäßwandzellen. Wird diese Abfolge gestört, können die Abwehrkräfte versagen, Tumore Angriffen entgehen oder übermäßiges Zell-Eindringen chronische Entzündungen und Autoimmunerkrankungen antreiben.
Warum traditionelle Labortests nicht ausreichen
Standard‑Assays zur Zellmigration reproduzieren selten die Kräfte und Strukturen, denen Zellen in echten Blutgefäßen ausgesetzt sind. Einfache filterbasierte Systeme erlauben das Zählen von Zellen, die durch eine Membran wandern, beruhen jedoch weitgehend auf der Schwerkraft und können die konstante Scherung des Blutflusses nicht nachahmen oder jeden Schritt der Überquerung sichtbar machen. Tiermodelle bilden mehr Komplexität ab, unterscheiden sich aber von der menschlichen Biologie und sind teuer und langsam. Eine realistischere Methode, der flussbasierte Adhäsionsassay, ermöglicht es, menschliche Endothelzellen in engen Kanälen zu kultivieren und Immunzellen unter kontrolliertem Fluss daran vorbeizupumpen. Bisher bremste diese Methode jedoch eine arbeitsintensive, operatorabhängige manuelle Auswertung von Tausenden Einzelzell‑Frames aus.
Filme von Zellen in Daten verwandeln mit KI
Die Autoren verbesserten den Flussassay und kombinierten ihn mit einem Deep‑Learning‑Modell zur automatischen Analyse. Sie kultivierten menschliche Endothelzellen in mikrofluidischen Slides, stimulierten sie so, dass die passenden Oberflächenverbindungen exprimiert wurden, und leiteten dann fluoreszent markierte T‑Zellen über diese lebende Barriere, während sie hochauflösende Bilder mit einem Konfokalmikroskop aufzeichneten. Bildverarbeitungs‑Schritte entfernten Hintergrundrauschen und separierten einzelne T‑Zellen, sodass einfache Formmerkmale wie Zellfläche, Ausdehnung und Rundheit gemessen werden konnten. Statt die KI jede subtile Phase der Migration unterscheiden zu lassen, fasste das Team die Zellen zu zwei zentralen Zuständen zusammen: solche, die noch an oder in der Gefäßwand sind, und solche, die vollständig auf die andere Seite übergegangen sind.
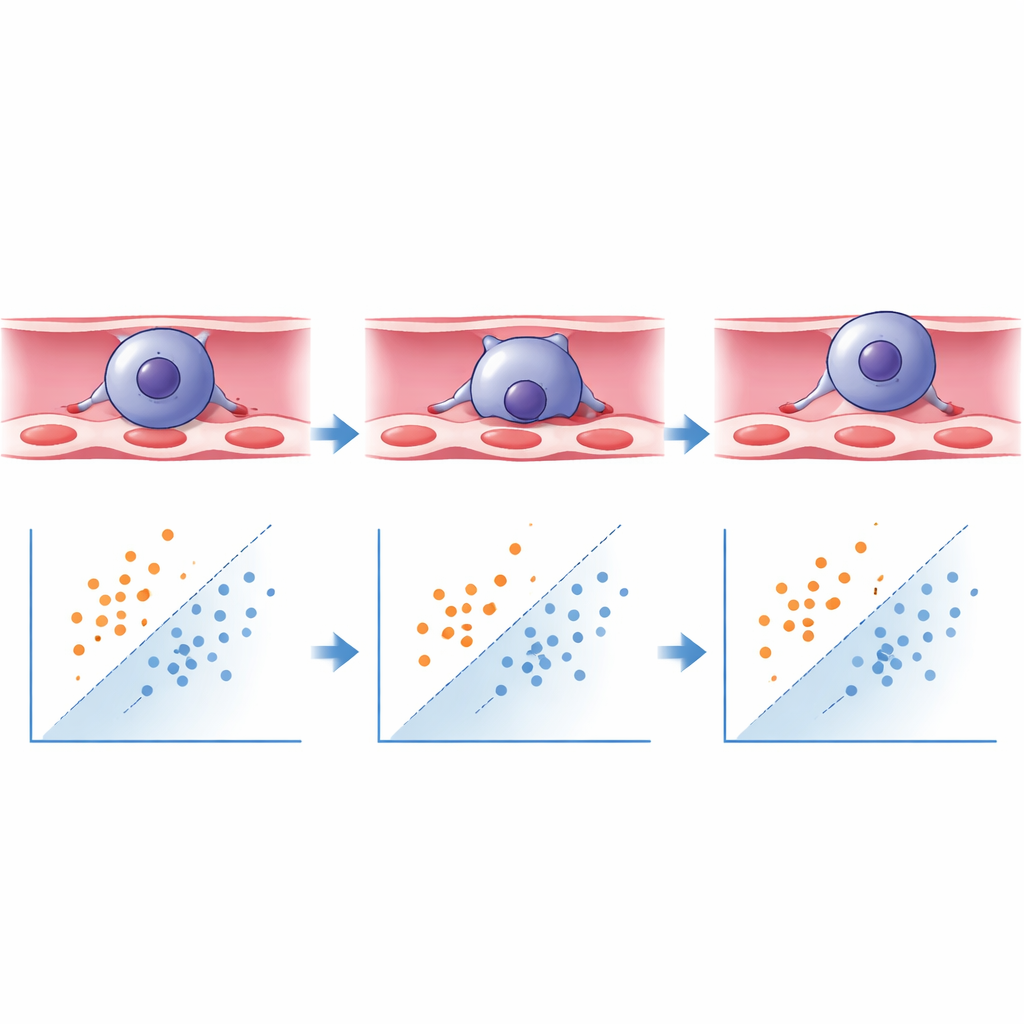
Was das neuronale Netzwerk gelernt hat
Mithilfe des Keras/TensorFlow‑Frameworks trainierten die Forschenden ein Deep‑Learning‑Modell, das jede segmentierte Zelle anhand dieser Formmerkmale als „transmigriert“ oder „noch nicht transmigriert“ klassifiziert. Das Modell erkannte, dass längliche Zellen mit hohem Seitenverhältnis eher mitten in der Überquerung oder bereits darüber hinweg waren, während rundere Zellen dazu neigten, noch auf der Blutseite angeheftet zu sein. Bei Tests an neuen, zuvor ungesehenen Bildern identifizierte das System transmigrierte Zellen mit über 93 % Genauigkeit und nicht‑transmigrierte Zellen mit etwa 88 % Genauigkeit und übertraf damit typische Benchmarks für zuverlässige automatisierte Klassifikation. Was früher rund zehn Stunden sorgfältiger manueller Auswertung durch zwei verblindete Expertinnen erforderte, lässt sich nun innerhalb von Minuten erledigen — mit verbesserter Konsistenz und praktisch ohne Bediener‑Bias.
Test an Immunzellen von Gesunden und Krebspatienten
Um zu zeigen, dass die Methode für reale Variationen geeignet ist, wandten die Autoren ihren KI‑gestützten Assay auf T‑Zellen von gesunden Spendern unterschiedlichen Alters und Geschlechts sowie auf Zellen von Patientinnen und Patienten mit duktalem Adenokarzinom der Bauchspeicheldrüse an — einem Krebs, der für ein besonders feindliches Tumormikroumfeld und geringe Immuninfiltration bekannt ist. Bei gesunden Spendern gab es keine wesentlichen Unterschiede in der Überquerungsleistung nach Alter oder Geschlecht. Im Gegensatz dazu waren T‑Zellen von Bauchspeicheldrüsenkrebs‑Patienten deutlich schlechter darin, die Gefäßwandzellen zu überwinden als T‑Zellen gesunder Personen — unabhängig davon, ob der Tumor eine häufige KRAS‑Mutation trug oder ob die Patientin bzw. der Patient eine Chemotherapie erhalten hatte. Diese explorativen Befunde deuten darauf hin, dass das Tumormilieu einen bleibenden Einfluss auf Immunzellen haben könnte, der ihre Fähigkeit zum effektiven Trafficking schwächt.
Ein neues Werkzeug zum Studium und zur Anpassung des Immun‑Traffickings
Durch die Kombination eines realistischen flussbasierten Assays mit Deep Learning haben die Autoren eine praktische Plattform geschaffen, die komplexe Bildsequenzen in schnelle, standardisierte Messungen verwandelt, wie gut Zellen Gefäßwände überqueren. Der Ansatz ist flexibel genug, um für andere Immunzellen, Tumorzellen oder organspezifische Endothelschichten neu trainiert zu werden und ließe sich künftig auf komplexere dreidimensionale Gefäßmodelle ausdehnen. Für Nicht‑Spezialisten lautet die Kernaussage: Beobachtung und Bewertung des Immunzell‑Traffickings müssen nicht länger eine langsame, manuelle Tätigkeit sein — mit KI kann es zu einem robusten, hochdurchsatzfähigen Werkzeug werden, das Forschenden hilft zu verstehen, warum manche Immunantworten versagen und wie neue Therapien die Fähigkeit der Zellen wiederherstellen könnten, die Gewebe zu erreichen, in denen sie am dringendsten gebraucht werden.
Zitation: Schumacher, T.M., Gottloeber, E.M., Koziel, E. et al. A deep learning approach to assess transendothelial cell trafficking performance. Sci Rep 16, 11602 (2026). https://doi.org/10.1038/s41598-026-46045-4
Schlüsselwörter: Trafficking von Immunzellen, transendotheliale Migration, Deep‑Learning‑Mikroskopie, flussbasierter Adhäsionsassay, Immunität bei Bauchspeicheldrüsenkrebs