Clear Sky Science · fr
Une approche par apprentissage profond pour évaluer la performance du trafic transendothélial des cellules
Observer les cellules immunitaires franchir la frontière
Notre organisme dépend de cellules immunitaires mobiles capables de quitter la circulation sanguine, de se faufiler entre les cellules qui tapissent les vaisseaux et de pénétrer dans les tissus pour lutter contre infections et cancers. Cet acte de franchissement est difficile à capturer en laboratoire, en particulier dans des conditions de flux sanguin réalistes. L’article présente une nouvelle façon d’observer ce parcours en détail puis d’utiliser l’intelligence artificielle (IA) pour évaluer rapidement dans quelle mesure les cellules immunitaires le traversent, dans l’objectif de mieux comprendre des maladies comme le cancer du pancréas et le déclin immunitaire lié à l’âge.
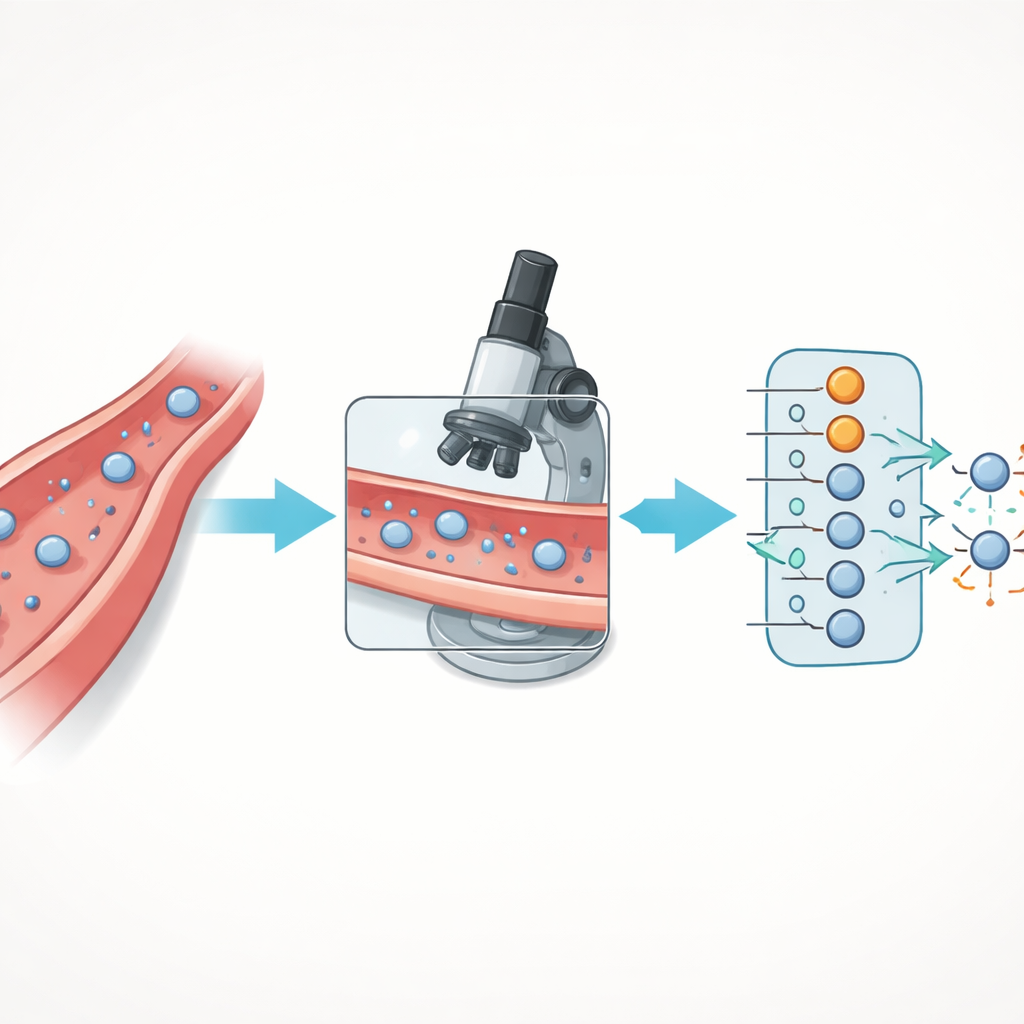
Comment les cellules sortent des vaisseaux
Les cellules immunitaires ne sortent pas des vaisseaux au hasard. Elles suivent une série d’étapes soigneusement orchestrées : d’abord elles sont capturées par la paroi vasculaire, puis elles roulent le long de celle‑ci, s’arrêtent, rampent et finalement s’insinuent entre ou à travers les cellules de l’endothélium pour atteindre le tissu en aval. Ce voyage en plusieurs étapes, appelé migration transendothéliale, repose sur un réseau d’attaches de surface et de molécules de signalisation présents à la fois sur les cellules immunitaires et sur les cellules endothéliales. Lorsque cette séquence est perturbée, les défenses immunitaires peuvent faiblir, les tumeurs échapper à l’attaque, ou une entrée cellulaire excessive peut provoquer inflammation chronique et maladies auto‑immunes.
Pourquoi les tests de laboratoire traditionnels sont insuffisants
Les tests standard de migration cellulaire reproduisent rarement les forces et les structures rencontrées dans de vrais vaisseaux sanguins. Les systèmes simples à base de filtres permettent de compter combien de cellules traversent une membrane, mais ils reposent essentiellement sur la gravité et ne peuvent imiter la contrainte de cisaillement constante du sang en écoulement ni révéler chaque étape du processus de franchissement. Les modèles animaux captent plus de complexité mais diffèrent de la biologie humaine, sont coûteux et lents. Une méthode plus réaliste, connue sous le nom d’essai d’adhésion en flux, permet de cultiver des cellules endothéliales humaines dans des microcanaux et de faire passer des cellules immunitaires au‑dessus sous flux contrôlé. Jusqu’à présent, cette méthode était limitée par un comptage manuel laborieux et dépendant de l’opérateur, frame par frame, de milliers de cellules.
Transformer des films de cellules en données avec l’IA
Les auteurs ont amélioré l’essai en flux et l’ont couplé à un modèle d’apprentissage profond pour automatiser l’analyse. Ils ont cultivé des cellules endothéliales humaines à l’intérieur de lames microfluidiques, les ont stimulées pour afficher les bons récepteurs de surface, puis ont fait circuler des lymphocytes T marqués par fluorescence au‑dessus de cette barrière vivante tout en enregistrant des images haute résolution avec un microscope confocal. Des étapes de traitement d’image ont éliminé le bruit de fond et séparé les lymphocytes T individuels, permettant de mesurer des caractéristiques de forme simples telles que la surface cellulaire, l’allongement et la circularité des contours. Plutôt que de demander à l’IA de distinguer chaque phase subtile du parcours, l’équipe a regroupé les cellules en deux états clés : celles qui sont encore sur ou dans la paroi vasculaire et celles qui ont entièrement traversé vers le côté opposé.
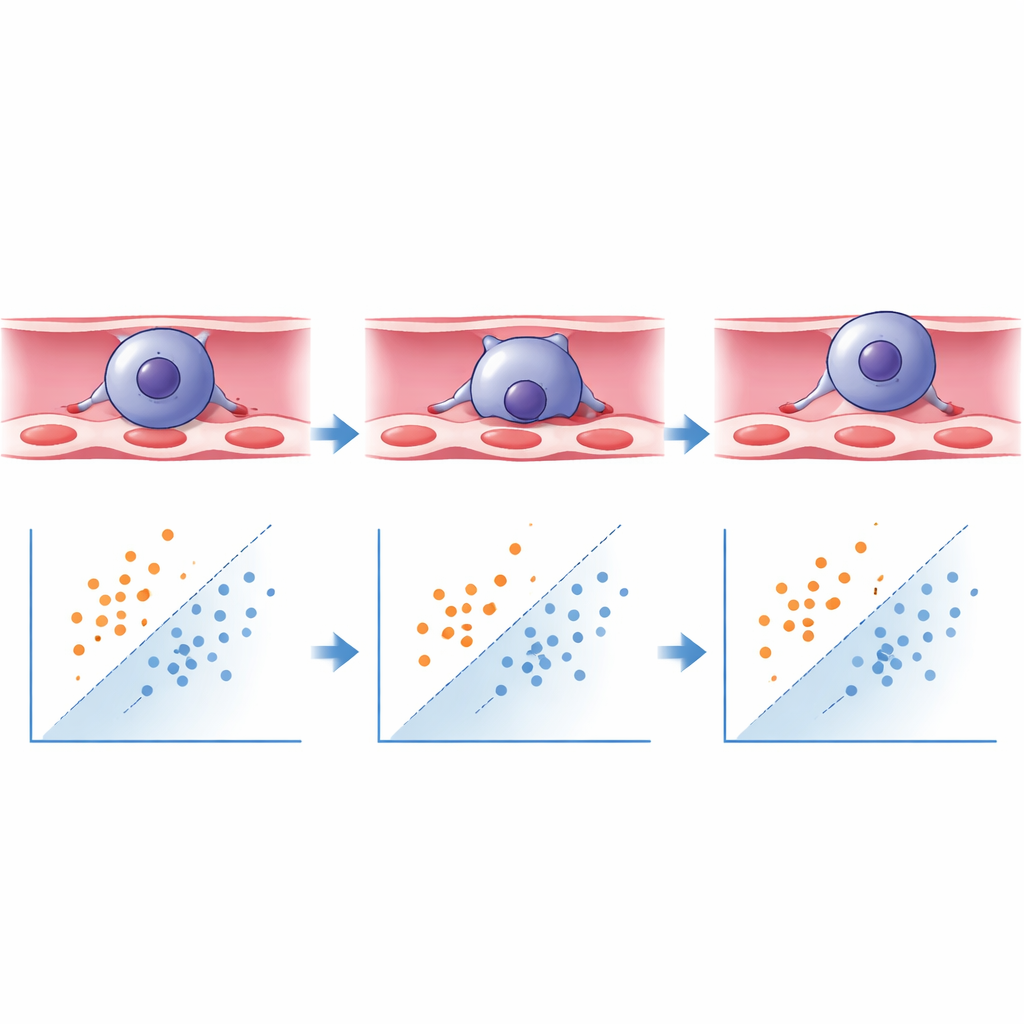
Ce que le réseau neuronal a appris
En utilisant le framework Keras/TensorFlow, les chercheurs ont entraîné un modèle d’apprentissage profond à classer chaque cellule segmentée comme « transmigrée » ou « pas encore transmigrée » en se basant sur ces caractéristiques de forme. Le modèle a appris que les cellules allongées avec un rapport d’aspect élevé avaient plus de chances d’être en cours de traversée, ou d’en être sorties, tandis que les cellules plus rondes avaient tendance à rester attachées du côté sanguin. Testé sur des images nouvelles et non vues auparavant, le système a identifié correctement les cellules transmigrées avec plus de 93 % de précision et les cellules non transmigrées avec environ 88 % de précision, dépassant nettement les seuils usuels pour une classification automatique fiable. Ce qui nécessitait auparavant près de dix heures de comptage manuel attentif par deux experts en aveugle peut désormais être réalisé en quelques minutes, avec une meilleure cohérence et quasiment sans biais opérateur.
Tester les cellules immunitaires de personnes saines et de patients atteints de cancer
Pour montrer que la méthode fonctionne malgré la variabilité du monde réel, l’équipe a appliqué son essai assisté par IA à des lymphocytes T de donneurs sains de différents âges et sexes, ainsi qu’à des patients atteints d’adénocarcinome canalaire pancréatique, un cancer connu pour son microenvironnement tumoral très hostile et sa faible infiltration immunitaire. Les donneurs sains n’ont montré aucune différence majeure de performance de franchissement liée à l’âge ou au sexe. En revanche, les lymphocytes T des patients atteints de cancer du pancréas étaient nettement moins aptes à terminer le passage à travers les cellules endothéliales que ceux des personnes saines, que la tumeur porte ou non une mutation KRAS fréquente ou que le patient ait reçu une chimiothérapie. Ces résultats exploratoires suggèrent que le microenvironnement tumoral peut laisser une empreinte durable sur les cellules immunitaires, affaiblissant leur capacité à migrer efficacement.
Un nouvel outil pour étudier et ajuster le trafic immunitaire
En associant un essai en flux réaliste à l’apprentissage profond, les auteurs ont créé une plateforme pragmatique qui transforme des séquences d’images complexes en mesures rapides et standardisées de la capacité des cellules à franchir les parois vasculaires. L’approche est suffisamment flexible pour être réentraînée sur d’autres types de cellules immunitaires, des cellules tumorales ou des couches endothéliales spécifiques d’organes, et pourrait être étendue à des modèles vasculaires tridimensionnels plus complexes à l’avenir. Pour les non‑spécialistes, le message clé est que l’observation et l’évaluation du trafic des cellules immunitaires n’ont plus besoin d’être un artisanat lent et manuel : grâce à l’IA, cela peut devenir un outil robuste et à haut débit qui aide les scientifiques à comprendre pourquoi certaines réponses immunes échouent et comment de nouveaux traitements pourraient restaurer la capacité des cellules à atteindre les tissus où elles sont le plus nécessaires.
Citation: Schumacher, T.M., Gottloeber, E.M., Koziel, E. et al. A deep learning approach to assess transendothelial cell trafficking performance. Sci Rep 16, 11602 (2026). https://doi.org/10.1038/s41598-026-46045-4
Mots-clés: trafic des cellules immunitaires, migration transendothéliale, microscopie par apprentissage profond, essai d'adhésion en flux, immunité du cancer du pancréas