Clear Sky Science · sv
En djupinlärningsmetod för att bedöma transendotelial cellsignaleringens genomförande
Att iaktta immunceller korsa gränsen
Våra kroppar är beroende av rörliga immunceller som kan lämna blodomloppet, pressa sig mellan fartygens beklädnadsceller och komma in i vävnader för att bekämpa infektioner och cancer. Denna gränsöverskridande handling är svår att fånga i laboratoriet, särskilt under realistiska blodflödesförhållanden. Artikeln presenterar ett nytt sätt att i detalj följa denna resa och låta artificiell intelligens (AI) snabbt bedöma hur väl immuncellerna lyckas ta sig över, med sikte på att bättre förstå sjukdomar som pankreascancer och åldersrelaterad nedsatt immunförsvar.
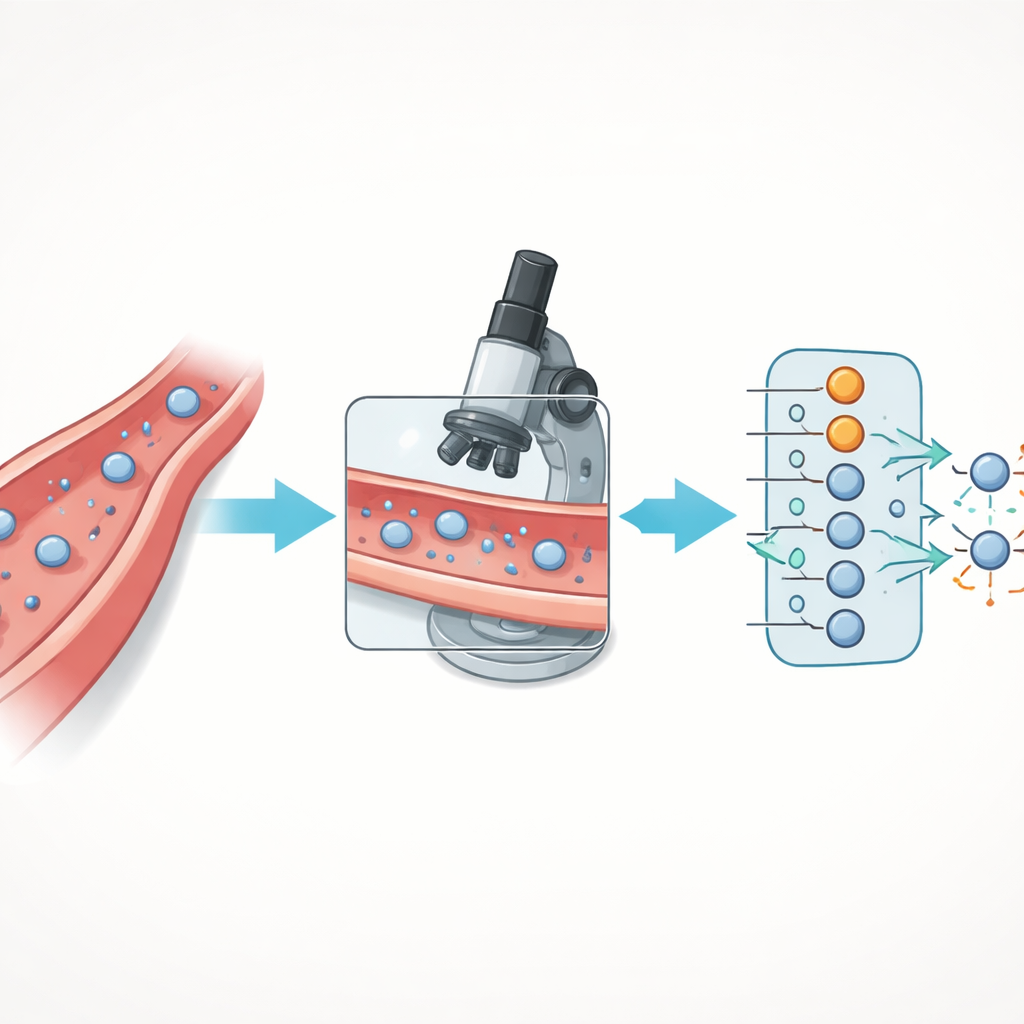
Hur celler smyger ut ur blodkärl
Immunceller lämnar inte blodkärl på måfå. De följer en noggrant koreograferad serie steg: först fångas de av kärlväggen, sedan rullar de längs den, stannar, kryper och slutligen pressar sig mellan eller genom beklädnadscellerna för att nå vävnaden bortom. Denna mångstegsresa, kallad transendotelial migration, bygger på ett nätverk av ytfästen och signalmolekyler på både immuncellerna och kärlcellernas yta. När denna sekvens störs kan det försämra immunförsvaret, göra att tumörer undviker attack eller att överdriven cellextravasation driver kronisk inflammation och autoimmuna sjukdomar.
Varför traditionella laboratorietester inte räcker till
Standardmetoder för att mäta cellmigration återskapar sällan de krafter och strukturer som cellerna möter i verkliga blodkärl. Enkla filterbaserade system låter forskare räkna hur många celler som passerar ett membran, men de förlitar sig i huvudsak på gravitation och kan inte efterlikna den konstanta skjuvning som följer av blodflöde eller avslöja varje steg i korsningssekvensen. Djurmodeller fångar mer komplexitet men skiljer sig från mänsklig biologi och är dyra och tidskrävande. En mer realistisk metod, känd som ett flödesbaserat adhesionstest, gör det möjligt att odla mänskliga kärlbeklädnadsceller i smala kanaler och pumpa immunceller förbi dem under kontrollerat flöde. Fram till nu har denna metod hållits tillbaka av tidskrävande, operatörsberoende manuell bedömning av tusentals celler bildruta för bildruta.
Att göra filmer av celler till data med AI
Författarna uppgraderade flödesassayet och kombinerade det med en djupinlärningsmodell för att automatisera analysen. De odlade mänskliga endotelceller i mikrofluidiska slides, stimulerade dem att visa rätt ytfästen och lät sedan fluorescensmärkta T‑celler strömma över denna levande barriär medan de spelade in högupplösta bilder med en konfokalmikroskop. Bildbehandlingssteg avlägsnade bakgrundsbrus och separerade individuella T‑celler, vilket gjorde det möjligt att mäta enkla formegenskaper som cellarea, hur långsträckta de var och hur runda deras konturer såg ut. Istället för att be AI:n skilja varje subtil fas av resan grupperade teamet cellerna i två nyckeltilstånd: de som fortfarande var på eller i kärlväggen och de som helt hade korsat till andra sidan.
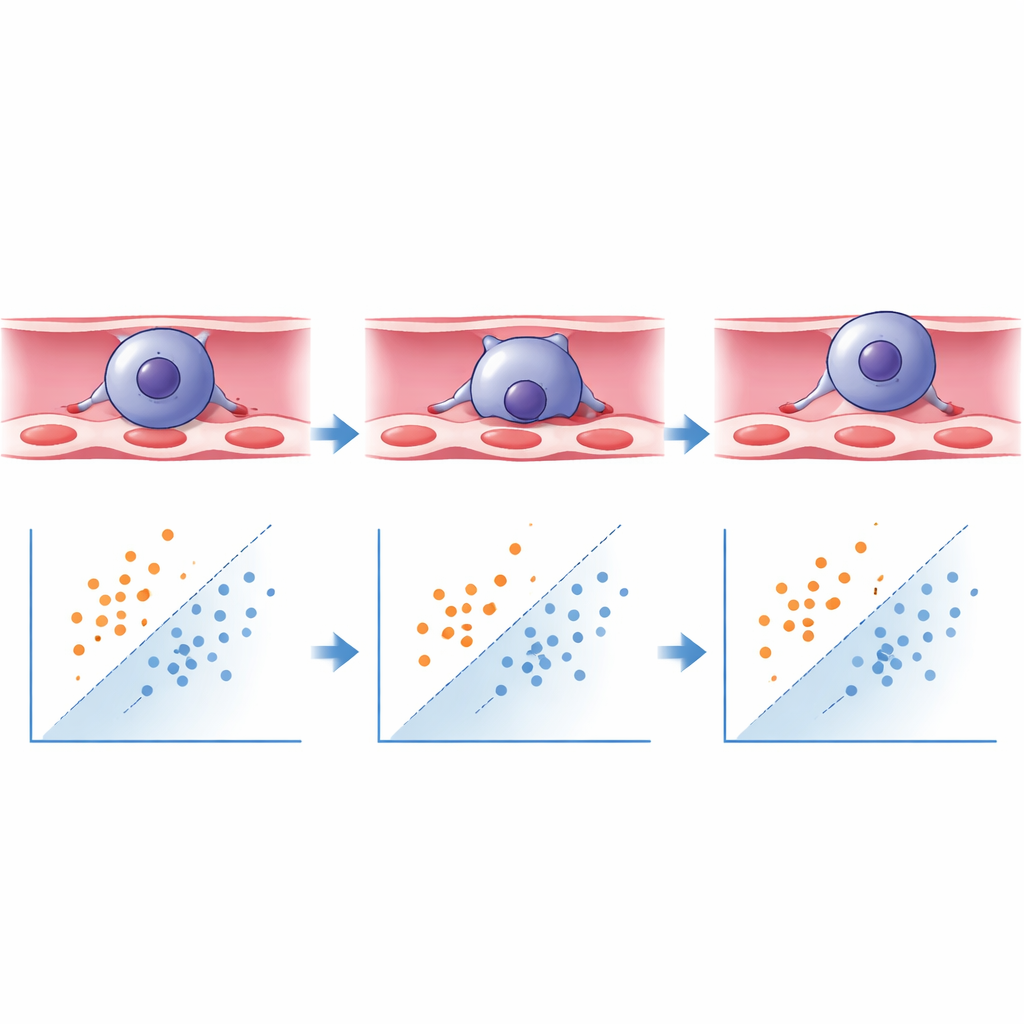
Vad neuronnätet lärde sig
Med hjälp av Keras/TensorFlow‑ramverket tränade forskarna en djupinlärningsmodell för att klassificera varje segmenterad cell som ”transmigration utförd” eller ”ännu inte transmigrerad” baserat på dessa formegenskaper. Modellen lärde sig att långsträckta celler med hög längd‑till‑bredd‑kvot var mer sannolika att vara mitt i, eller klara med, korsningen, medan rundare celler tenderade att fortfarande vara fästa på blodsidan. När systemet testades på nya, tidigare osedda bilder identifierade det transmigrerade celler korrekt med över 93 % noggrannhet och icke‑transmigrerade celler med cirka 88 % noggrannhet, vilket med god marginal överstiger vanliga riktmärken för tillförlitlig automatisk klassificering. Vad som tidigare krävde omkring tio timmars noggrant manuellt arbete av två blinda experter kan nu göras på minuter, med förbättrad konsistens och praktiskt taget utan operatörsbias.
Testning av immunceller från friska personer och cancerpatienter
För att visa att metoden fungerar över verklig variation tillämpade teamet sitt AI‑assisterade assay på T‑celler från friska givare i olika åldrar och av båda könen, samt från patienter med pankreatisk ductal adenom, en cancer känd för sin starkt ogynnsamma tumörmiljö och svaga immuncellsinfiltration. Friska givare visade inga större skillnader i korsningsförmåga beroende på ålder eller kön. Däremot var T‑celler från patienter med pankreascancer markant sämre på att slutföra resan över kärlbeklädnadscellerna än T‑celler från friska personer, oavsett om tumören bar den vanliga KRAS‑mutationen eller om patienten hade genomgått cytostatikabehandling. Dessa explorativa resultat antyder att tumörmiljön kan lämna ett varaktigt avtryck på immunceller som försvagar deras förmåga att traffikera effektivt.
Ett nytt verktyg för att studera och skräddarsy immultrafiken
Genom att förena ett realistiskt flödesbaserat assay med djupinlärning har författarna skapat en praktisk plattform som förvandlar komplexa bildsekvenser till snabba, standardiserade mått på hur väl celler korsar kärlväggar. Metoden är tillräckligt flexibel för att tränas om för andra immunceller, tumörceller eller organspecifika endotelager, och kan i framtiden utvidgas till mer komplexa tredimensionella kärlmodeller. För icke‑specialister är huvudbudskapet att iakttagande och bedömning av immuncellstrafik inte längre behöver vara ett långsamt, manuellt hantverk: med AI kan det bli ett robust, höggenomströmningsverktyg som hjälper forskare att undersöka varför vissa immunrespons misslyckas och hur nya behandlingar kan återställa cellernas förmåga att nå de vävnader där de behövs mest.
Citering: Schumacher, T.M., Gottloeber, E.M., Koziel, E. et al. A deep learning approach to assess transendothelial cell trafficking performance. Sci Rep 16, 11602 (2026). https://doi.org/10.1038/s41598-026-46045-4
Nyckelord: immuncellsframdrift, transendotelial migration, djupinlärningmikroskopi, flödesbaserat adhesionstest, immunitet vid pankreascancer