Clear Sky Science · nl
Een deep learning-benadering om transendotheliale celtrafficking te beoordelen
Immune cellen zien de grens oversteken
Ons lichaam is afhankelijk van rondzwervende immuuncellen die de bloedbaan kunnen verlaten, zich tussen de cellen die de bloedvaten bekleden kunnen wringen en weefsels binnendringen om infecties en kankers te bestrijden. Deze grensoverschrijdende handeling is moeilijk vast te leggen in het laboratorium, zeker onder realistische bloedstroomcondities. Het artikel beschrijft een nieuwe manier om deze reis in detail te volgen en vervolgens kunstmatige intelligentie (AI) snel te laten bepalen hoe goed immuuncellen de oversteek maken, met het oog op het begrijpen van ziekten zoals alvleesklierkanker en leeftijdsgerelateerde achteruitgang van het immuunsysteem.
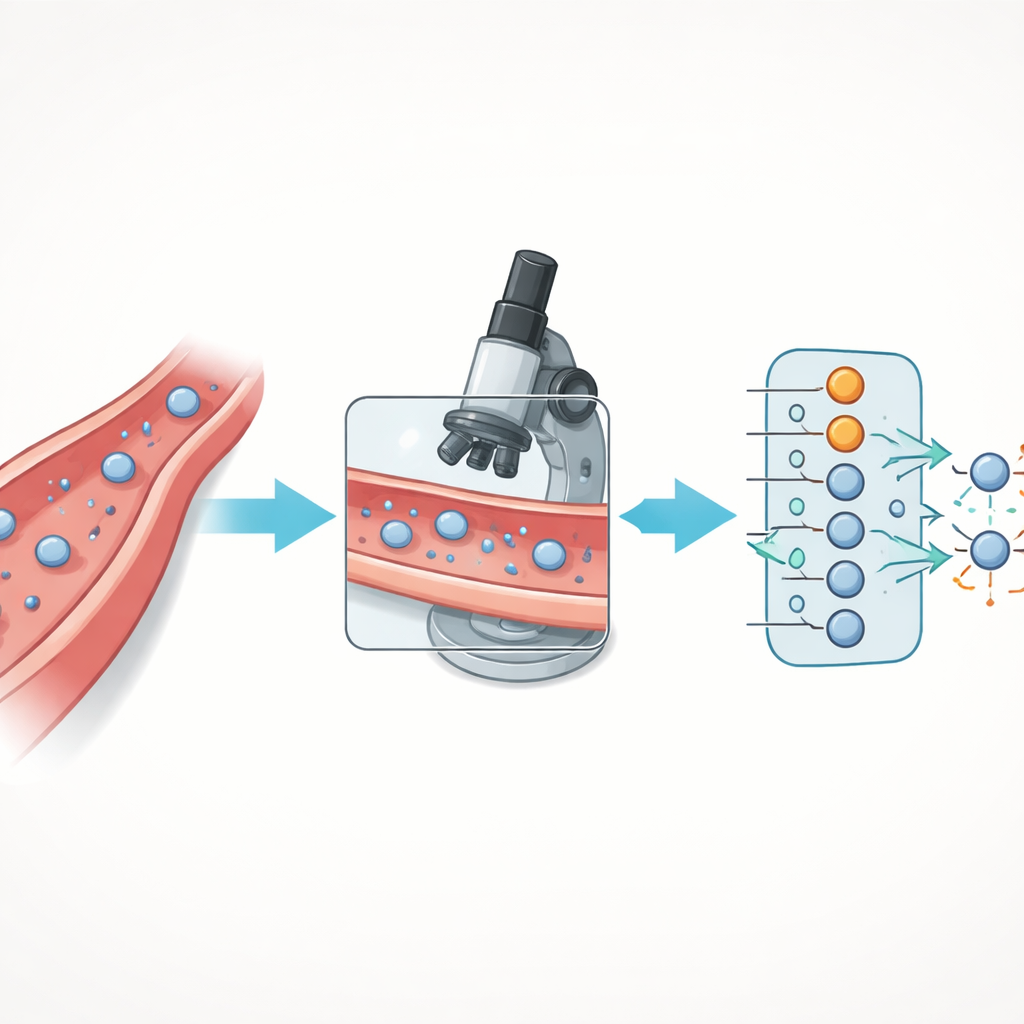
Hoe cellen uit bloedvaten ontsnappen
Immuuncellen glippen niet willekeurig uit bloedvaten. Ze volgen een zorgvuldig gechoreografeerde reeks stappen: eerst worden ze gevangen door de vaatwand, vervolgens rollen ze erlangs, blijven ze staan, kruipen ze en duwen ze tenslotte tussen of door de bekledende cellen om het onderliggende weefsel te bereiken. Deze meerstapsreis, transendotheliale migratie genoemd, berust op een netwerk van oppervlaktehaken en signaalmoleculen op zowel de immuuncellen als de vaatbekledende cellen. Als deze volgorde verstoord raakt, kunnen immuunverdedigingen falen, kunnen tumoren aanvallen ontlopen, of kan overdreven celtoegang chronische ontsteking en auto-immuunziekte bevorderen.
Waarom traditionele labtesten tekortschieten
Standaard laboratoriumassays voor celmigratie bootsen zelden de krachten en structuren na die cellen in echte bloedvaten tegenkomen. Eenvoudige filtersystemen laten onderzoekers tellen hoeveel cellen door een membraan bewegen, maar ze vertrouwen grotendeels op zwaartekracht en kunnen de constante schuifkracht van stromend bloed niet nabootsen of elk stadium van de oversteeksequentie zichtbaar maken. Diermodellen vangen meer complexiteit, maar verschillen van de menselijke biologie en zijn duur en traag. Een realistischer methode, de zogenoemde flow-gebaseerde adhesie-assay, stelt onderzoekers in staat menselijke vaatbekledende (endotheel)cellen in smalle kanaaltjes te laten groeien en immuuncellen eronder gecontroleerd stroomopwaarts langs te pompen. Tot nu toe werd deze methode echter beperkt door arbeidsintensieve, operatorafhankelijke handmatige scoring van duizenden cellen frame voor frame.
Films van cellen omzetten in data met AI
De auteurs verbeterden de flow-assay en combineerden deze met een deep learning-model om de analyse te automatiseren. Ze kweken menselijke endotheelcellen in microfluïdische slides, brachten ze in een staat waarin de juiste oppervlaktehaken tot expressie kwamen, en lieten vervolgens fluorescent gelabelde T-cellen over deze levende barrière stromen terwijl ze hoge-resolutiebeelden met een confocale microscoop opnamen. Beeldverwerkingsstappen verwijderden achtergrondruis en scheidden individuele T-cellen, waardoor eenvoudige vormkenmerken konden worden gemeten zoals celoppervlak, mate van uitrekking en hoe rond hun omtrek leek. In plaats van de AI te vragen elke subtiele fase van de reis te onderscheiden, groepeerden de onderzoekers cellen in twee kernstaten: die nog op of in de vaatwand zaten en die volledig naar de andere zijde waren overgestoken.
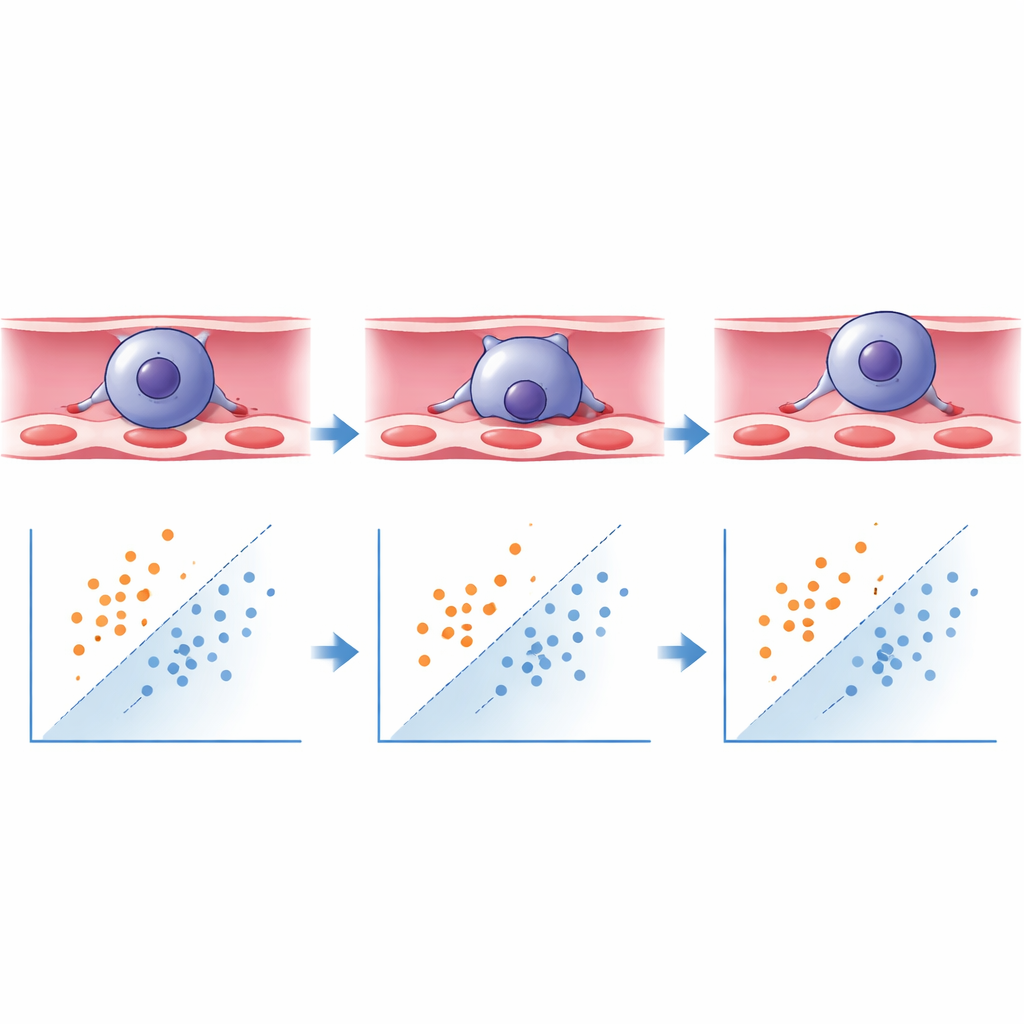
Wat het neurale netwerk leerde
Met het Keras/TensorFlow-framework trainden de onderzoekers een deep learning-model om elke gesegmenteerde cel te classificeren als "getransmigreerd" of "nog niet getransmigreerd" op basis van deze vormkenmerken. Het model leerde dat uitgerekte cellen met een hoge aspectverhouding waarschijnlijker bezig waren met, of klaar waren met, de oversteek, terwijl meer ronde cellen geneigd waren nog aan de bloedzijde vast te zitten. Bij test op nieuwe, eerder ongeziene beelden, identificeerde het systeem getransmigreerde cellen correct met meer dan 93% nauwkeurigheid en niet-getransmigreerde cellen met ongeveer 88% nauwkeurigheid, ruim boven gangbare drempels voor betrouwbare geautomatiseerde classificatie. Wat voorheen ongeveer tien uur zorgvuldige handmatige scoring door twee geblindeerde experts vergde, kan nu in enkele minuten worden uitgevoerd, met verbeterde consistentie en vrijwel geen operatorbias.
Immuuncellen testen van gezonde personen en kankerpatiënten
Om aan te tonen dat de methode werkt bij variatie uit de echte wereld, pasten de onderzoekers hun AI-ondersteunde assay toe op T-cellen van gezonde donors van verschillende leeftijden en geslachten, evenals op patiënten met pancreatisch ductaal adenocarcinoom, een kanker die bekendstaat om zijn zeer vijandige tumoromgeving en slechte immuuninfiltratie. Gezonde donors toonden geen belangrijke verschillen in oversteekprestaties naar leeftijd of geslacht. Daarentegen presteerden T-cellen van pancreaskankerpatiënten aanzienlijk slechter in het voltooien van de oversteek door de vaatbekledende cellen dan T-cellen van gezonde personen, ongeacht of de tumor een veelvoorkomende KRAS-mutatie droeg of de patiënt chemotherapie had gekregen. Deze verkennende resultaten suggereren dat de tumoromgeving mogelijk een blijvend stempel op immuuncellen achterlaat die hun vermogen om effectief te migreren verzwakt.
Een nieuw hulpmiddel om immuunverkeer te bestuderen en te sturen
Door een realistische flow-gebaseerde assay te combineren met deep learning, hebben de auteurs een praktisch platform gecreëerd dat complexe beeldreeksen omzet in snelle, gestandaardiseerde metingen van hoe goed cellen vaatwanden oversteken. De aanpak is flexibel genoeg om te worden bijgetraind voor andere immuuncellen, tumorcellen of orgaanspecifieke endotheliale lagen, en kan in de toekomst worden uitgebreid naar complexere driedimensionale vatmodellen. Voor niet-specialisten is de hoofdboodschap dat het observeren en scoren van immuuncelverkeer niet langer een langzaam, handmatig ambacht hoeft te zijn: met AI kan het een robuust, high-throughput instrument worden dat wetenschappers helpt onderzoeken waarom sommige immuunreacties falen en hoe nieuwe behandelingen het vermogen van cellen kunnen herstellen om de weefsels te bereiken waar ze het hardst nodig zijn.
Bronvermelding: Schumacher, T.M., Gottloeber, E.M., Koziel, E. et al. A deep learning approach to assess transendothelial cell trafficking performance. Sci Rep 16, 11602 (2026). https://doi.org/10.1038/s41598-026-46045-4
Trefwoorden: immuuncelverkeer, transendotheliale migratie, deep learning-microscopie, flow-gebaseerde adhesie-assay, immuniteit bij alvleesklierkanker