Clear Sky Science · zh
人乳头瘤病毒相关子宫颈腺癌侵袭模式的空间转录组学图谱
这对女性健康的重要性
人们常把宫颈癌视为单一疾病,但宫颈肿瘤的行为并不完全相同。本研究聚焦于与人乳头瘤病毒(HPV)相关的子宫颈内腺癌,提出一个简单却至关重要的问题:为什么有些肿瘤相对局限,而另一些却深度侵袭并更具危害性?通过绘制肿瘤及其周围组织不同部位的基因表达图谱,作者发现了线索,未来可能帮助医生更好地评估风险并设计更有针对性的治疗方案。
癌症扩散的不同方式
临床上已知HPV相关的子宫颈内腺癌可根据侵袭模式分为Silva A、B、C三型。A型肿瘤倾向于以成形的腺体生长并保持较好的组织学结构,而C型肿瘤则以更具破坏性、弥漫性的方式侵袭,更易转移至淋巴结并导致生存率下降。一个简化的两分法将A型和部分B型归为低风险,而C型及伴随血管侵袭的B型归为高风险。迄今仍缺乏的是对这些不同侵袭模式在分子层面上发生了什么的理解,尤其是肿瘤“生活”的邻近环境——即能够抑制或促进癌症生长的周围支持性组织和免疫细胞。
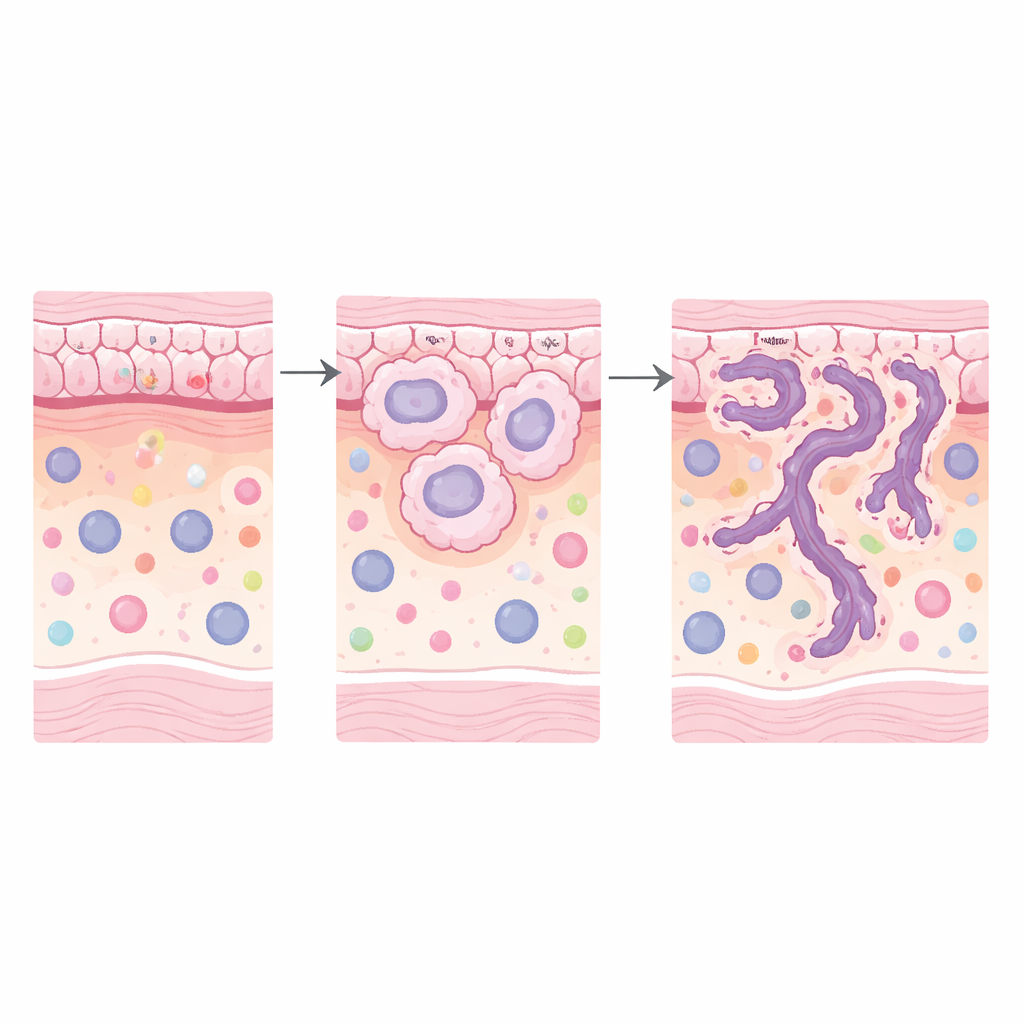
在原位读取基因活动
为了解这一点,研究者在七例外科切除的肿瘤标本上使用了空间转录组学技术,这些标本在同一组织切片内包含不止一种侵袭模式。这一巧妙设计使他们能够在同一位患者体内比较低风险与高风险区域,减少了个体间背景差异的干扰。借助GeoMX平台,他们选择了数十个小区域,既包括肿瘤细胞也包括周围的基质免疫微环境(SIME)。通过荧光标记将来自肿瘤上皮与邻近非肿瘤组织的RNA区分开来,然后对这些RNA进行测序,观察每个区室中哪些基因被激活或沉默,并用统计方法找出与高风险侵袭一致的变化。
肿瘤如何重塑其支架结构
一个引人注目的模式浮现:参与重塑机体结构支架的基因——即细胞外基质(ECM)相关基因——在高风险区域显著上调,无论是在肿瘤细胞内还是周围组织中。与基质降解、基质组织、细胞粘附及相关信号通路(包括PI3K–Akt信号)相关的途径均被激活。在癌上皮细胞中,若干关键基因尤为突出——KRT6A、TNC、LAMC2和FN1——这些基因多编码有助于细胞附着、运动或重塑周围环境的蛋白。在邻近的间质中,诸如MMP9和POSTN等基因也上调,这些基因与切割及重建基质纤维以及更具侵袭性的肿瘤行为相关。总体而言,这些变化描绘出高风险肿瘤主动在组织中开辟通路并营造有利于侵袭的微环境的图景。
助力而非阻碍的免疫细胞
在更危险的侵袭模式中,周围的免疫格局也发生了变化。SIME中的基因特征显示先天免疫臂的活性增强并且巨噬细胞的存在增加。通过计算方法,团队推断出所谓的M2样巨噬细胞——通常与伤口愈合和支持肿瘤而非攻击肿瘤相关——在高风险区域更为丰富。在蛋白水平上也得到印证:针对巨噬细胞标志CD68的组织染色显示在最具侵袭性的肿瘤模式周围巨噬细胞群体更为密集。数据表明,重塑的基质与富含巨噬细胞的间质可能协同作用,创造出有助于肿瘤更深层推进的“培养”环境。
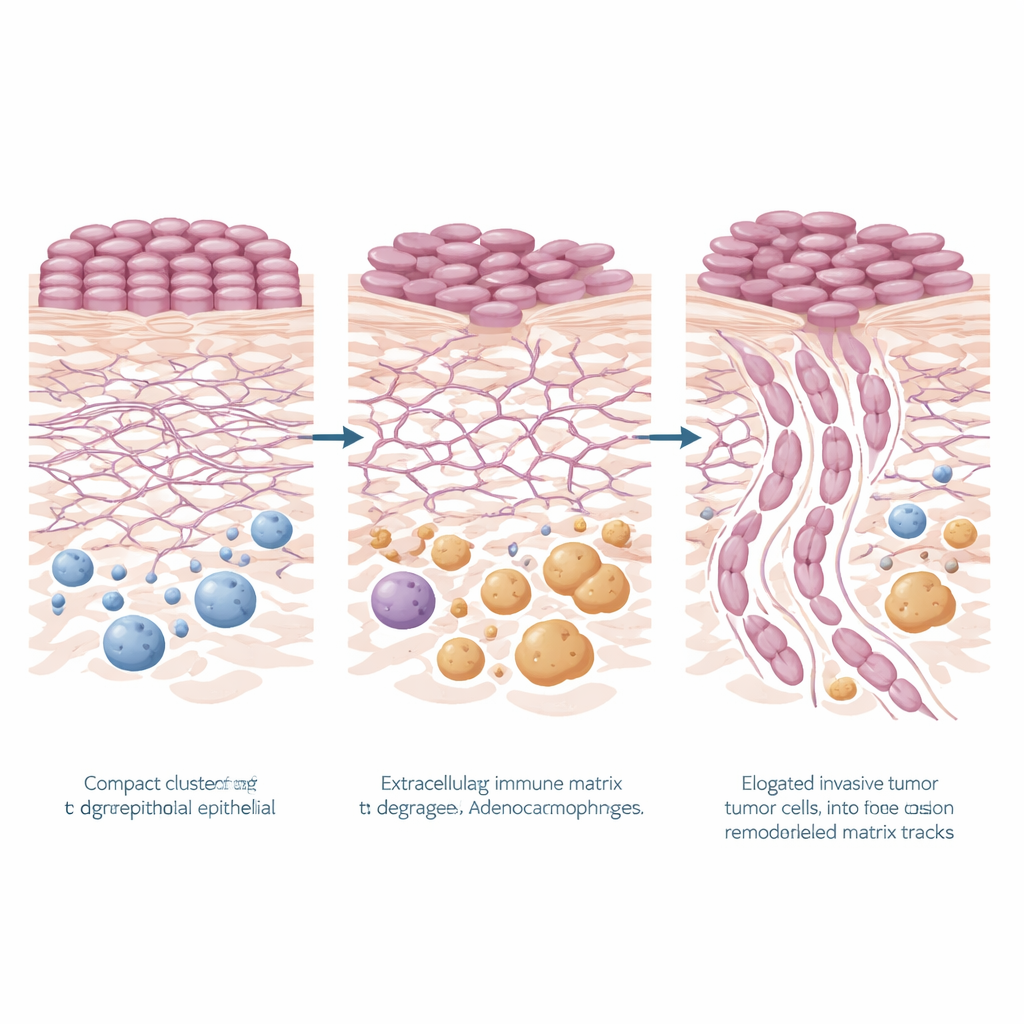
一个简单的基因评分提示风险
为评估临床影响,作者从在高风险肿瘤上皮中显著上调且在肿瘤中表达高于正常宫颈的基因中构建了一个四基因签名:KRT6A、TNC、LAMC2和FN1。他们将这些基因的表达组合为一个综合评分,并在来自癌症基因组图谱(TCGA)的一组独立宫颈腺癌样本中进行验证。即便样本量较小,评分较高的肿瘤总体生存仍呈下降趋势,并且一个阈值能够比单凭分期更好地将患者区分为低风险与高风险组。尽管样本数量有限且需在更大队列中进一步验证,这类基于基因的工具类似于已用于乳腺癌指导治疗决策的分子检测。
展望
通俗地说,这项研究表明更具危险性的HPV相关子宫颈内腺癌并非只是“更大的”安全型肿瘤;它们在生物学上存在差异。高风险区域的癌细胞与邻近组织共同重塑组织支架并招募辅助性的免疫细胞,尤其是某些巨噬细胞,以支持侵袭。由这些变化提炼出的四基因签名提示了未来:简单的分子检测可能在分期仍显早期时就标识出更有可能表现为侵袭性的肿瘤。研究结果还指向了新的治疗方向:针对细胞外基质重塑或调整先天免疫反应的药物,可能对具有该类高风险侵袭模式的女性患者具有潜在价值。
引用: Axelrod, M.L., Zhou, R. & Sun, L. Spatial transcriptomic landscape of invasion patterns in human papillomavirus-associated endocervical adenocarcinoma. Sci Rep 16, 13246 (2026). https://doi.org/10.1038/s41598-026-43717-z
关键词: 宫颈腺癌, HPV相关癌症, 肿瘤微环境, 细胞外基质重塑, 预后基因签名