Clear Sky Science · ru
Пространственный транскриптомный ландшафт паттернов инвазии при аденокарциноме эндоцервикса, связанной с вирусом папилломы человека
Почему это важно для женского здоровья
Шейный рак часто воспринимают как единое заболевание, однако опухоли шейки матки ведут себя по‑разному. В этом исследовании подробно рассматривается форма, связанная с вирусом папилломы человека (ВПЧ), — аденокарцинома эндоцервикса — и ставится простой, но ключевой вопрос: почему одни опухоли остаются относительно локализованными, тогда как другие глубоко инвазируют и становятся более опасными? Картируя, какие гены активны в разных частях опухоли и окружающей ткани, авторы обнаруживают подсказки, которые в будущем могут помочь врачам точнее прогнозировать риск и разрабатывать более целевые методы лечения.
Разные способы распространения рака
Врачам уже известно, что аденокарциномы эндоцервикса, связанные с ВПЧ, делятся на паттерны инвазии, известные как схемы Силвы A, B и C. Опухоли по типу A имеют тенденцию расти в округлых железах и оставаться более организованными, тогда как опухоли типа C проникают деструктивно и диффузно и гораздо чаще метастазируют в лимфатические узлы и ухудшают выживаемость. Упрощённая двухуровневая система относит опухоли типа A и некоторые типа B к низкому риску, а тип C и опухоли типа B с инвазией в сосуды — к высокому риску. Недостаёт понимания того, что происходит на молекулярном уровне внутри этих паттернов, особенно в живом окружении опухоли — соседней строме и иммунных клетках, которые могут либо сдерживать, либо поощрять рост рака.
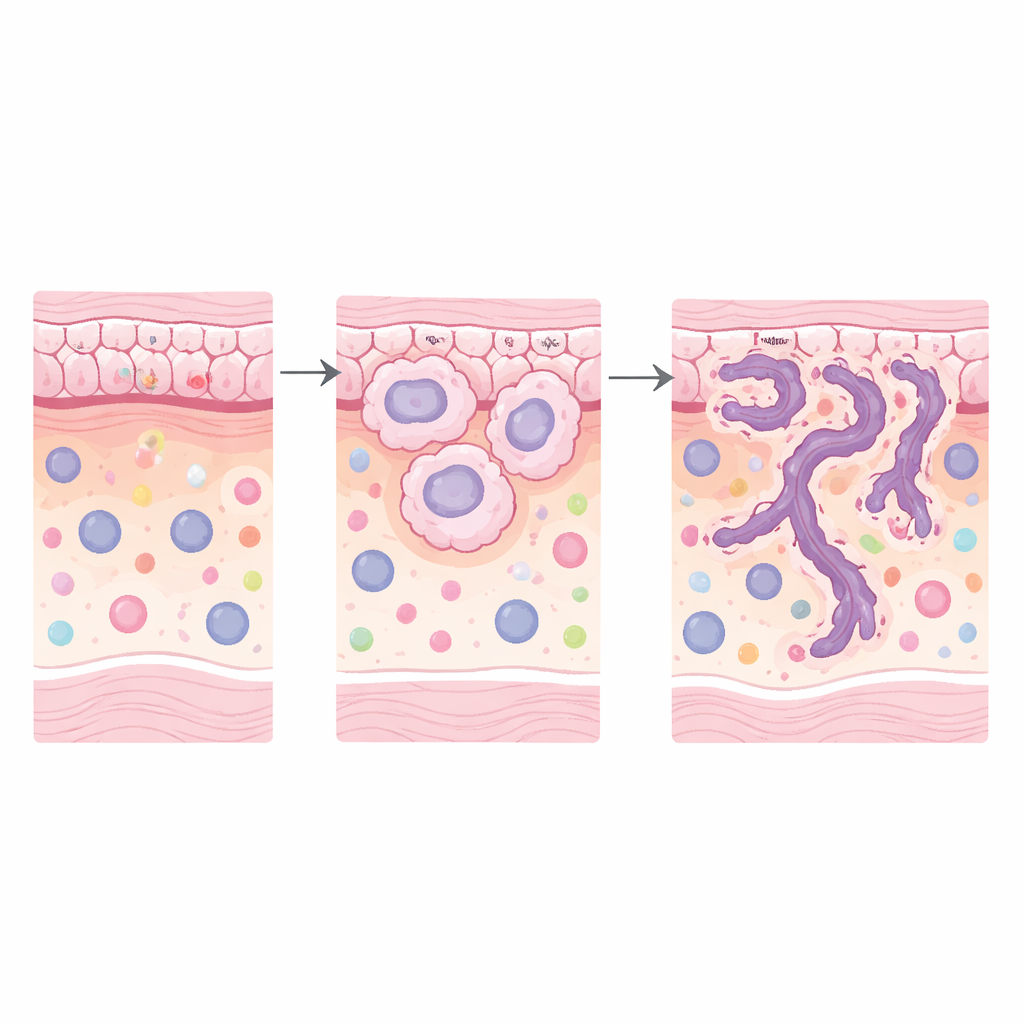
Чтение активности генов in situ
Для этого исследователи применили технологию пространственной транскриптомики к семи хирургически удалённым опухолям, в которых в одном образце присутствовало более одного паттерна инвазии. Такой подход позволил сравнить зоны низкого и высокого риска в пределах одного пациента, снизив фоновые различия между людьми. Используя платформу GeoMX, они отобрали десятки небольших областей, включающих как раковые клетки, так и окружающую стромально‑иммунную микроокружение (SIME). С помощью флуоресцентных маркеров разделяли РНК, происходящую из эпителия опухоли, и из соседней нетуморной ткани. Затем они секвенировали РНК, чтобы увидеть, какие гены включены или выключены в каждом компартменте, и применили статистические методы для выявления устойчивых изменений, связанных с инвазией высокого риска.
Как опухоль перестраивает свою «опору»
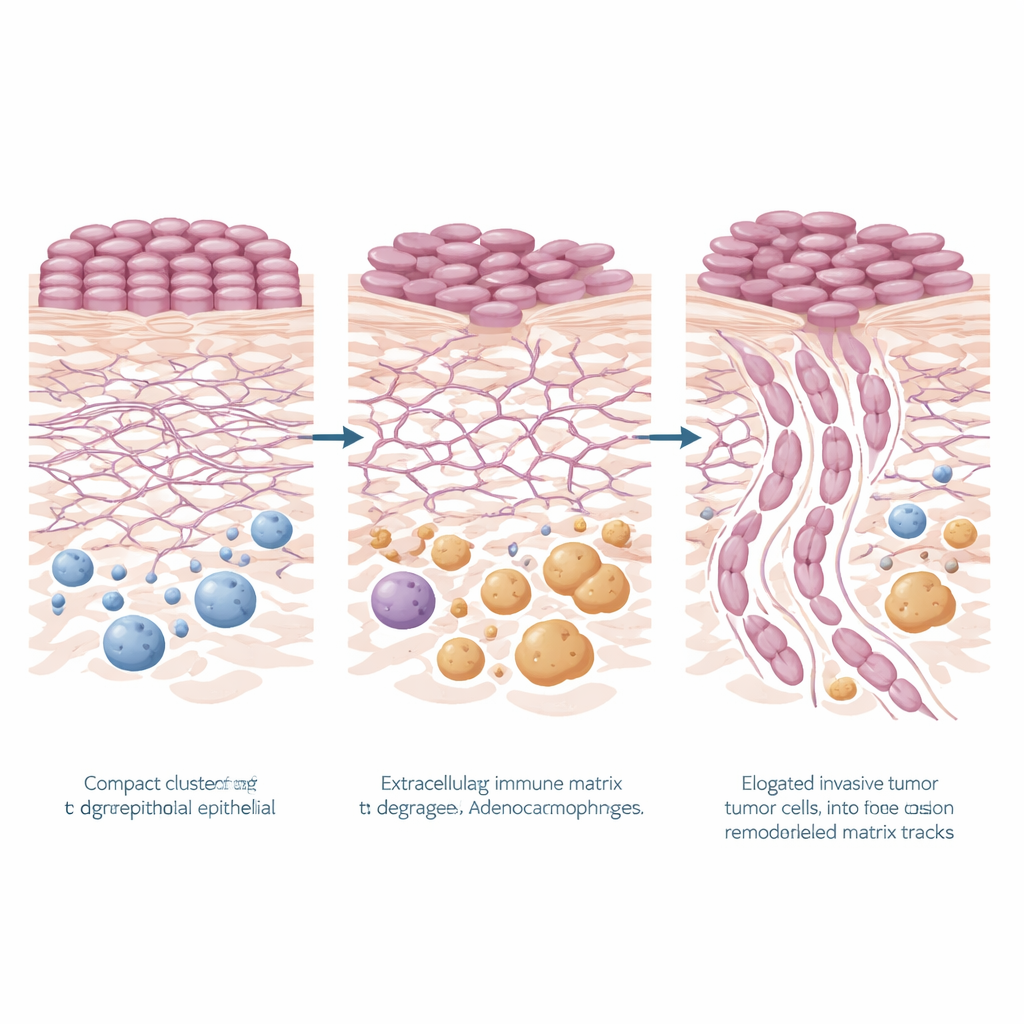
Выявился яркий паттерн: гены, связанные с ремоделированием структурной опоры организма — внеклеточного матрикса — значительно повышены в зонах высокого риска, как в самих опухолевых клетках, так и в окружающей ткани. Были активны пути, связанные с разрушением матрикса, организацией матрикса, прикреплением клеток и сопутствующей сигнализацией (включая путь PI3K–Akt). В эпителии опухоли выделялись несколько ключевых генов — KRT6A, TNC, LAMC2 и FN1 — многие из которых кодируют белки, помогающие клеткам прикрепляться, перемещаться или перестраивать своё окружение. В соседней строме также увеличивалась экспрессия генов, таких как MMP9 и POSTN, связанных с разрезанием и перестройкой волокон матрикса и более агрессивным поведением опухоли. В совокупности эти изменения рисуют картину опухолей высокого риска, активно прокладывающих пути через ткань и создающих микроокружение, благоприятное для инвазии.
Иммунные клетки, которые помогают, а не мешают
Окружающий иммунный ландшафт также изменялся в более опасных паттернах. Геновые сигнатуры в SIME указывали на усиленную активность врождённого звена иммунной системы и повышенное присутствие макрофагов, типа лейкоцитов. С помощью вычислительных методов команда предположила, что так называемые макрофаги типа M2 — часто ассоциируемые с заживлением ран и поддержкой опухоли, а не с её уничтожением — встречались чаще в регионах высокого риска. Это подтвердилось на белковом уровне: окрашивание ткани на маркер макрофагов CD68 показало более плотные популяции макрофагов вокруг наиболее инвазивных паттернов опухоли. Данные позволяют предположить, что перестроенный матрикс и строма, богатая макрофагами, могут совместно создавать питательную нишу, помогающую раку проникать глубже.
Простой геновый балл, сигнализирующий о проблеме
Чтобы оценить клиническое значение, авторы построили четырёхгенную сигнатуру из генов, сильно повышенных в эпителии опухоли высокого риска и более экспрессированных в опухоли, чем в нормальной шейке: KRT6A, TNC, LAMC2 и FN1. Они объединили экспрессию этих генов в единый балл и протестировали его на независимой выборке аденокарцином шейки матки из The Cancer Genome Atlas. Даже в этой небольшой группе опухоли с более высокими показателями склонны были к худшей общей выживаемости, и пороговое значение позволяло разделить пациентов на группы с низким и высоким риском лучше, чем стадия одна. Хотя числа невелики и требуется валидация в больших когортах, такой генетический инструмент напоминает тесты, уже применяемые в раке молочной железы для выбора лечения.
Что это значит в перспективе
Проще говоря, это исследование показывает, что более опасные аденокарциномы эндоцервикса, ассоциированные с ВПЧ, не являются просто «большими» версиями безопасных опухолей — они биологически отличаются. Зоны высокого риска характеризуются тем, что раковые клетки и соседняя ткань совместно перестраивают тканевый каркас и привлекают вспомогательные иммунные клетки, особенно определённые макрофаги, которые поддерживают инвазию. Четырёхгенная сигнатура, выделенная из этих изменений, намекает на будущее, где простые молекулярные тесты смогут выявлять пациенток с опухолями, склонными к агрессивному поведению, даже при ранней стадии. Результаты также указывают на новые терапевтические подходы: препараты, нацеленные на ремоделирование внеклеточного матрикса или перестройку врождённого иммунного ответа, могут оказаться перспективными для пациенток с паттернами инвазии высокого риска при этом типе рака шейки матки.
Цитирование: Axelrod, M.L., Zhou, R. & Sun, L. Spatial transcriptomic landscape of invasion patterns in human papillomavirus-associated endocervical adenocarcinoma. Sci Rep 16, 13246 (2026). https://doi.org/10.1038/s41598-026-43717-z
Ключевые слова: аденокарцинома шейки матки, рак, связанный с ВПЧ, опухолевый микросреда, ремоделирование внеклеточного матрикса, прогностическая геновая сигнатура