Clear Sky Science · sv
Spatialt transkriptomiskt landskap för invasionsmönster i humant papillomavirus‑associerad endocervikal adenokarcinom
Varför detta är viktigt för kvinnors hälsa
Cervixcancer uppfattas ofta som en enda sjukdom, men livmoderhalsens cancrar beter sig inte alla likadant. Denna studie granskar noggrant en form kopplad till humant papillomvirus (HPV), kallad endocervikal adenokarcinom, och ställer en enkel men avgörande fråga: varför förblir vissa tumörer relativt begränsade medan andra invaderar djupt och blir farligare? Genom att kartlägga vilka gener som är aktiva i olika delar av tumören och den omgivande vävnaden avslöjar författarna ledtrådar som en dag kan hjälpa läkare att bättre förutsäga risk och utforma mer riktade behandlingar.
Olika sätt en cancer kan sprida sig
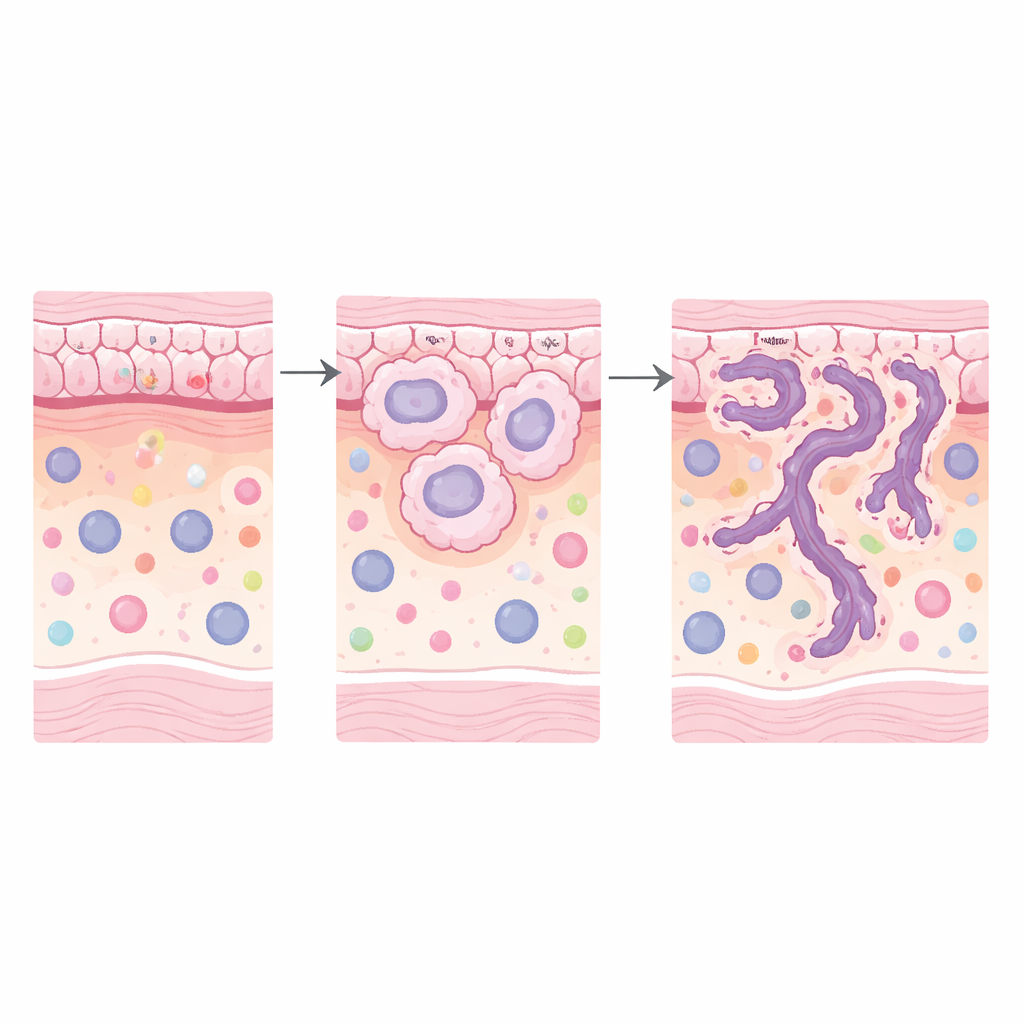
Läkare vet redan att HPV‑associerade endocervikala adenokarcinom kan grupperas i invasionsmönster, kända som Silva‑mönster A, B och C. Mönster A‑tumörer tenderar att växa i rundade körtlar och behålla ett mer organiserat utseende, medan mönster C‑tumörer invaderar på ett mer destruktivt, diffust sätt och har mycket större sannolikhet att sprida sig till lymfkörtlar och försämra överlevnaden. Ett förenklat tvåstegssystem märker mönster A och vissa B‑tumörer som lågrisk, och mönster C samt B‑tumörer med kärlinvasion som högrisk. Det som saknats är en förståelse för vad som händer på molekylär nivå i dessa olika mönster, särskilt i tumörens närmiljö — den intilliggande stödjevävnaden och immuncellerna som antingen kan hämma eller uppmuntra tumörtillväxt.
Läsa genaktivitet på plats
För att ta itu med detta använde forskarna en teknik kallad spatial transkriptomik på sju kirurgiskt avlägsnade tumörer som innehöll mer än ett invasionsmönster i samma prov. Denna smarta design gjorde det möjligt att jämföra lågrisk‑ och högriskområden inom en och samma patient och minimerade bakgrundsskillnader mellan individer. Med GeoMX‑plattformen valde de dussintals små regioner som inkluderade både cancerceller och den omgivande stromala immunsubmikromiljön (SIME). Fluorescerande markörer användes för att skilja RNA som kom från tumörepitel från RNA i närliggande icke‑tumörvävnad. De sekvenserade sedan RNA för att se vilka gener som var påslagna eller avstängda i varje compartment och använde statistiska verktyg för att hitta konsekventa förändringar kopplade till högriskinvasion.
Hur tumören omformar sitt skelett
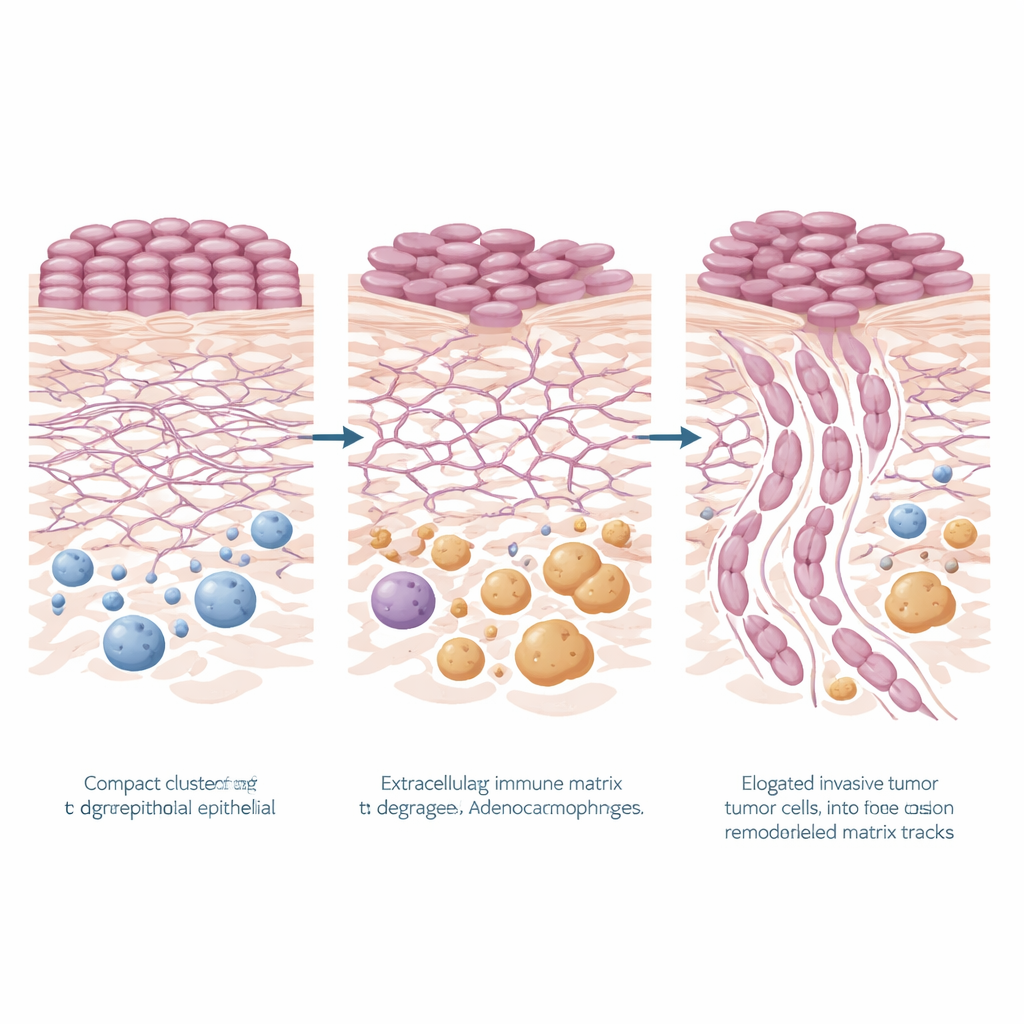
Ett slående mönster framträdde: gener involverade i ombyggnad av kroppens strukturella stomme, känd som extracellulär matrix, var kraftigt uppreglerade i högriskregioner, både i tumörcellerna och i den omgivande vävnaden. Vägar kopplade till matrixnedbrytning, matrixorganisation, cellfäste och relaterad signalering (inklusive PI3K–Akt‑signalering) var alla förhöjda. Flera nyckelgener stack ut i cancerepitelet — KRT6A, TNC, LAMC2 och FN1 — många som kodar för proteiner som hjälper celler att fästa, röra sig eller omforma sin omgivning. I den närliggande stroman var gener som MMP9 och POSTN, associerade med att klippa och bygga om matrixfibrer och med aggressivare tumörbeteende, också ökade. Tillsammans målar dessa förändringar upp en bild av högrisktumörer som aktivt skapar nya vägar genom vävnad och bygger en mikromiljö som gynnar invasion.
Immunceller som hjälper snarare än hindrar
Den omgivande immunmiljön förändrades också i de mer farliga mönstren. Gensignaturer i SIME pekade på ökad aktivitet i det medfödda immunförsvaret och en förhöjd närvaro av makrofager, en typ av vita blodkroppar. Med beräkningsmetoder drog teamet slutsatsen att så kallade M2‑liknande makrofager — ofta förknippade med sårläkning och tumörstöd snarare än attack — var mer talrika i högriskregionerna. Detta bekräftades på proteinnivå: vävnadsfärgning för CD68, en markör för makrofager, visade tätare makrofagpopulationer kring de mest invasiva tumörmönstren. Data tyder på att ombyggd matrix och makrofagrik stroma kan samverka för att skapa en näringsgivande nisch som hjälper cancern att tränga djupare.
En enkel genpoäng som signalerar fara
För att undersöka klinisk betydelse byggde författarna en fyragensigatur från de gener som var starkt uppreglerade i högrisk tumörepitel och mer uttryckta i tumör än i normal cervix: KRT6A, TNC, LAMC2 och FN1. De kombinerade uttrycket av dessa gener till en enda poäng och testade den i en oberoende uppsättning cervikala adenokarcinom från The Cancer Genome Atlas. Även i denna lilla grupp tenderade tumörer med högre poäng att ha sämre total överlevnad, och ett cut‑off‑värde kunde skilja patienter i lägre respektive högre risk bättre än stadium ensam. Även om antalen är blygsamma och behöver valideras i större kohorter, liknar denna typ av genbaserat verktyg tester som redan används vid bröstcancer för att vägleda behandlingsbeslut.
Vad allt detta betyder framöver
Enkelt uttryckt visar studien att mer farliga HPV‑associerade endocervikala adenokarcinom inte bara är "större" versioner av säkerare tumörer; de är biologiskt olika. Högriskregioner kännetecknas av att cancerceller och närliggande vävnad gemensamt omformar vävnadsstommen och rekryterar hjälparimmunceller, särskilt vissa makrofager, för att stödja invasion. Den fyragensignatur som destillerats ur dessa förändringar antyder en framtid där enkla molekylära tester kan identifiera patienter vars tumörer sannolikt kommer att bete sig aggressivt, även när stadiet ser tidigt ut. Resultaten pekar också mot nya behandlingsvägar: läkemedel som riktar in sig på ombyggnad av extracellulär matrix eller omformar det medfödda immunsvaret kan vara lovande för kvinnor med högriskinvasionsmönster i denna typ av cervixcancer.
Citering: Axelrod, M.L., Zhou, R. & Sun, L. Spatial transcriptomic landscape of invasion patterns in human papillomavirus-associated endocervical adenocarcinoma. Sci Rep 16, 13246 (2026). https://doi.org/10.1038/s41598-026-43717-z
Nyckelord: cervikal adenokarcinom, HPV‑relaterad cancer, tumörmikromiljö, ombyggnad av extracellulär matrix, prognostiskt gen‑signatur