Clear Sky Science · fr
Paysage transcriptomique spatial des modes d’invasion dans l’adénocarcinome endocervical associé au papillomavirus humain
Pourquoi cela compte pour la santé des femmes
Le cancer du col est souvent considéré comme une maladie unique, mais les cancers du col ne se comportent pas tous de la même façon. Cette étude examine de près une forme liée au papillomavirus humain (VPH), l’adénocarcinome endocervical, et pose une question simple mais cruciale : pourquoi certaines tumeurs restent relativement limitées tandis que d’autres envahissent profondément et deviennent plus dangereuses ? En cartographiant les gènes actifs dans différentes parties de la tumeur et des tissus environnants, les auteurs dégagent des indices qui pourraient, un jour, aider les cliniciens à mieux prédire le risque et à concevoir des traitements plus ciblés.
Différentes façons dont un cancer peut se propager
Les médecins savent déjà que les adénocarcinomes endocervicaux associés au VPH peuvent être classés en patterns d’invasion, appelés patterns Silva A, B et C. Les tumeurs de pattern A ont tendance à croître en glandes arrondies et à rester plus organisées, tandis que les tumeurs de pattern C envahissent de manière plus destructive et diffuse et sont beaucoup plus susceptibles de métastaser aux ganglions lymphatiques et d’aggraver le pronostic. Un système simplifié à deux niveaux regroupe les tumeurs de pattern A et certaines B comme à faible risque, et les tumeurs de pattern C ainsi que les B avec invasion vasculaire comme à haut risque. Ce qui manquait jusqu’à présent, c’est la compréhension de ce qui se passe au niveau moléculaire dans ces différents patterns, en particulier dans le voisinage vivant de la tumeur — le tissu de soutien et les cellules immunitaires proches qui peuvent soit freiner soit favoriser la croissance cancéreuse.
Lire l’activité génique in situ
Pour aborder cette question, les chercheurs ont utilisé une technologie de transcriptomique spatiale sur sept tumeurs retirées chirurgicalement qui comportaient plus d’un pattern d’invasion dans le même spécimen. Ce plan astucieux leur a permis de comparer des zones à faible et à haut risque chez un même patient, réduisant ainsi les différences de fond entre individus. Avec la plateforme GeoMX, ils ont sélectionné des dizaines de petites régions incluant à la fois les cellules tumorales et le microenvironnement stromal immunitaire (SIME). Des marqueurs fluorescents ont servi à séparer l’ARN provenant de l’épithélium tumoral de celui du tissu non tumoral adjacent. Ils ont ensuite séquencé l’ARN pour voir quels gènes étaient activés ou réprimés dans chaque compartiment et utilisé des outils statistiques pour détecter des changements cohérents associés à l’invasion à haut risque.
Comment la tumeur remodèle son échafaudage
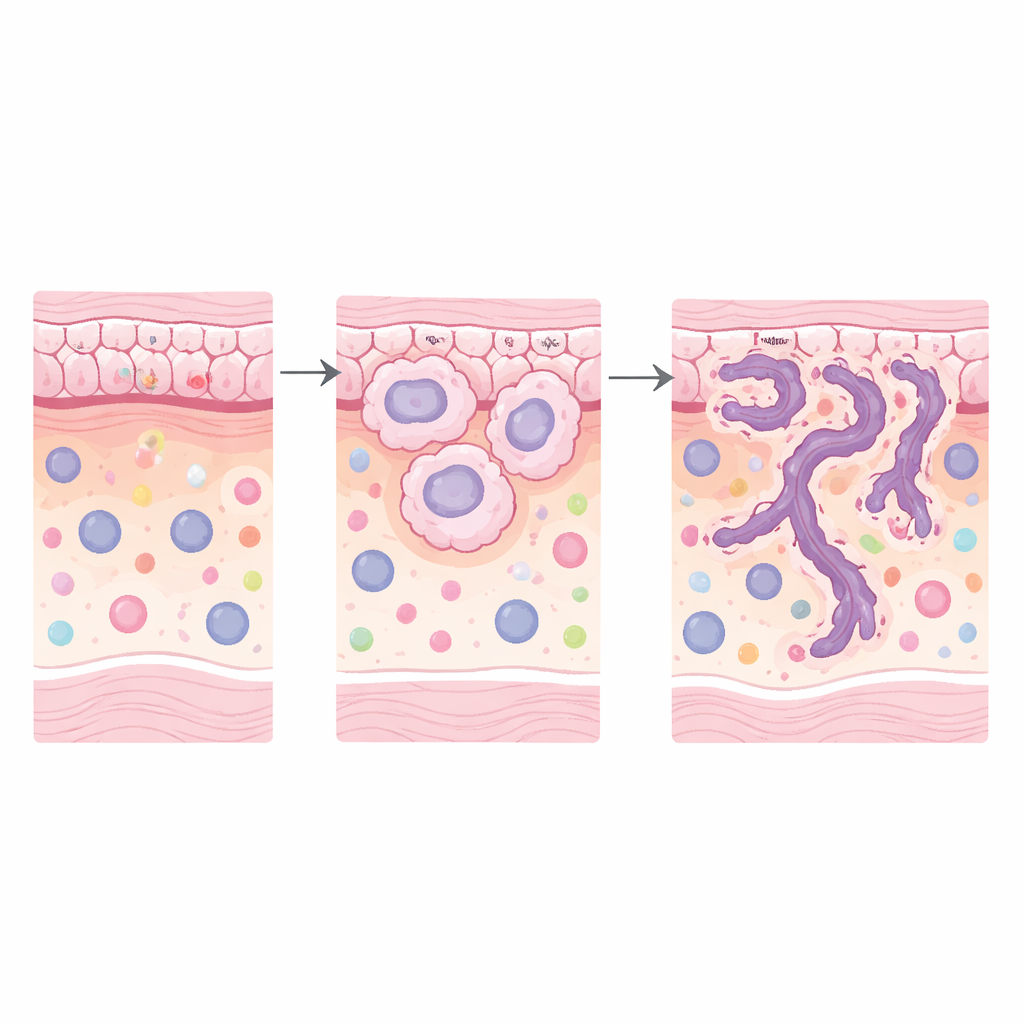
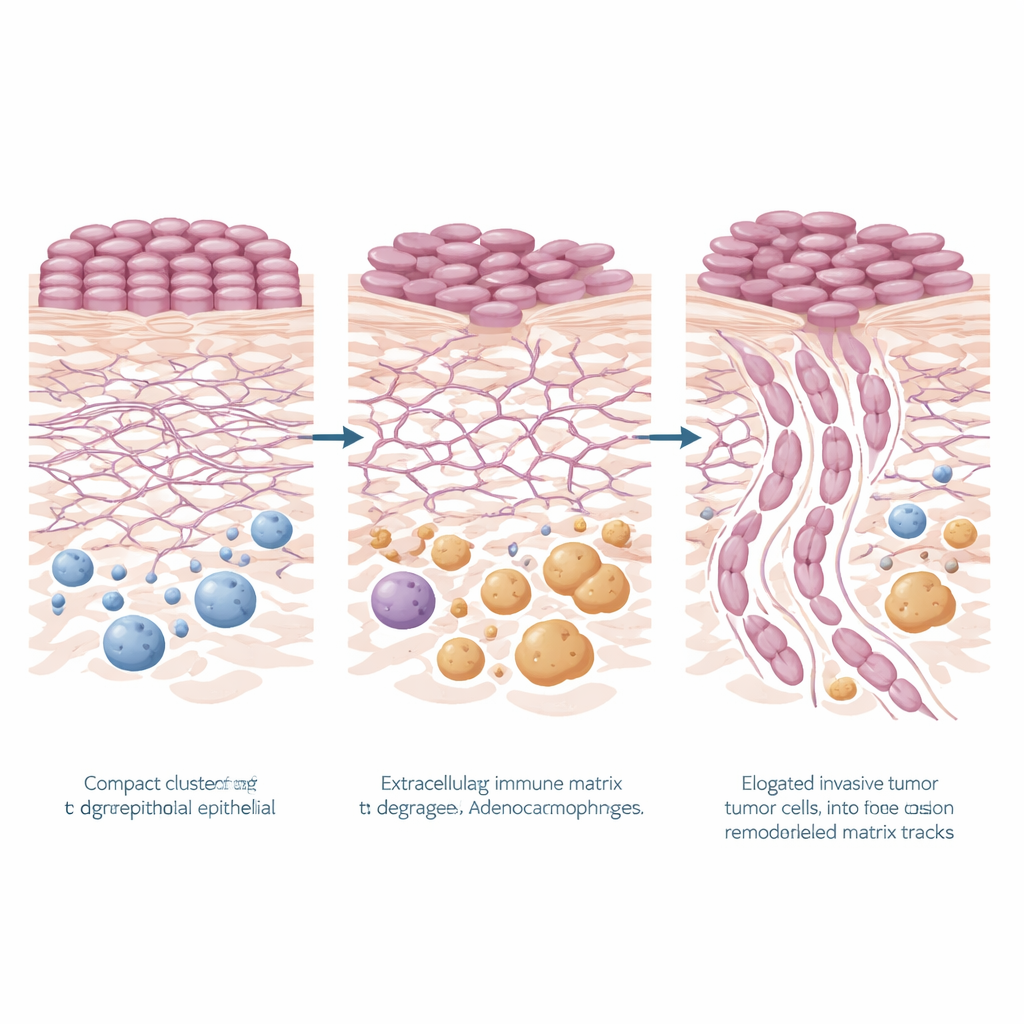
Un motif frappant est apparu : les gènes impliqués dans le remaniement de l’échafaudage structurel de l’organisme, la matrice extracellulaire, étaient fortement augmentés dans les régions à haut risque, tant dans les cellules tumorales que dans les tissus environnants. Des voies liées à la dégradation de la matrice, à l’organisation de la matrice, à l’adhérence cellulaire et aux signaux associés (y compris la voie PI3K–Akt) étaient toutes élevées. Plusieurs gènes clés se distinguaient dans l’épithélium tumoral — KRT6A, TNC, LAMC2 et FN1 — dont beaucoup codent pour des protéines qui aident les cellules à s’attacher, à se déplacer ou à remodeler leur environnement. Dans le stroma voisin, des gènes tels que MMP9 et POSTN, associés à la coupe et à la reconstruction des fibres de matrice et à un comportement tumoral plus agressif, étaient également augmentés. Ensemble, ces changements dessinent le portrait de tumeurs à haut risque qui ouvrent activement de nouveaux passages dans les tissus et construisent un microenvironnement favorable à l’invasion.
Des cellules immunitaires qui aident plutôt que freinent
Le paysage immunitaire environnant changeait aussi dans les patterns plus dangereux. Les signatures géniques dans le SIME indiquaient une activité accrue du bras inné du système immunitaire et une présence plus importante de macrophages, un type de globule blanc. À l’aide de méthodes computationnelles, l’équipe a inféré que les macrophages dits de type M2 — souvent associés à la cicatrisation et au soutien tumoral plutôt qu’à l’attaque — étaient plus abondants dans les régions à haut risque. Cela a été confirmé au niveau protéique : des colorations tissulaires pour le CD68, un marqueur des macrophages, montraient des populations de macrophages plus denses autour des patterns tumoraux les plus invasifs. Les données suggèrent que la matrice remodelée et un stroma riche en macrophages peuvent agir de concert pour créer une niche nourrissante qui aide la tumeur à pénétrer plus profondément.
Un score génique simple qui signale un risque
Pour explorer l’impact clinique, les auteurs ont construit une signature à quatre gènes à partir de ceux fortement surexprimés dans l’épithélium tumoral à haut risque et davantage exprimés dans la tumeur que dans le col normal : KRT6A, TNC, LAMC2 et FN1. Ils ont combiné l’expression de ces gènes en un seul score et l’ont testé sur un jeu indépendant d’adénocarcinomes cervicaux provenant du Cancer Genome Atlas. Même dans ce petit groupe, les tumeurs ayant des scores plus élevés avaient tendance à présenter une survie globale plus mauvaise, et une valeur seuil permettait de séparer les patientes en groupes à risque plus faible ou plus élevé mieux que le seul stade. Bien que les effectifs soient modestes et nécessitent une validation sur des cohortes plus larges, ce type d’outil moléculaire s’apparente aux tests déjà utilisés en oncologie du sein pour guider les décisions thérapeutiques.
Ce que cela signifie pour l’avenir
En termes accessibles, cette étude montre que les adénocarcinomes endocervicaux associés au VPH les plus dangereux ne sont pas de simples versions « plus grandes » de tumeurs plus sûres ; ils sont biologiquement différents. Les régions à haut risque se caractérisent par des cellules tumorales et des tissus voisins qui remodèlent conjointement l’échafaudage tissulaire et recrutent des cellules immunitaires auxiliaires, en particulier certains macrophages, pour soutenir l’invasion. La signature à quatre gènes extraite de ces changements laisse entrevoir un avenir où des tests moléculaires simples pourraient repérer les patientes dont les tumeurs ont un comportement agressif, même lorsque le stade clinique paraît précoce. Les résultats orientent aussi vers de nouvelles pistes thérapeutiques : des médicaments ciblant le remaniement de la matrice extracellulaire ou modulant la réponse immunitaire innée pourraient être prometteurs pour les femmes présentant des patterns d’invasion à haut risque dans ce type de cancer du col.
Citation: Axelrod, M.L., Zhou, R. & Sun, L. Spatial transcriptomic landscape of invasion patterns in human papillomavirus-associated endocervical adenocarcinoma. Sci Rep 16, 13246 (2026). https://doi.org/10.1038/s41598-026-43717-z
Mots-clés: adénocarcinome cervical, cancer lié au VPH, microenvironnement tumoral, remaniement de la matrice extracellulaire, signature génique pronostique