Clear Sky Science · de
Räumlich-transkriptomische Landschaft der Invasionsmuster beim humanen Papillomavirus-assoziierten Endozervix-Adenokarzinom
Warum das für die Gesundheit von Frauen wichtig ist
Zervixkarzinom wird oft als eine einzelne Erkrankung betrachtet, doch Gebärmutterhalskrebse verhalten sich nicht alle gleich. Diese Studie untersucht eine mit dem humanen Papillomavirus (HPV) verknüpfte Form, das endozervikale Adenokarzinom, und stellt eine einfache, aber entscheidende Frage: Warum bleiben manche Tumoren relativ lokal begrenzt, während andere tief invasiv werden und gefährlicher sind? Indem die Autoren aufzeichnen, welche Gene in verschiedenen Bereichen des Tumors und seines Umfelds aktiv sind, liefern sie Hinweise, die Ärzten eines Tages helfen könnten, das Risiko besser vorherzusagen und gezieltere Therapien zu entwickeln.
Verschiedene Arten, wie Krebs sich ausbreiten kann
Ärztinnen und Ärzte wissen bereits, dass HPV-assoziierte endozervikale Adenokarzinome in Invasionsmuster gruppiert werden können, die als Silva-Muster A, B und C bezeichnet sind. Muster A wachsen tendenziell in gerundeten Drüsen und bleiben organisierter, während Muster C invasiv in einer destruktiven, diffusen Weise wachsen und deutlich häufiger in Lymphknoten metastasieren und das Überleben verschlechtern. Ein vereinfachtes Zwei-Stufen-System klassifiziert Muster A und einige B-Tumoren als niedriges Risiko und Muster C sowie B-Tumoren mit Gefäßinvasion als hohes Risiko. Was bislang fehlte, ist ein Verständnis dafür, was auf molekularer Ebene in diesen unterschiedlichen Mustern vor sich geht, insbesondere in der unmittelbaren Nachbarschaft des Tumors – dem umgebenden Stützgewebe und den Immunzellen, die das Tumorwachstum einschränken oder fördern können.
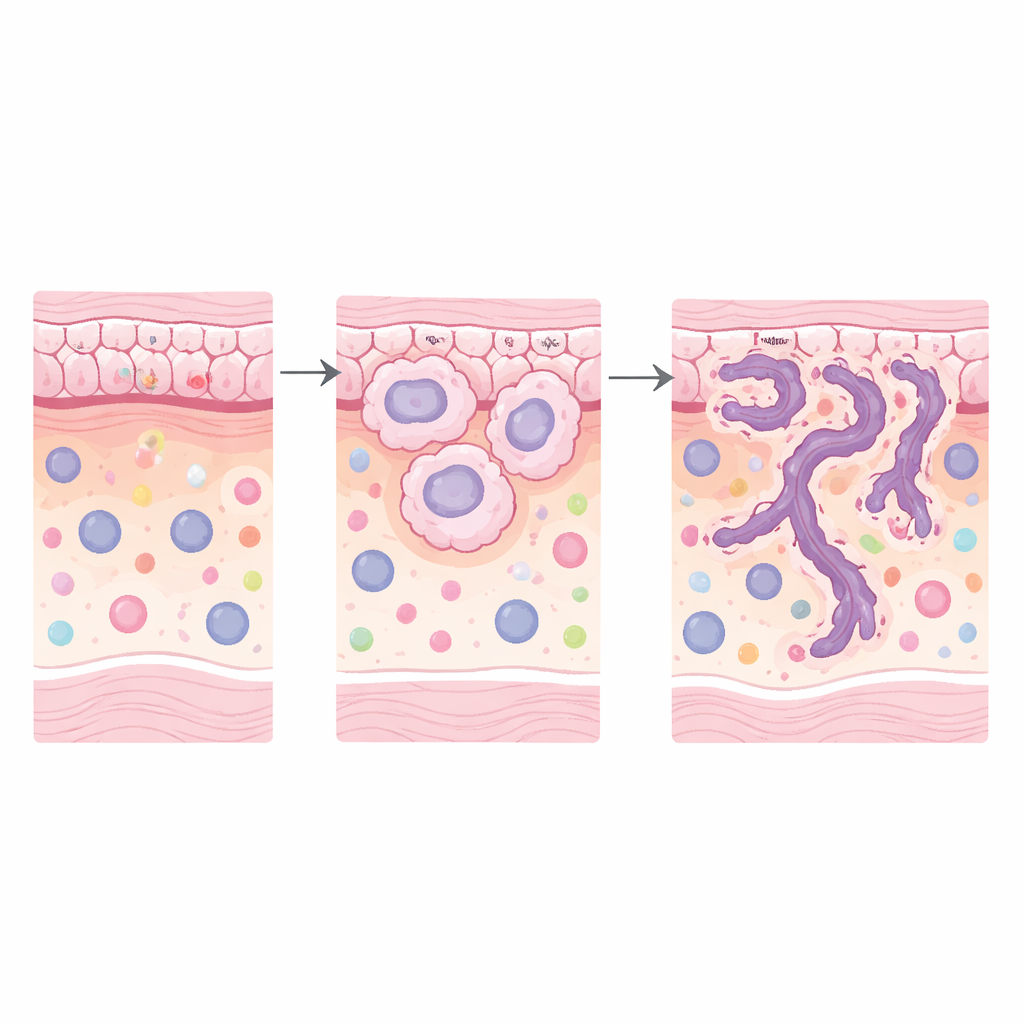
Genaktivität im räumlichen Kontext lesen
Um dies zu untersuchen, verwendeten die Forschenden eine Technologie namens räumliche Transkriptomik an sieben chirurgisch entfernten Tumoren, die mehr als ein Invasionsmuster im gleichen Präparat aufwiesen. Dieses clevere Design erlaubte Vergleiche zwischen Niedrig-Risiko- und Hoch-Risiko-Bereichen innerhalb desselben Patienten und reduzierte so personenbezogene Hintergrundunterschiede. Mit der GeoMX-Plattform wählten sie Dutzende kleiner Regionen aus, die sowohl Tumorzellen als auch die umgebende stromale Immunmikroumgebung (SIME) enthielten. Fluoreszente Marker wurden genutzt, um RNA aus dem Tumorepithel von der nahegelegenen Nicht-Tumor-Gewebe-RNA zu trennen. Anschließend sequenzierten sie die RNA, um zu sehen, welche Gene in jedem Kompartiment ein- oder ausgeschaltet waren, und setzten statistische Werkzeuge ein, um konsistente Veränderungen zu identifizieren, die mit Hoch-Risiko-Invasion verbunden sind.
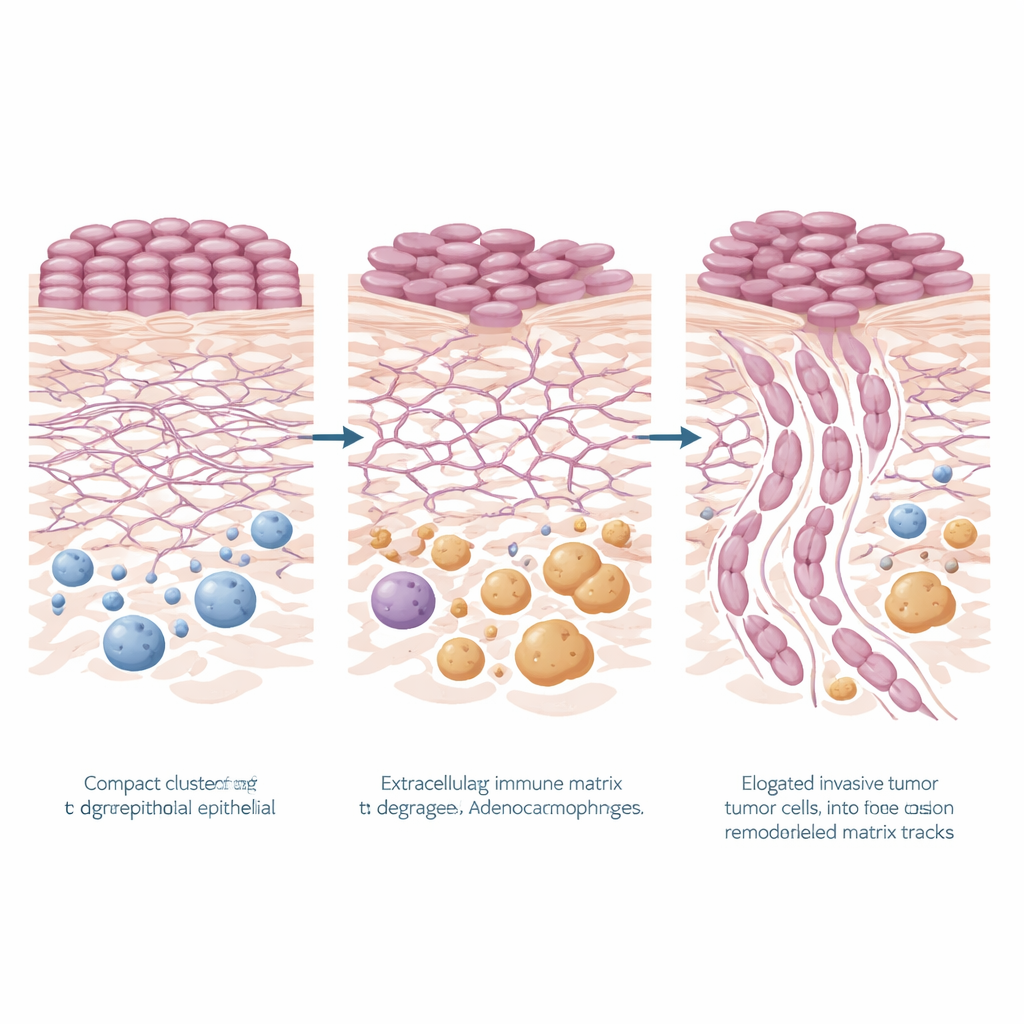
Wie der Tumor sein Gerüst umgestaltet
Ein auffälliges Muster zeigte sich: Gene, die an der Umgestaltung des strukturellen Gerüsts des Körpers beteiligt sind, der sogenannten extrazellulären Matrix, waren in Hoch-Risiko-Regionen stark erhöht – sowohl in den Tumorzellen als auch im umgebenden Gewebe. Signalwege, die mit Matrixabbau, Matrixorganisation, Zelladhäsion und verwandten Signalwegen (einschließlich PI3K–Akt-Signalgebung) verknüpft sind, waren alle angehoben. Mehrere Schlüsselgene hoben sich im Karzinom-Epithel hervor – KRT6A, TNC, LAMC2 und FN1 – viele davon kodieren Proteine, die Zellen beim Anheften, Bewegen oder Umgestalten ihrer Umgebung unterstützen. Im benachbarten Stroma waren Gene wie MMP9 und POSTN erhöht, die mit dem Zerschneiden und Wiederaufbauen von Matrixfasern und mit aggressiverem Tumorverhalten assoziiert sind. Gemeinsam zeichnen diese Veränderungen das Bild von Hoch-Risiko-Tumoren, die aktiv neue Pfade durch das Gewebe schneiden und eine Mikroumgebung schaffen, die Invasion fördert.
Immunzellen, die eher helfen als hindern
Auch die umgebende Immunlandschaft verschob sich in den gefährlicheren Mustern. Gensignaturen in der SIME deuteten auf eine erhöhte Aktivität des angeborenen Immunsystems und eine verstärkte Präsenz von Makrophagen hin, einer Art weiße Blutkörperchen. Mit rechnerischen Methoden schloss das Team darauf, dass sogenannte M2-ähnliche Makrophagen – oft mit Wundheilung und Tumorunterstützung statt Angriff assoziiert – in Hoch-Risiko-Regionen häufiger vorkommen. Dies wurde auf Proteinebene bestätigt: Gewebefärbungen für CD68, ein Makrophagenmarker, zeigten dichtere Makrophagenpopulationen um die invasivsten Tumormuster. Die Daten legen nahe, dass die umgestaltete Matrix und ein makrophagenreiches Stroma zusammenarbeiten könnten, um eine nährende Nische zu schaffen, die dem Krebs das tiefere Eindringen erleichtert.
Ein einfacher Gen-Score, der Gefahr signalisiert
Um den klinischen Einfluss zu prüfen, entwickelten die Autoren eine Vier-Gen-Signatur aus denen, die in Hoch-Risiko-Tumorepithelien stark hochreguliert und in Tumoren stärker exprimiert waren als im normalen Gebärmutterhals: KRT6A, TNC, LAMC2 und FN1. Sie kombinierten die Expression dieser Gene zu einem einzigen Score und testeten ihn an einer unabhängigen Kohorte von Zervixadenokarzinomen aus The Cancer Genome Atlas. Selbst in dieser kleinen Gruppe neigten Tumoren mit höheren Scores zu einem schlechteren Gesamtergebnis, und ein Schwellenwert konnte Patienten besser als das Stadium allein in niedrigere und höhere Risikogruppen einteilen. Obwohl die Zahlen begrenzt sind und eine Validierung in größeren Kohorten benötigen, ähnelt ein solches genbasiertes Instrument Tests, die bereits beim Brustkrebs verwendet werden, um Therapieentscheidungen zu leiten.
Was das für die Zukunft bedeutet
Anschaulich zeigt diese Studie, dass gefährlichere HPV-assoziierte endozervikale Adenokarzinome nicht einfach „größere“ Versionen sichererer Tumoren sind; sie sind biologisch anders. Hoch-Risiko-Regionen sind durch Tumorzellen und Nachbargewebe gekennzeichnet, die gemeinsam das Gewebegerüst umgestalten und unterstützende Immunzellen, insbesondere bestimmte Makrophagen, rekrutieren, um die Invasion zu fördern. Die aus diesen Veränderungen abgeleitete Vier-Gen-Signatur deutet auf eine Zukunft hin, in der einfache molekulare Tests Patientinnen identifizieren könnten, deren Tumoren wahrscheinlich aggressiv verlaufen, selbst wenn das Stadium noch früh erscheint. Die Befunde zeigen zudem neue therapeutische Ansatzpunkte: Wirkstoffe, die die Umgestaltung der extrazellulären Matrix hemmen oder das angeborene Immunsystem umprogrammieren, könnten für Frauen mit Hoch-Risiko-Invasionsmustern bei dieser Form des Zervixkarzinoms vielversprechend sein.
Zitation: Axelrod, M.L., Zhou, R. & Sun, L. Spatial transcriptomic landscape of invasion patterns in human papillomavirus-associated endocervical adenocarcinoma. Sci Rep 16, 13246 (2026). https://doi.org/10.1038/s41598-026-43717-z
Schlüsselwörter: Zervixadenokarzinom, HPV-assoziierter Krebs, Tumormikroumgebung, Umlagerung der extrazellulären Matrix, prognostische Gen-Signatur