Clear Sky Science · zh
从内含子滞留中识别结直肠癌的免疫原性新抗原
将隐藏的遗传错误转化为癌症靶点
结直肠癌是全球最常见的癌症之一,对于许多患者,尤其是那些肿瘤携带极少DNA突变的患者,目前的个性化癌症疫苗可供利用的靶点非常有限。本研究揭示了一个令人惊讶的新疫苗靶点来源,它并不来自经典的基因突变,而是来自肿瘤细胞处理RNA的方式。研究者聚焦于一种称为内含子滞留的过程——即在原始遗传信息中某些片段被错误地保留下来——从而发现了大量非典型的蛋白片段,这些片段可以被免疫系统识别并可能成为攻击目标。
为何癌症疫苗需要新的靶点
目前大多数实验性癌症疫苗基于“新抗原”——仅在肿瘤细胞上出现而不在健康组织中存在的小蛋白片段。传统上,科学家通过扫描患者肿瘤的DNA以寻找点突变及其他小变化,然后预测哪些改变的蛋白片段可能被呈递给免疫细胞。问题在于,许多肿瘤——包括常见的微卫星稳定型结直肠癌——本身并不携带足够的DNA突变来产生大量强免疫原性的新抗原。这种匮乏让为大范围患者设计疫苗变得困难,也限制了这些治疗的有效性。
当细胞的编辑机制出现失误
作者没有只关注DNA变化,而是转向了RNA——细胞用来合成蛋白质的中间信息。正常情况下,细胞会在翻译前移除这些信息中的非编码片段(称为内含子)。然而在许多癌症中,这种编辑过程变得粗糙,内含子被意外保留。研究团队对23例结直肠癌患者的肿瘤与邻近健康组织的RNA测序数据进行了专门的软件管线分析,发现肿瘤样本中持续显示出比健康组织更多的内含子滞留事件,每个肿瘤有数百例此类事件,在患者群体中有数千个更常被保留的内含子。许多受影响的基因参与细胞分裂和DNA处理——这些是癌症中常被扰动的关键过程。
从错误的信息到新的免疫标志
滞留的内含子不仅使RNA变得混乱;它们还能被翻译成免疫系统从未见过的异常蛋白片段。研究者将滞留的内含子序列翻译成短肽,并利用计算工具预测哪些肽段可能与常见的细胞表面呈递分子(HLA蛋白)紧密结合。随后他们交叉比对公共蛋白质数据库,只保留那些在结直肠癌样本中出现但在健康组织中未见的肽段。通过这一筛选,他们选出一组候选肽,并用灵敏的PCR检测确认,许多含内含子的RNA在肿瘤中的表达水平确实高于配对的正常组织。
教导T细胞识别这些新靶点
为检验这些来源于内含子的片段能否真正激活免疫系统,研究团队用体外培养并加载候选肽的免疫细胞训练来自健康供者的人类CD8 T细胞。若干肽触发了强烈反应:经训练的T细胞分泌免疫信号分子、激活标志表达上调,并在遇到呈递匹配肽的细胞时显示出杀伤迹象。额外的质谱证据表明,至少部分这些肽确实在结直肠肿瘤内自然产生。值得注意的是,作者还鉴定出24个内含子来源的新抗原,约出现在30%的患者中,并被预测能很好地结合患者群体中最常见的HLA类型,这提示这些靶点有可能是共享的,而非完全个体化的。
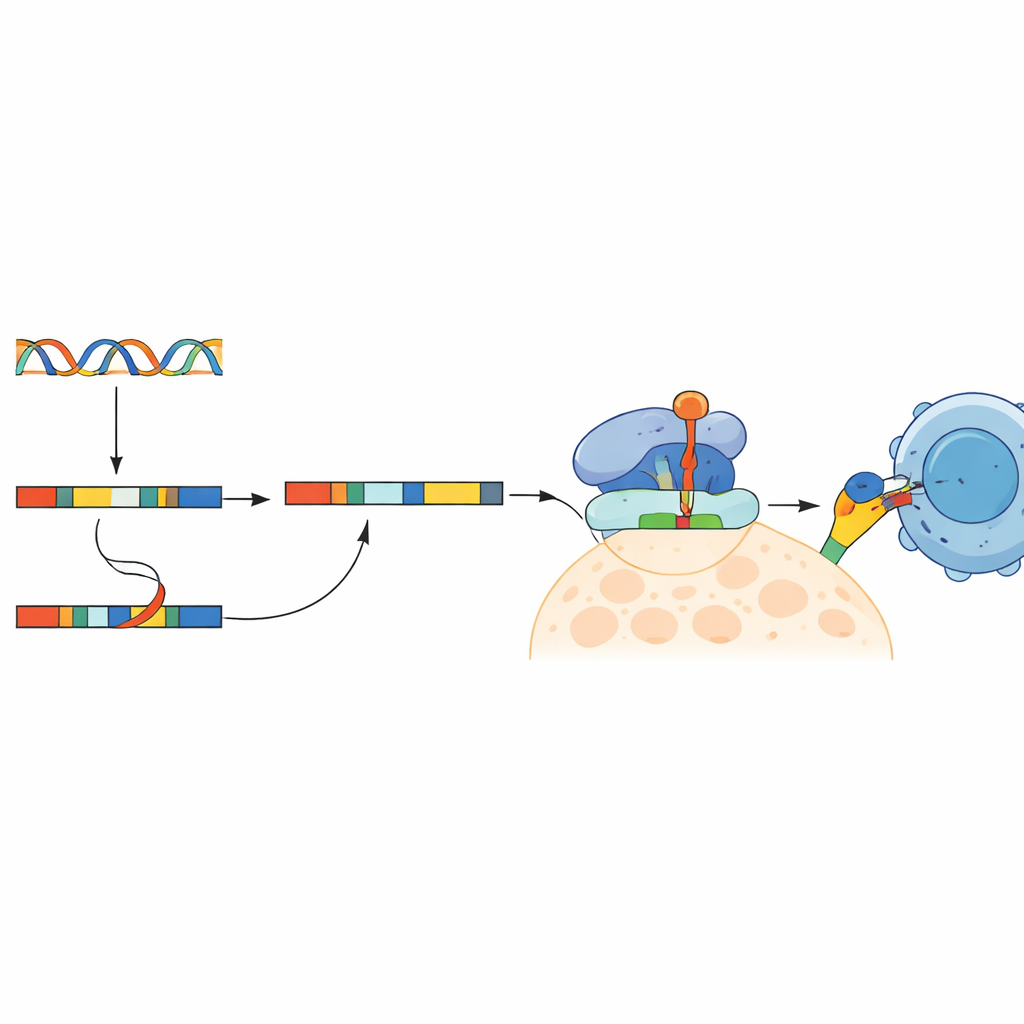
通向更广谱癌症疫苗的新途径
这项工作表明,内含子滞留——这一曾被忽视的RNA加工特性——能够在结直肠癌细胞上产生真实且可被免疫识别的靶点。通过证明这些基于内含子的新抗原存在、在患者间有时是共享的,并且能在体外激活杀伤性T细胞,该研究为新一类癌症疫苗成分打开了大门。对于那些肿瘤缺乏大量经典DNA突变的患者,尤其是微卫星稳定型结直肠癌患者,挖掘这一隐藏层的异常蛋白片段可能大幅扩展未来个性化与现成免疫治疗的选择。
引用: Manoharan, T., Kee, B.B.R., Cheng, C.Z.M. et al. Identification of immunogenic neoantigens from intron retention in colorectal cancer. Sci Rep 16, 12796 (2026). https://doi.org/10.1038/s41598-026-43687-2
关键词: 结直肠癌, 癌症疫苗, 新抗原, 内含子滞留, 免疫疗法