Clear Sky Science · de
Identifizierung immunogener Neoantigene aus Intron-Retention bei kolorektalem Krebs
Verborgene genetische Fehler als Krebsziele nutzen
Kolorektales Karzinom gehört zu den weltweit häufigsten Krebsarten, und für viele Patientinnen und Patienten — insbesondere solche mit Tumoren, die nur wenige DNA-Mutationen tragen — bieten die heutigen personalisierten Krebsimpfstoffe nur wenig Ansatzpunkte. Diese Studie zeigt eine überraschende neue Quelle für Impfstoffziele, die sich nicht in klassischen Genmutationen, sondern in der Art und Weise verbirgt, wie Tumorzellen ihre RNA verarbeiten. Indem die Forschenden einen Prozess namens Intron-Retention in den Blick nehmen — bei dem Stücke der ursprünglichen genetischen Botschaft versehentlich erhalten bleiben — entdecken sie einen reichen Vorrat ungewöhnlicher Proteinfragmente, die das Immunsystem erkennen und potenziell angreifen kann.
Warum Krebsimpfstoffe neue Ziele brauchen
Die meisten experimentellen Krebsimpfstoffe basieren heute auf „Neoantigenen“ — kurzen Proteinfragmenten, die nur auf Tumorzellen, nicht aber auf gesundem Gewebe vorkommen. Üblicherweise suchen Forschende diese Ziele, indem sie die Tumor-DNA eines Patienten nach Punktmutationen und anderen kleinen Veränderungen scannen und dann vorhersagen, welche veränderten Proteinabschnitte dem Immunsystem präsentiert werden könnten. Das Problem ist, dass viele Tumoren, darunter die häufige mikrosatellitenstabile Form des kolorektalen Karzinoms, einfach nicht genügend DNA-Mutationen aufweisen, um viele starke Neoantigene zu erzeugen. Diese Knappheit erschwert die Entwicklung von Impfstoffen für große Patientengruppen und begrenzt die Wirksamkeit dieser Therapien.
Wenn die zelluläre Bearbeitungsmaschine nachlässt
Statt sich nur auf DNA-Veränderungen zu beschränken, richteten die Autorinnen und Autoren ihren Blick auf die RNA, die Zwischenbotschaft, die Zellen zur Proteinproduktion lesen. Normalerweise entfernen Zellen nicht-codierende Abschnitte, sogenannte Introns, aus diesen Botschaften, bevor sie übersetzt werden. In vielen Krebsarten wird dieser Bearbeitungsprozess jedoch unsauber, und Introns bleiben versehentlich erhalten. Das Team analysierte RNA-Sequenzierungsdaten aus Tumoren und angrenzendem gesundem Gewebe von 23 Patientinnen und Patienten mit kolorektalem Krebs mithilfe einer spezialisierten Analyse-Pipeline. Sie fanden, dass Tumorproben konsistent mehr Ereignisse von Intron-Retention zeigten als gesundes Gewebe, mit Hunderten solcher Ereignisse pro Tumor und Tausenden von Introns, die in der Patientengruppe gehäuft erhalten blieben. Viele der betroffenen Gene sind an Zellteilung und DNA-Handhabung beteiligt — Schlüsselfunktionen, die in Krebs oft gestört sind.
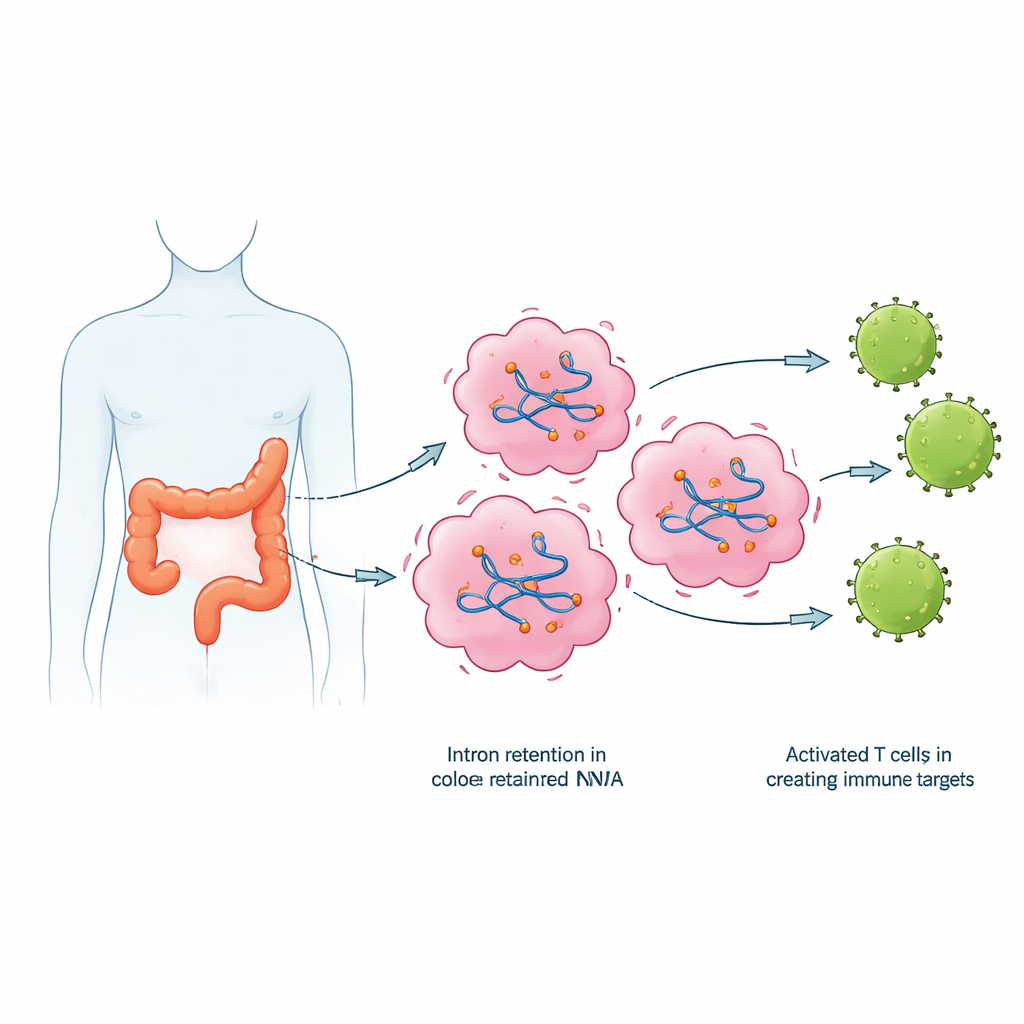
Von fehlerhaften Botschaften zu neuen Immunmarkern
Retinierte Introns sorgen nicht nur für RNA-Müll; sie können in abnorme Proteinfragmente umgesetzt werden, die das Immunsystem noch nie gesehen hat. Die Forschenden übersetzten die Sequenzen der retained Introns in kurze Peptide und nutzten Computerwerkzeuge, um vorherzusagen, welche davon stark an verbreitete Präsentationsmoleküle des Immunsystems (HLA-Proteine) an der Zelloberfläche binden könnten. Anschließend verglichen sie öffentlich verfügbare Proteindaten, um nur Peptide zu behalten, die in Proben von kolorektalen Karzinomen, nicht aber in gesundem Gewebe nachgewiesen wurden. Aus diesem Screening wählten sie eine Reihe von Kandidatenpeptiden aus und bestätigten mittels sensitiver PCR-Tests, dass viele der zugrundeliegenden intronhaltigen RNAs in Tumoren tatsächlich in höheren Mengen vorkamen als im jeweils passenden Normalgewebe.
Den T‑Zellen beibringen, die neuen Ziele zu erkennen
Um zu prüfen, ob diese Intronderivate das Immunsystem wirklich wecken können, trainierte das Team CD8-T-Zellen von gesunden Spendern mithilfe im Labor kultivierter Immunzellen, die mit den Kandidatenpeptiden geladen waren. Mehrere Peptide lösten starke Reaktionen aus: die trainierten T‑Zellen schütteten Immunbotschaften aus, schalteten Aktivierungsmarker ein und zeigten Anzeichen von zytotoxischer Aktivität, wenn sie auf Zellen trafen, die das passende Peptid präsentierten. Zusätzliche Massenspektrometrie-Belege deuteten darauf hin, dass zumindest einige dieser Peptide natürlich in kolorektalen Tumoren produziert werden. Auffällig war auch, dass die Autorinnen und Autoren 24 intronbasierte Neoantigene identifizierten, die bei etwa 30 % der Patientinnen und Patienten vorkamen und wahrscheinlich gut an die in der Gruppe häufigsten HLA-Typen binden — ein Hinweis auf geteilte statt rein individuelle Impfstoffziele.
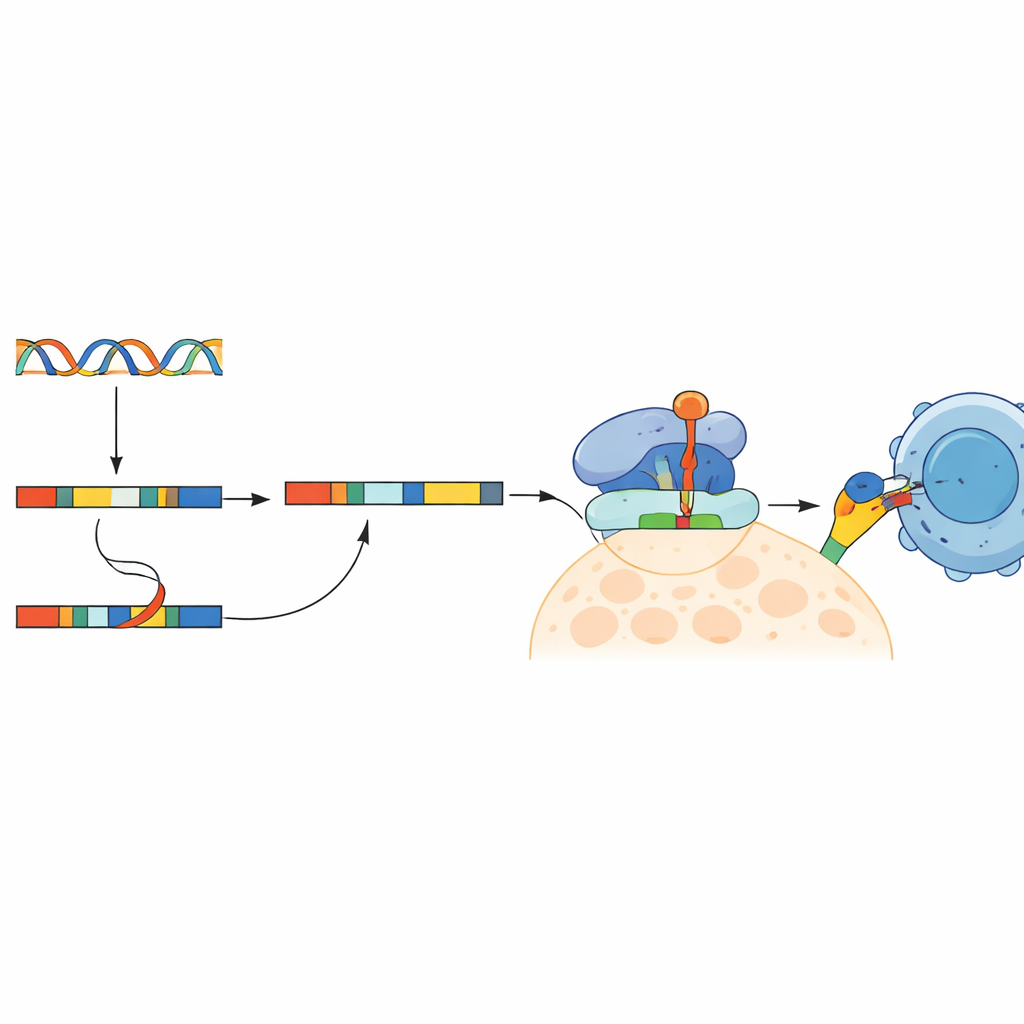
Neue Wege zu breiteren Krebsimpfstoffen
Diese Arbeit zeigt, dass Intron-Retention — eine lange übersehene Eigenart der RNA‑Verarbeitung — echte, immunologisch sichtbare Ziele auf kolorektalen Krebszellen erzeugen kann. Indem die Studie nachweist, dass diese intronbasierten Neoantigene vorhanden sind, bisweilen zwischen Patientinnen und Patienten geteilt werden und T‑Zellen im Labor aktivieren können, ebnet sie den Weg für eine neue Klasse von Inhaltsstoffen für Krebsimpfstoffe. Für Patientinnen und Patienten, deren Tumoren nur wenige klassische DNA‑Mutationen aufweisen, insbesondere bei mikrosatellitenstabilem kolorektalem Krebs, könnte das Anzapfen dieser verborgenen Schicht abnormaler Proteinfragmente die künftigen Optionen für personalisierte und vorgefertigte Immuntherapien deutlich erweitern.
Zitation: Manoharan, T., Kee, B.B.R., Cheng, C.Z.M. et al. Identification of immunogenic neoantigens from intron retention in colorectal cancer. Sci Rep 16, 12796 (2026). https://doi.org/10.1038/s41598-026-43687-2
Schlüsselwörter: kolorektales Karzinom, Krebsimpfstoffe, Neoantigene, Intron-Retention, Immuntherapie