Clear Sky Science · pl
Identyfikacja immunogennych neoantygenów wynikających z zatrzymania intronów w raku jelita grubego
Przekształcanie ukrytych błędów genetycznych w cele przeciwnowotworowe
Rak jelita grubego jest jednym z najczęstszych nowotworów na świecie, a dla wielu pacjentów, zwłaszcza tych z guzami zawierającymi niewiele zmian w DNA, współczesne spersonalizowane szczepionki przeciwnowotworowe mają niewiele punktów zaczepienia. To badanie ujawnia zaskakujące nowe źródło celów szczepionkowych, ukryte nie w klasycznych mutacjach genów, lecz w sposobie przetwarzania RNA przez komórki nowotworowe. Skupiając się na procesie zwanym zatrzymaniem intronów — gdy fragmenty surowych komunikatów genetycznych są omyłkowo pozostawione — badacze odkrywają obfite źródło nietypowych fragmentów białkowych, które układ odpornościowy może rozpoznać i potencjalnie zaatakować.
Dlaczego szczepionki przeciwnowotworowe potrzebują nowych celów
Większość eksperymentalnych szczepionek przeciwnowotworowych opiera się dziś na „neoantygenach” — małych fragmentach białek występujących wyłącznie na komórkach nowotworowych, a nie w tkankach zdrowych. Tradycyjnie poszukuje się tych celów, skanując DNA guza pacjenta w poszukiwaniu punktowych mutacji i innych drobnych zmian, a następnie przewidując, które zmienione fragmenty białek mogą zostać zaprezentowane komórkom odpornościowym. Problem w tym, że wiele guzów, w tym powszechna forma raka jelita grubego o stabilnych mikrosatelitach, po prostu nie ma wystarczająco dużo mutacji DNA, aby wygenerować liczne silne neoantygeny. Ta niedobór utrudnia projektowanie szczepionek dla szerokich grup pacjentów i ogranicza skuteczność tych terapii.
Kiedy mechanizm edycyjny komórki zawodzi
Zamiast skupiać się wyłącznie na zmianach w DNA, autorzy zwrócili uwagę na RNA — pośrednie komunikaty, które komórki odczytują, by wytwarzać białka. Normalnie komórki usuwają niekodujące fragmenty zwane intronami z tych komunikatów przed translacją. W wielu nowotworach jednak ten proces edycji staje się niedokładny i introny bywają przypadkowo pozostawiane. Zespół przeanalizował dane z sekwencjonowania RNA pochodzące z guzów i przyległej zdrowej tkanki od 23 pacjentów z rakiem jelita grubego, używając wyspecjalizowanego pipeline’u bioinformatycznego. Stwierdzili, że próbki guzów konsekwentnie wykazywały więcej zdarzeń zatrzymania intronów niż tkanka zdrowa — setki takich zdarzeń na guz i tysiące intronów częściej zatrzymywanych w grupie pacjentów. Wiele dotkniętych genów brało udział w podziale komórek i obsłudze DNA — kluczowych procesach często zakłóconych w nowotworach.
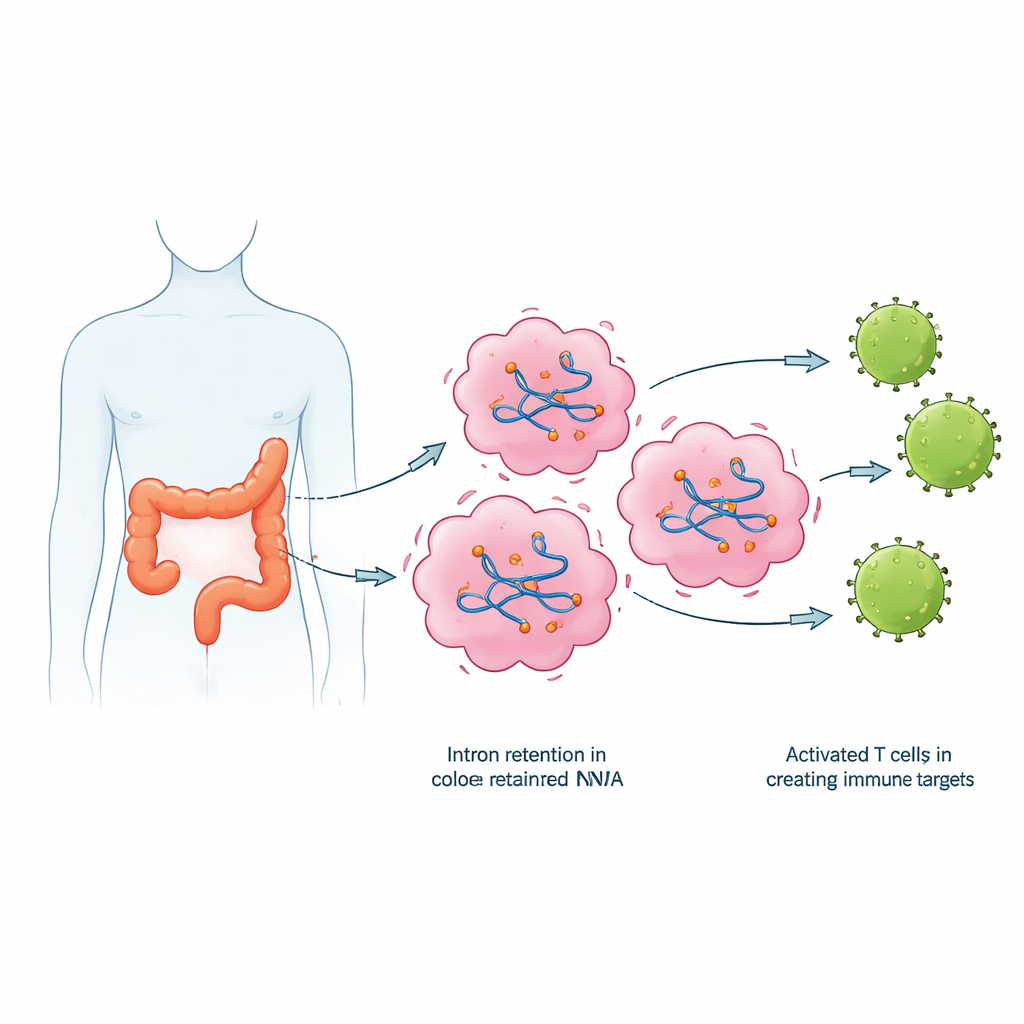
Z wadliwych komunikatów do nowych znaczników immunologicznych
Zatrzymane introny robią więcej niż tylko zaśmiecają RNA; mogą być przekształcone w nietypowe fragmenty białkowe, których układ odpornościowy nigdy wcześniej nie widział. Badacze przetłumaczyli sekwencje zatrzymanych intronów na krótkie peptydy i użyli narzędzi komputerowych, by przewidzieć, które z nich mogą silnie wiązać się z powszechnymi cząsteczkami prezentującymi antygen (białkami HLA) na powierzchni komórek. Następnie sprawdzili publiczne zbiory danych białkowych, by zachować tylko peptydy występujące w próbkach raka jelita grubego, ale nie w tkankach zdrowych. Z tej selekcji wybrali zestaw kandydackich peptydów i potwierdzili za pomocą czułych testów PCR, że wiele odpowiednich RNA zawierających introny rzeczywiście występowało w wyższych poziomach w guzach niż w dopasowanej tkance normalnej.
Nauczanie limfocytów T rozpoznawania nowych celów
Aby sprawdzić, czy te fragmenty pochodzące z intronów mogą rzeczywiście pobudzać układ odpornościowy, zespół zaszczepił ludzkie limfocyty CD8 od zdrowych dawców, używając w laboratorium komórek odpornościowych załadowanych kandydackimi peptydami. Kilka peptydów wywołało silne reakcje: wyszkolone limfocyty T wydzielały sygnały immunologiczne, włączały markery aktywacji i wykazywały oznaki zdolności zabijania, gdy napotkały komórki prezentujące dopasowany peptyd. Dodatkowe dowody z masowej spektrometrii sugerują, że przynajmniej niektóre z tych peptydów są naturalnie wytwarzane w obrębie guzów jelita grubego. Co ważne, autorzy zidentyfikowali również 24 neoantygeny pochodzące z intronów, które pojawiały się u około 30% pacjentów i były przewidywane jako dobrze wiążące się z najczęstszymi typami HLA w tej grupie, co sugeruje możliwość występowania udostępnionych, a nie wyłącznie indywidualnych, celów szczepionkowych.
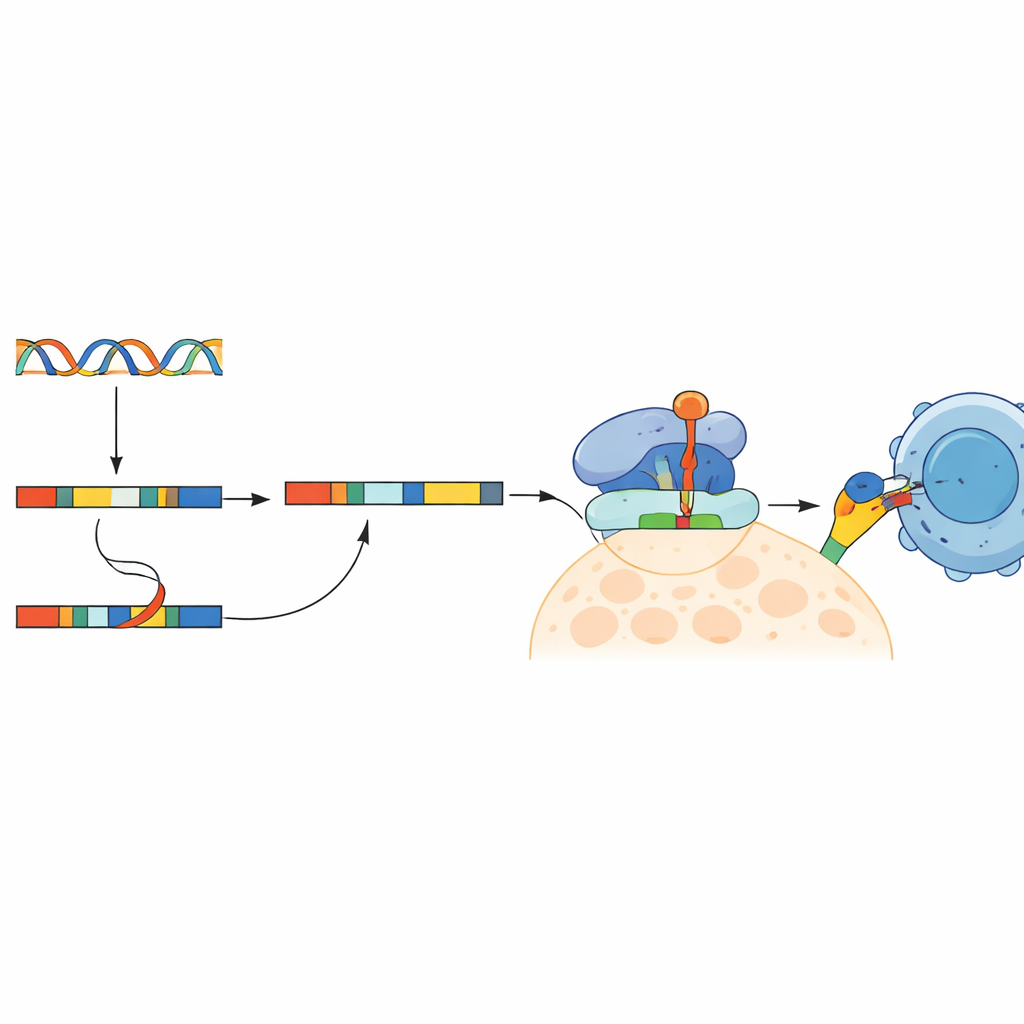
Nowe ścieżki ku szerszym szczepionkom przeciwnowotworowym
Ta praca pokazuje, że zatrzymanie intronów — niegdyś pomijana osobliwość przetwarzania RNA — może generować prawdziwe, widoczne dla układu odpornościowego cele na komórkach raka jelita grubego. Udowadniając, że te oparte na intronach neoantygeny istnieją, czasami są współdzielone między pacjentami i potrafią aktywować cytotoksyczne limfocyty T in vitro, badanie otwiera drogę do nowej klasy składników szczepionek przeciwnowotworowych. Dla pacjentów, których guzy mają niewiele klasycznych mutacji DNA, szczególnie z rakiem jelita grubego o stabilnych mikrosatelitach, wykorzystanie tej ukrytej warstwy nieprawidłowych fragmentów białkowych może znacznie poszerzyć przyszłe opcje zarówno dla terapii spersonalizowanych, jak i gotowych „z półki” immunoterapii.
Cytowanie: Manoharan, T., Kee, B.B.R., Cheng, C.Z.M. et al. Identification of immunogenic neoantigens from intron retention in colorectal cancer. Sci Rep 16, 12796 (2026). https://doi.org/10.1038/s41598-026-43687-2
Słowa kluczowe: rak jelita grubego, szczepionki przeciwnowotworowe, neoantygeny, zatrzymanie intronów, immunoterapia