Clear Sky Science · nl
Identificatie van immunogene neoantigenen door intronretentie bij colorectale kanker
Verborgen genetische fouten omzetten in kankertargets
Colorectale kanker is een van de meest voorkomende vormen van kanker wereldwijd, en voor veel patiënten — vooral zij met tumoren die weinig DNA-mutaties dragen — bieden de huidige gepersonaliseerde kankervaccins weinig aanknopingspunten. Deze studie onthult een verrassende nieuwe bron van vaccinantigenen die niet ligt in klassieke genmutaties, maar in de manier waarop tumorcellen hun RNA verwerken. Door te focussen op een proces dat intronretentie heet — waarbij stukken van de ruwe genetische boodschappen per ongeluk achterblijven — ontdekken onderzoekers een rijke voorraad ongewone eiwitfragmenten die het immuunsysteem kan herkennen en mogelijk aanvallen.
Waarom kankervaccins nieuwe targets nodig hebben
De meeste experimentele kankervaccins van vandaag zijn opgebouwd uit “neoantigenen” — kleine eiwitfragmenten die alleen op tumorcellen voorkomen en niet op gezonde weefsels. Traditioneel zoeken wetenschappers naar deze targets door het DNA van een patiëntstumor te scannen op puntmutaties en andere kleine veranderingen, en vervolgens te voorspellen welke veranderde eiwitstukjes aan immuuncellen getoond zouden kunnen worden. Het probleem is dat veel tumoren, inclusief de veelvoorkomende microsatelliet-stabiele vorm van colorectale kanker, simpelweg niet genoeg DNA-mutaties hebben om veel sterke neoantigenen te genereren. Die schaarste bemoeilijkt het ontwerpen van vaccins voor grote groepen patiënten en beperkt de effectiviteit van deze behandelingen.
Wanneer het bewerkingsmachinerie van de cel uitglijdt
In plaats van alleen naar DNA-veranderingen te kijken, richtten de auteurs zich op RNA, de tussentijdse boodschappen die cellen lezen om eiwitten te maken. Normaal verwijderen cellen niet-coderende segmenten, introns genaamd, uit deze boodschappen voordat ze worden vertaald. In veel kankers raakt dit bewerkingsproces echter slordig en blijven introns per ongeluk achter. Het team analyseerde RNA-sequencinggegevens van tumoren en nabijgelegen gezond weefsel van 23 patiënten met colorectale kanker met behulp van een gespecialiseerde softwarepijplijn. Ze vonden dat tumorsamples consequent meer intronretentiegebeurtenissen toonden dan gezond weefsel, met honderden van zulke gebeurtenissen per tumor en duizenden introns die vaker behouden waren in de patiëntenreeks. Veel van de aangetaste genen waren betrokken bij celdeling en DNA-hantering — sleutelprocessen die vaak verstoord zijn bij kanker.
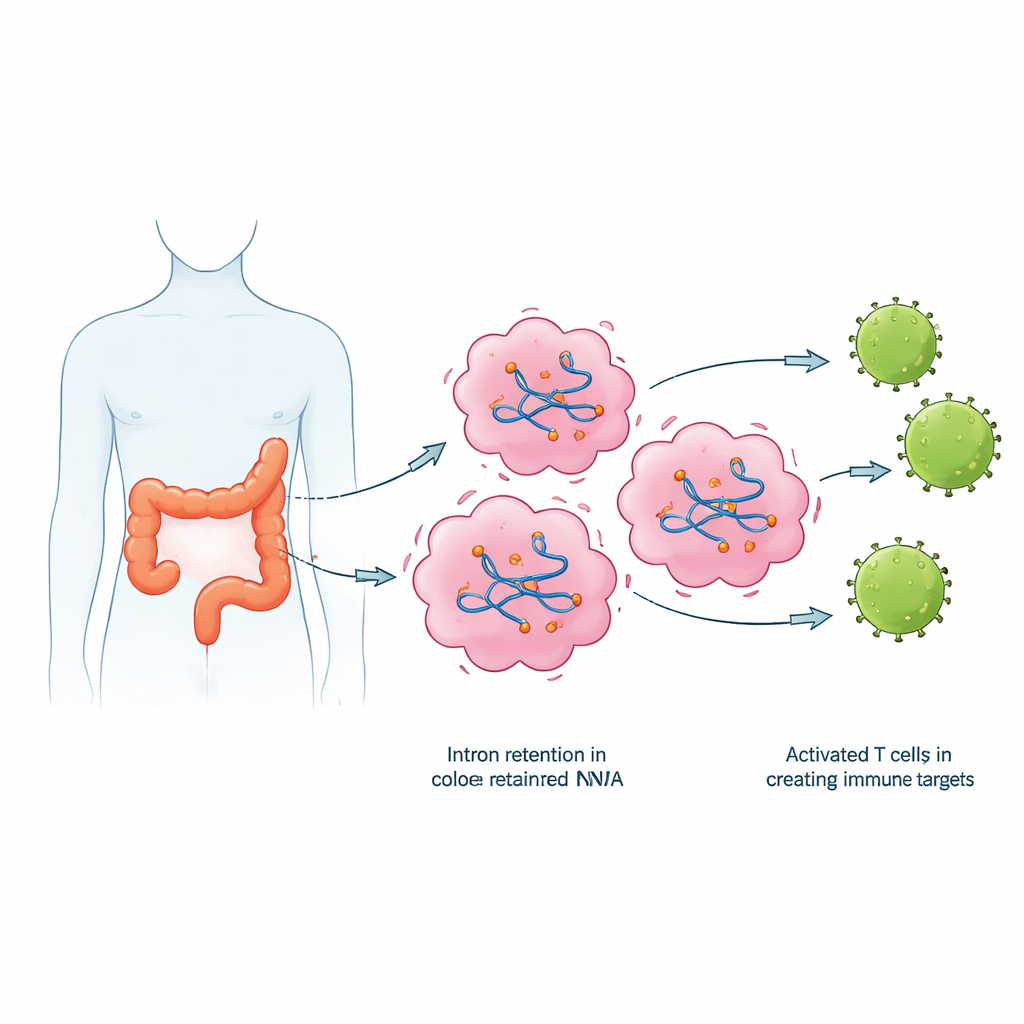
Van foutieve boodschappen naar nieuwe immuunvlaggen
Behouden introns doen meer dan alleen RNA verstoppen; ze kunnen worden omgezet in abnormale eiwitfragmenten die het immuunsysteem nog nooit heeft gezien. De onderzoekers vertaalden sequenties van behouden introns naar korte peptiden en gebruikten computertools om te voorspellen welke daarvan sterk zouden kunnen binden aan gangbare immuun-presentatiemoleculen (HLA-eiwitten) op celoppervlakken. Vervolgens controleerden ze openbare eiwitdatasets om alleen peptiden over te houden die in colorectale kankemonsters voorkwamen maar niet in gezond weefsel. Uit dit scherm selecteerden ze een reeks kandidaatpeptiden en bevestigden met gevoelige PCR-tests dat veel van de onderliggende intron-bevattende RNA's daadwerkelijk op hogere niveaus in tumoren aanwezig waren dan in het overeenkomstige normale weefsel.
T-cellen leren de nieuwe targets herkennen
Om te onderzoeken of deze intron-afgeleide fragmenten het immuunsysteem echt kunnen activeren, trainden de onderzoekers menselijke CD8-T-cellen van gezonde donoren met in het lab gekweekte immuuncellen geladen met de kandidaatpeptiden. Verschillende peptiden wekten sterke reacties op: getrainde T-cellen scheidden immuunsignalen af, zetten activatiemarkers aan en toonden aanwijzingen voor doding wanneer ze cellen tegenkwamen die het bijpassende peptide presenteerden. Aanvullend bewijs uit massaspectrometrie suggereerde dat ten minste sommige van deze peptiden natuurlijk in colorectale tumoren worden geproduceerd. Opvallend was ook dat de auteurs 24 intron-afgeleide neoantigenen identificeerden die bij ongeveer 30% van de patiënten voorkwamen en werden voorspeld goed te binden aan de meest gangbare HLA-typen in de groep, wat wijst op de mogelijkheid van gedeelde, in plaats van uitsluitend unieke, vaccintargets.
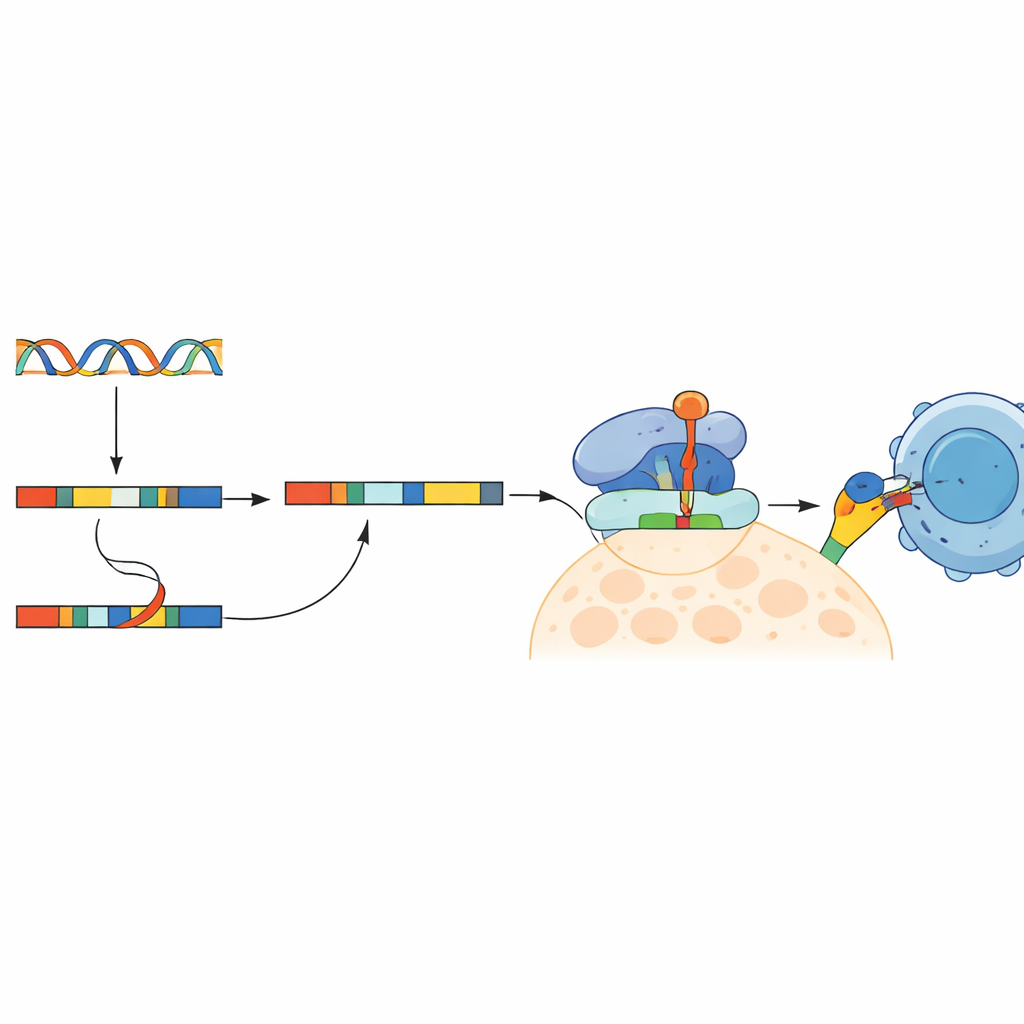
Nieuwe wegen naar bredere kankervaccins
Dit werk toont aan dat intronretentie — een ooit over het hoofd gezien eigenaardigheid van RNA-verwerking — echte, immuunzichtbare targets kan genereren op cellen van colorectale kanker. Door aan te tonen dat deze intron-gebaseerde neoantigenen aanwezig zijn, soms tussen patiënten gedeeld worden en in staat zijn om in het laboratorium cytotoxische T-cellen te activeren, opent de studie de deur naar een nieuwe klasse van ingrediënten voor kankervaccins. Voor patiënten wiens tumoren weinig klassieke DNA-mutaties hebben, met name die met microsatelliet-stabiele colorectale kanker, kan het aanboren van deze verborgen laag van abnormale eiwitfragmenten toekomstige opties voor zowel gepersonaliseerde als kant-en-klare immunotherapieën aanzienlijk vergroten.
Bronvermelding: Manoharan, T., Kee, B.B.R., Cheng, C.Z.M. et al. Identification of immunogenic neoantigens from intron retention in colorectal cancer. Sci Rep 16, 12796 (2026). https://doi.org/10.1038/s41598-026-43687-2
Trefwoorden: colorectale kanker, kankervaccins, neoantigenen, intronretentie, immunotherapie