Clear Sky Science · fr
Identification d’immuno-néoantigènes issus de la rétention d’introns dans le cancer colorectal
Transformer des défauts génétiques cachés en cibles contre le cancer
Le cancer colorectal est l’un des cancers les plus fréquents dans le monde et, pour de nombreux patients, en particulier ceux dont les tumeurs portent peu de mutations de l’ADN, les vaccins personnalisés actuels ont peu de cibles exploitables. Cette étude met en lumière une source surprenante de cibles vaccinales qui ne provient pas des mutations classiques des gènes, mais de la manière dont les cellules tumorales traitent leur ARN. En se concentrant sur un phénomène appelé rétention d’introns — lorsque des segments des messages génétiques bruts sont laissés par erreur — les chercheurs découvrent une riche réserve de fragments protéiques inhabituels que le système immunitaire peut reconnaître et potentiellement attaquer.
Pourquoi les vaccins contre le cancer ont besoin de nouvelles cibles
La plupart des vaccins contre le cancer en expérimentation aujourd’hui sont construits à partir de « néoantigènes » — de petits fragments protéiques qui n’apparaissent que sur les cellules tumorales et pas sur les tissus sains. Traditionnellement, les scientifiques recherchent ces cibles en analysant l’ADN tumoral du patient pour déceler des mutations ponctuelles et d’autres petites altérations, puis en prédisant quels peptides altérés pourraient être présentés aux cellules immunitaires. Le problème est que de nombreuses tumeurs, y compris la forme microsatellite-stable courante du cancer colorectal, ne portent tout simplement pas suffisamment de mutations de l’ADN pour générer beaucoup de néoantigènes robustes. Cette rareté complique la conception de vaccins pour de larges groupes de patients et limite l’efficacité de ces traitements.
Quand la machinerie d’édition cellulaire déraille
Plutôt que de se limiter aux altérations de l’ADN, les auteurs se sont tournés vers l’ARN, ces messages intermédiaires que la cellule lit pour fabriquer des protéines. Normalement, la cellule élimine des segments non codants appelés introns de ces messages avant la traduction. Dans de nombreux cancers, toutefois, ce processus d’édition devient imprécis et des introns sont laissés par accident. L’équipe a analysé des données de séquençage d’ARN provenant de tumeurs et de tissus sains adjacents chez 23 patients atteints d’un cancer colorectal à l’aide d’un pipeline logiciel spécialisé. Ils ont observé que les échantillons tumoraux présentaient systématiquement davantage d’événements de rétention d’introns que les tissus sains, avec des centaines d’événements par tumeur et des milliers d’introns plus fréquemment retenus au sein du groupe de patients. De nombreux gènes affectés participent à la division cellulaire et à la gestion de l’ADN — des processus clés souvent perturbés dans le cancer.
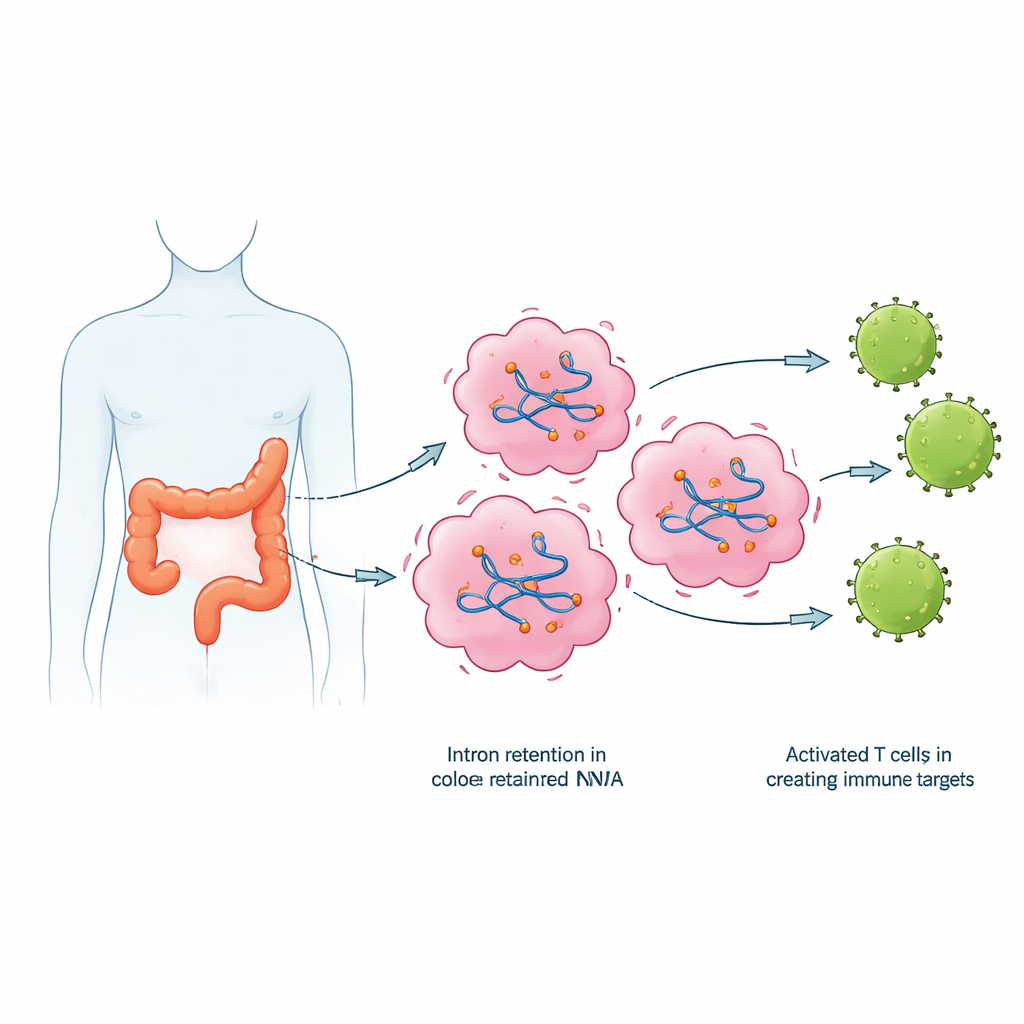
Des messages défectueux à de nouveaux signaux immunitaires
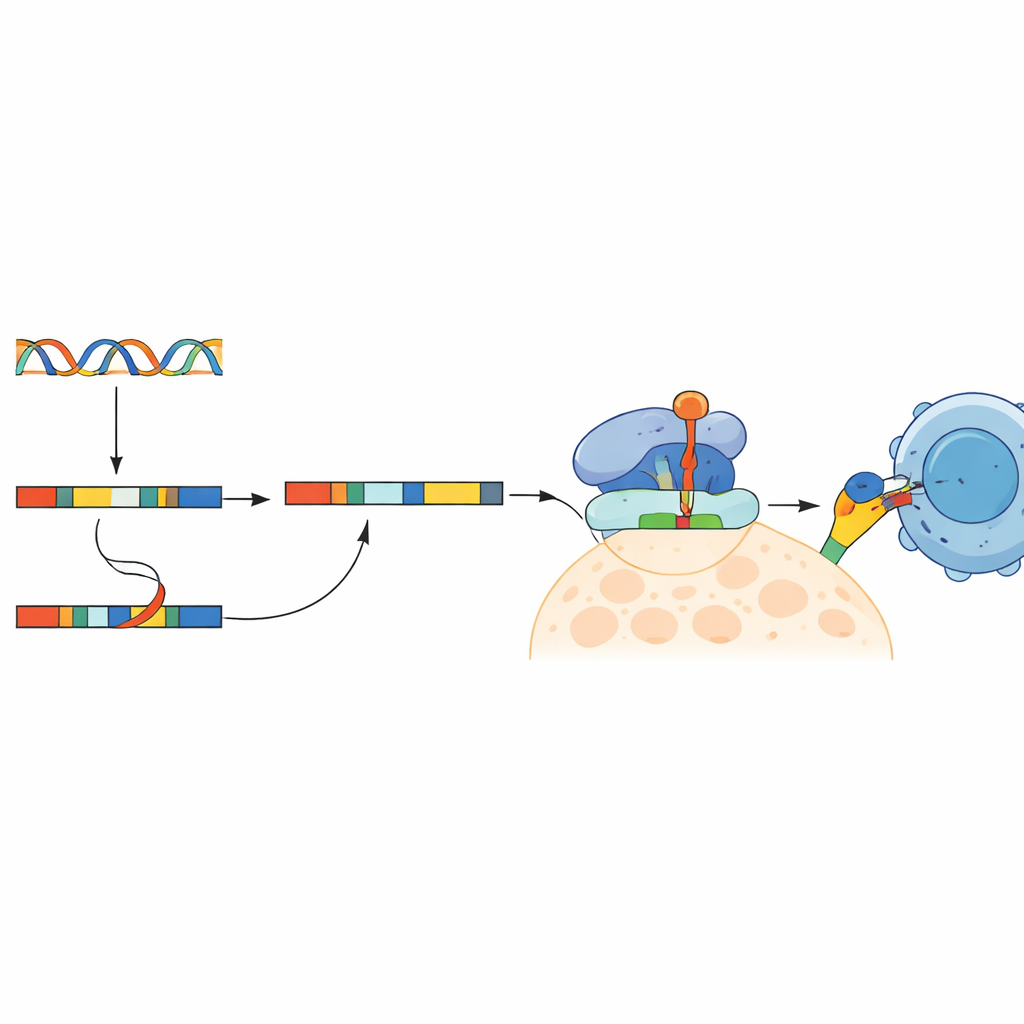
Les introns retenus font plus que surcharger l’ARN ; ils peuvent être convertis en fragments protéiques anormaux que le système immunitaire n’a jamais vus. Les chercheurs ont traduit les séquences d’introns retenus en courts peptides et utilisé des outils informatiques pour prédire lesquels pourraient se lier fortement aux molécules de présentation immunitaire courantes (protéines HLA) à la surface des cellules. Ils ont ensuite croisé ces peptides avec des jeux de données protéiques publics pour ne conserver que ceux observés dans des échantillons de cancer colorectal mais pas dans les tissus sains. À partir de ce crible, ils ont sélectionné un ensemble de peptides candidats et ont confirmé, via des tests PCR sensibles, que beaucoup des ARN contenant ces introns étaient effectivement présents à des niveaux plus élevés dans les tumeurs que dans les tissus normaux appariés.
Apprendre aux cellules T à reconnaître ces nouvelles cibles
Pour vérifier si ces fragments dérivés d’introns pouvaient réellement stimuler le système immunitaire, l’équipe a entraîné des lymphocytes T CD8 humains issus de donneurs sains en utilisant des cellules immunitaires cultivées en laboratoire chargées des peptides candidats. Plusieurs peptides ont déclenché des réponses fortes : les cellules T entraînées ont sécrété des signaux immunitaires, exprimé des marqueurs d’activation et montré des signes de cytotoxicité lorsqu’elles ont rencontré des cellules présentant le peptide correspondant. Des preuves supplémentaires par spectrométrie de masse suggèrent qu’au moins certains de ces peptides sont naturellement produits à l’intérieur des tumeurs colorectales. Fait notable, les auteurs ont également identifié 24 néoantigènes dérivés d’introns présents chez environ 30 % des patients et prédits comme de bons ligands des types HLA les plus courants du groupe, ce qui laisse entrevoir la possibilité de cibles vaccinales partagées, plutôt que purement individuelles.
Nouvelles voies vers des vaccins anticancéreux plus larges
Ce travail montre que la rétention d’introns — une bizarrerie autrefois négligée du traitement de l’ARN — peut générer de véritables cibles visibles par le système immunitaire sur les cellules du cancer colorectal. En prouvant que ces néoantigènes issus d’introns existent, qu’ils sont parfois partagés entre patients et qu’ils peuvent activer des cellules T cytotoxiques en laboratoire, l’étude ouvre la voie à une nouvelle classe d’ingrédients pour vaccins anticancéreux. Pour les patients dont les tumeurs manquent de nombreuses mutations classiques de l’ADN, en particulier ceux atteints d’un cancer colorectal microsatellite-stable, exploiter cette couche cachée de fragments protéiques anormaux pourrait considérablement élargir les options futures tant pour les immunothérapies personnalisées que prête-à-l’emploi.
Citation: Manoharan, T., Kee, B.B.R., Cheng, C.Z.M. et al. Identification of immunogenic neoantigens from intron retention in colorectal cancer. Sci Rep 16, 12796 (2026). https://doi.org/10.1038/s41598-026-43687-2
Mots-clés: cancer colorectal, vaccins contre le cancer, néoantigènes, rétention d’introns, immunothérapie