Clear Sky Science · zh
果蝇胶质瘤中促肿瘤Ca2+信号依赖Slowpoke和Ca-α1T通道
为何脑肿瘤与神经系统“对话”
胶质母细胞瘤是一种致命的脑癌,它并非孤立生长,而是融入大脑自身的电路,通过劫持正常信号来推动扩散并损伤周围神经元。本研究利用模式生物果蝇(Drosophila melanogaster),揭示了细胞膜上的微小孔道——离子通道——如何帮助肿瘤细胞放大内部的钙信号,从而驱动增殖、重塑连接并最终缩短寿命。通过明确哪些通道最为关键,这项工作为在更复杂动物(包括人类)中减缓侵袭性脑肿瘤提供了新的潜在途径。
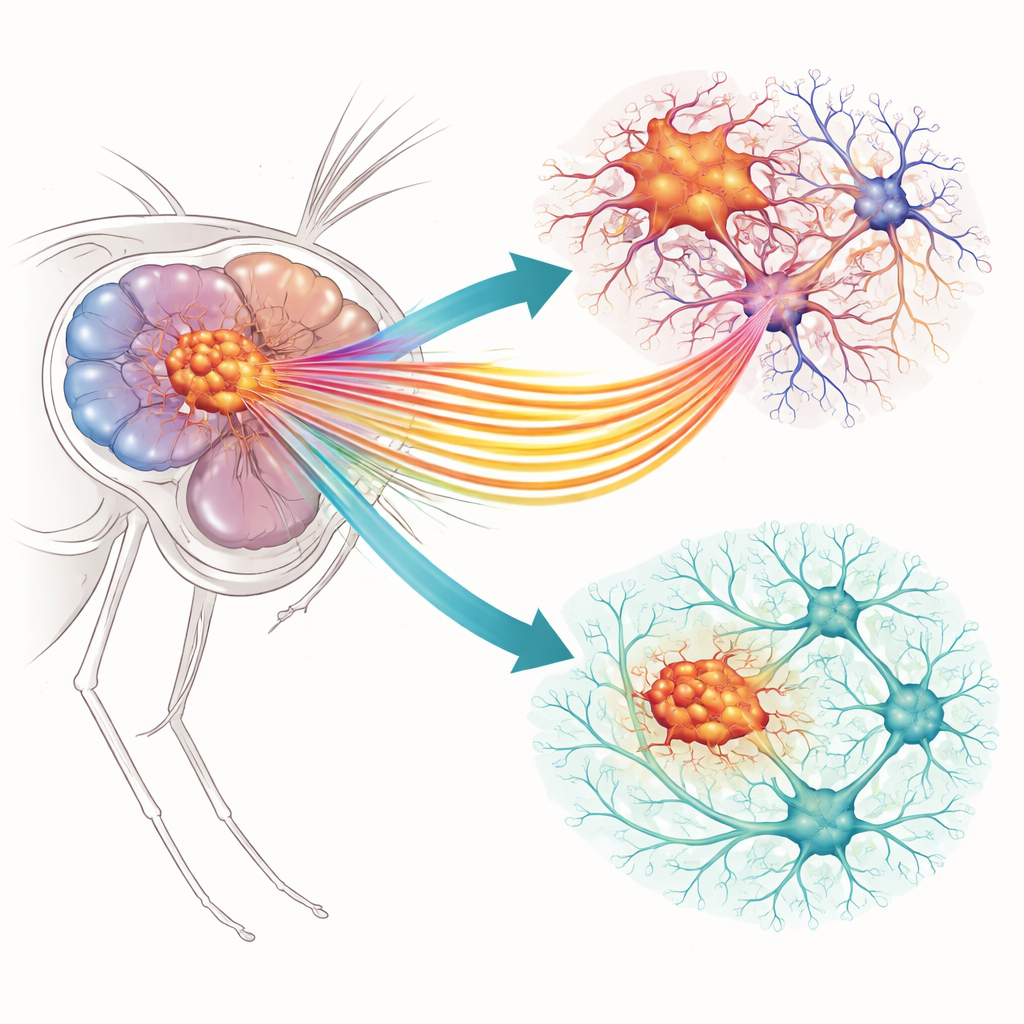
两扇微小的门,却有重大后果
研究者聚焦于胶质肿瘤细胞中的两种特定离子通道——胶质细胞是大脑中的支持细胞,但在肿瘤中已变为失控的一类细胞。其中一种称为Slo,当细胞内钙浓度升高时允许钾离子流出;另一种Ca-α1T则是在膜被激活时让钙离子流入。它们在哺乳动物中的近缘同源物已在体外人类胶质母细胞瘤研究中被关联,但在活体脑网络中的行为尚不清楚。研究团队使用一种成熟的果蝇模型,在该模型中胶质细胞带有类似癌变的增殖通路突变(EGFR和PI3K),这样他们得以比较正常脑与带肿瘤脑,并考察下调各通道对肿瘤行为及周围神经系统的影响。
为肿瘤生长“调低音量”
首先,科学家确认这两种通道在健康和带肿瘤的果蝇胶质细胞中均有表达。Ca-α1T在肿瘤细胞中表达略高,而Slo在正常与胶质瘤胶质细胞中的水平相近。随后他们使用靶向遗传工具(RNA干扰)仅在胶质细胞中降低每种通道的表达。在带胶质瘤的果蝇中,下调任一通道都会显著减少肿瘤胶质细胞数量,并缩小那些通常深入脑组织的膨胀胶质膜网络。对钙活动报告蛋白的测量显示,胶质瘤细胞通常表现出明显升高的钙信号,但当任一通道被沉默时,这种过度活跃回落至接近正常水平。与此同时,两条主要促生长通路ERK和PI3K的活性标志也被降低,表明这些膜通道有助于“供能”肿瘤内部的生长线路。
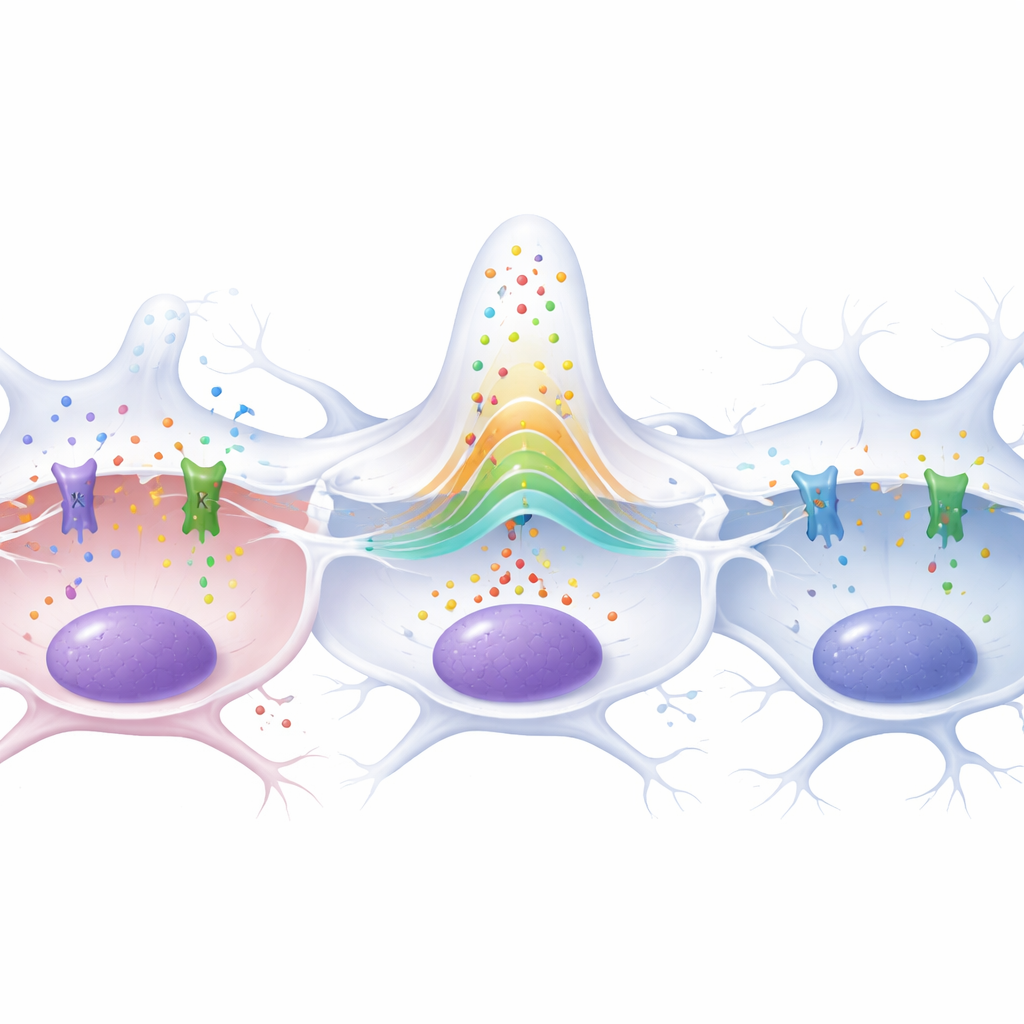
保护神经元并延长果蝇寿命
尽管两种通道都推动了增殖,但它们对大脑的影响并不完全相同。研究团队在神经肌肉接头处计数突触,这是一项敏感的果蝇神经元健康读数。带肿瘤的幼虫失去了约70%的这些突触,反映出强烈的肿瘤诱导性神经退行性变。下调Ca-α1T并未挽救这种丧失。相反,在肿瘤胶质细胞中减少Slo则显著将突触数量恢复至接近正常,表明Slo在胶质瘤如何伤害神经元方面具有特殊作用。这一差异在成虫中更为明显:带肿瘤的个体比健康对照早逝,但当在肿瘤细胞中降低Slo时,它们的生存曲线几乎与无肿瘤果蝇重合。相比之下,下调Ca-α1T并未延长寿命,甚至在健康果蝇中缩短了存活时间。
重塑代谢与化学通讯
为探明这些通道如何在基因层面重塑肿瘤细胞行为,作者对果蝇头部进行了RNA测序。肿瘤大脑显示出广泛的代谢与突触信号变化,包括碳水化合物利用和谷氨酸介导通信的增强,均是侵袭性胶质瘤的特征。下调Ca-α1T主要抑制了与糖分解和储存相关的基因活性,包括与“瓦尔堡效应”相关的酶类——即癌细胞依赖改变的葡萄糖代谢。另一方面,降低Slo则选择性地降低了编码关键谷氨酸受体亚基和帮助胶质瘤细胞与神经元形成并稳定连接的细胞黏附分子的基因表达。其中一种类似于人类AMPA型谷氨酸受体,先前已与肿瘤过度生长和预后不良相关;另一种则对应一种在人类中因过度活化而与更差生存相关的突触蛋白。
对未来脑癌治疗的意义
总体而言,这项研究表明Slo和Ca-α1T两种通道都作为钙依赖生长信号的放大器,帮助胶质瘤细胞增殖、伸展长膜管并维持强大的生长通路处于开启状态。然而,只有Slo显示出双重作用:不仅减缓肿瘤扩张,还保护神经元并延长带肿瘤动物的寿命。将Slo与异常的突触通讯和谷氨酸信号联系起来,提示其在人类中的近缘通道是特别有前景的靶点:阻断它们可能削弱肿瘤、切断其与神经元的有害对话并改善脑功能。尽管果蝇与患者相距甚远,但它们共享的分子机制使其成为指引未来应优先研究哪些通道和通路以用于胶质母细胞瘤治疗的有价值模型。
引用: Alza, L., Montes-Labrador, P., Megías, D. et al. Pro-tumoral Ca2+ signaling is dependent on Slowpoke and Ca-α1T channels in Drosophila melanogaster glioma. Sci Rep 16, 12297 (2026). https://doi.org/10.1038/s41598-026-42712-8
关键词: 胶质母细胞瘤, 钙信号, 离子通道, 谷氨酸受体, 脑肿瘤