Clear Sky Science · pt
Sinalização pró-tumoral por Ca2+ depende dos canais Slowpoke e Ca-α1T em glioma de Drosophila melanogaster
Por que tumores cerebrais se comunicam com o sistema nervoso
O glioblastoma, uma forma letal de câncer cerebral, não cresce isoladamente. Ele se integra à própria rede do cérebro, sequestrando sinais normais para alimentar sua disseminação e danificar neurônios vizinhos. Este estudo usa a mosca-da-fruta, Drosophila melanogaster, para descobrir como pequenos poros na membrana celular, chamados canais iônicos, ajudam as células tumorais a amplificar sinais internos de cálcio que impulsionam o crescimento, remodelam suas conexões e, em última instância, encurtam a expectativa de vida. Ao identificar quais canais são mais importantes, o trabalho sugere novas maneiras de desacelerar tumores cerebrais agressivos em animais mais complexos, inclusive em humanos.
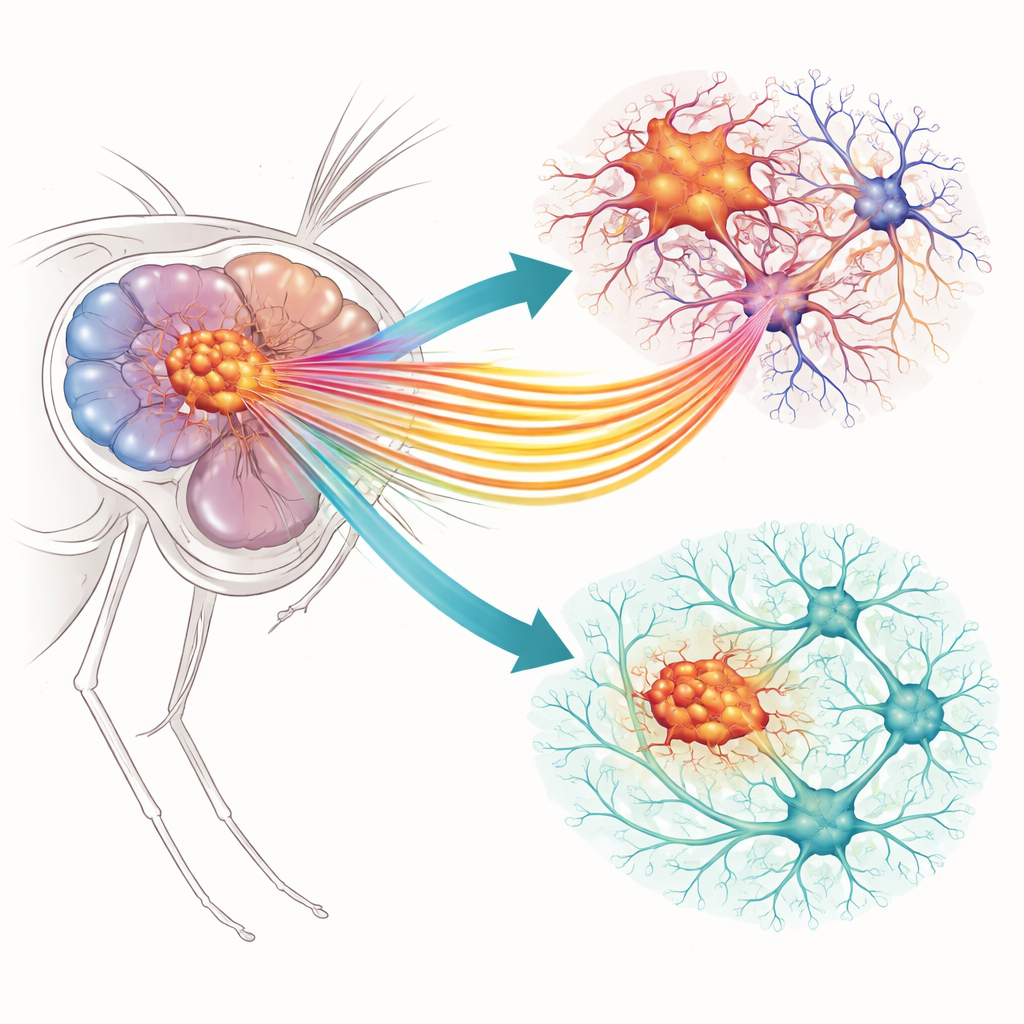
Dois portões minúsculos com grandes consequências
Os pesquisadores concentraram-se em dois canais iônicos específicos em células gliais tumorais, as células de suporte do cérebro que ficaram desreguladas. Um, chamado Slo, permite a saída de íons potássio da célula quando os níveis de cálcio aumentam. O outro, Ca-α1T, é um canal de cálcio que deixa íons cálcio entrarem quando a membrana celular é ativada. Seus equivalentes próximos em mamíferos já foram associados ao glioblastoma humano em culturas celulares, mas seu comportamento dentro de uma rede cerebral viva era menos claro. Usando um modelo bem estabelecido em moscas no qual as células gliais carregam mutações semelhantes a câncer em vias de crescimento (EGFR e PI3K), a equipe pôde comparar cérebros normais e com tumor e investigar como reduzir cada canal afetava o comportamento tumoral e o sistema nervoso circundante.
Reduzindo o volume do crescimento tumoral
Primeiro, os cientistas confirmaram que ambos os canais estão presentes em células gliais de cérebros de moscas saudáveis e com tumor. Ca-α1T apresentou níveis um tanto maiores em células tumorais, enquanto os níveis de Slo eram semelhantes em glia normal e em glioma. Em seguida, utilizaram ferramentas genéticas direcionadas (interferência por RNA) para diminuir a quantidade de cada canal apenas nas células gliais. Em moscas com gliomas, reduzir tanto Slo quanto Ca-α1T diminuiu drasticamente o número de células gliais tumorais e encolheu a rede de membrana glial inchada que normalmente se estende profundamente no tecido cerebral. Medições de um repórter de atividade de cálcio revelaram que as células do glioma normalmente exibem sinalização de cálcio fortemente elevada, mas essa hiperatividade caiu para níveis próximos ao normal quando qualquer um dos canais foi silenciado. Ao mesmo tempo, marcadores de duas vias principais que impulsionam o crescimento, ERK e PI3K, também foram reduzidos, mostrando que esses canais de membrana ajudam a alimentar a maquinaria interna de crescimento do tumor.
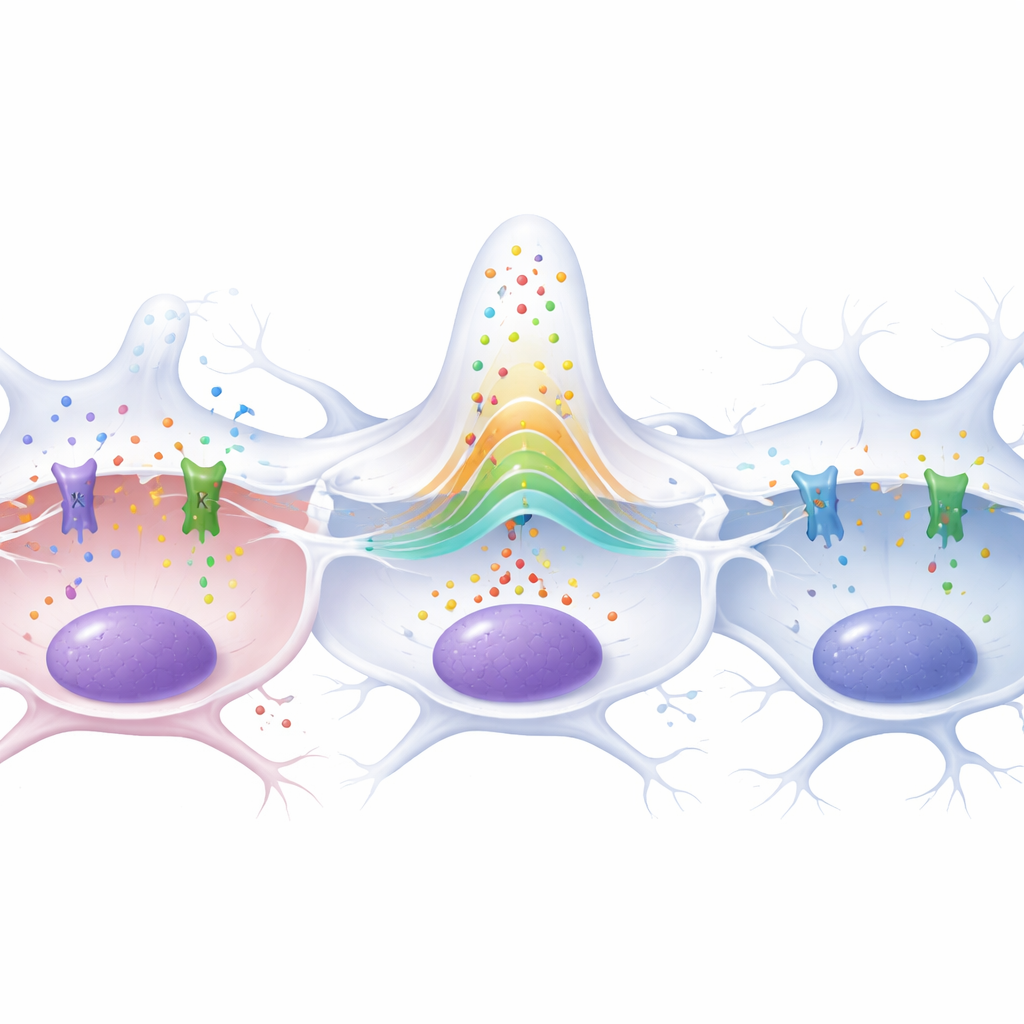
Protegendo neurônios e prolongando a vida das moscas
Embora ambos os canais contribuíssem para a proliferação, eles não tiveram efeitos idênticos no cérebro. A equipe contou sinapses na junção neuromuscular, uma medida sensível da saúde neuronal na mosca. Larvas com glioma perderam cerca de 70% dessas sinapses, refletindo forte neurodegeneração induzida pelo tumor. Reduzir Ca-α1T não reverteu essa perda. Em contraste, diminuir Slo nas glia tumorais restaurou significativamente o número de sinapses em direção ao normal, indicando que Slo tem um papel especial em como as células do glioma prejudicam neurônios. Essa diferença ficou ainda mais clara em moscas adultas: animais com gliomas morreram muito mais cedo que controles saudáveis, mas quando Slo foi reduzido nas células tumorais, as curvas de sobrevivência quase se sobrepuseram às das moscas sem tumor. Reduzir Ca-α1T, em comparação, não estendeu a vida e até encurtou a sobrevivência em moscas saudáveis.
Reprogramando metabolismo e comunicação química
Para entender como esses canais remodelam o comportamento das células tumorais ao nível gênico, os autores realizaram sequenciamento de RNA em cabeças de mosca. Cérebros tumorais mostraram amplas mudanças no metabolismo e na sinalização sináptica, incluindo aumento da atividade no uso de carboidratos e na comunicação baseada em glutamato, ambas características de gliomas agressivos. Reduzir Ca-α1T atenuou principalmente genes envolvidos na degradação e armazenamento de açúcar, incluindo enzimas relacionadas ao “efeito Warburg”, em que células cancerosas dependem fortemente de metabolismo de glicose alterado. Reduzir Slo, por outro lado, diminuiu seletivamente genes que codificam subunidades-chave de receptores de glutamato e moléculas de adesão celular que ajudam as células do glioma a formar e estabilizar conexões com neurônios. Um desses, semelhante a receptores de glutamato do tipo AMPA humanos, já foi associado a crescimento tumoral excessivo e piores desfechos, enquanto outro espelha uma proteína sináptica humana ligada a pior sobrevida quando hiperativa.
O que isso significa para futuras terapias contra câncer cerebral
No conjunto, o estudo mostra que tanto os canais Slo quanto Ca-α1T atuam como amplificadores de sinais de crescimento dependentes de cálcio em células de glioma, ajudando-as a se multiplicar, estender longos tubos de membrana e manter vias poderosas de crescimento ativas. Ainda assim, apenas Slo surge como uma alavanca dupla que não só desacelera a expansão tumoral, mas também protege neurônios e prolonga a vida de animais com tumor. Ao vincular Slo à comunicação sináptica anômala e à sinalização por glutamato, o trabalho aponta os parentes humanos desse canal como alvos especialmente promissores: bloqueá-los pode enfraquecer o tumor, cortar seu diálogo nocivo com neurônios e melhorar a função cerebral. Embora as moscas-da-fruta estejam longe de pacientes, sua maquinaria molecular compartilhada as torna um guia valioso para quais canais e vias merecem investigação mais próxima em futuras terapias para glioblastoma.
Citação: Alza, L., Montes-Labrador, P., Megías, D. et al. Pro-tumoral Ca2+ signaling is dependent on Slowpoke and Ca-α1T channels in Drosophila melanogaster glioma. Sci Rep 16, 12297 (2026). https://doi.org/10.1038/s41598-026-42712-8
Palavras-chave: glioblastoma, sinalização por cálcio, canais iônicos, receptores de glutamato, tumores cerebrais