Clear Sky Science · es
La señalización de Ca2+ pro-tumoral depende de los canales Slowpoke y Ca-α1T en glioma de Drosophila melanogaster
Por qué los tumores cerebrales hablan con el sistema nervioso
El glioblastoma, una forma mortal de cáncer cerebral, no crece aislado. Se integra en el cableado del propio cerebro, secuestrando señales normales para alimentar su expansión y dañar a las neuronas vecinas. Este estudio usa la mosca de la fruta, Drosophila melanogaster, para descubrir cómo pequeños poros en las membranas celulares, llamados canales iónicos, ayudan a las células tumorales a amplificar señales internas de calcio que impulsan el crecimiento, remodelan sus conexiones y, en última instancia, acortan la esperanza de vida. Al identificar qué canales son los más importantes, el trabajo sugiere nuevas formas de frenar tumores cerebrales agresivos en animales más complejos, incluidos los humanos.
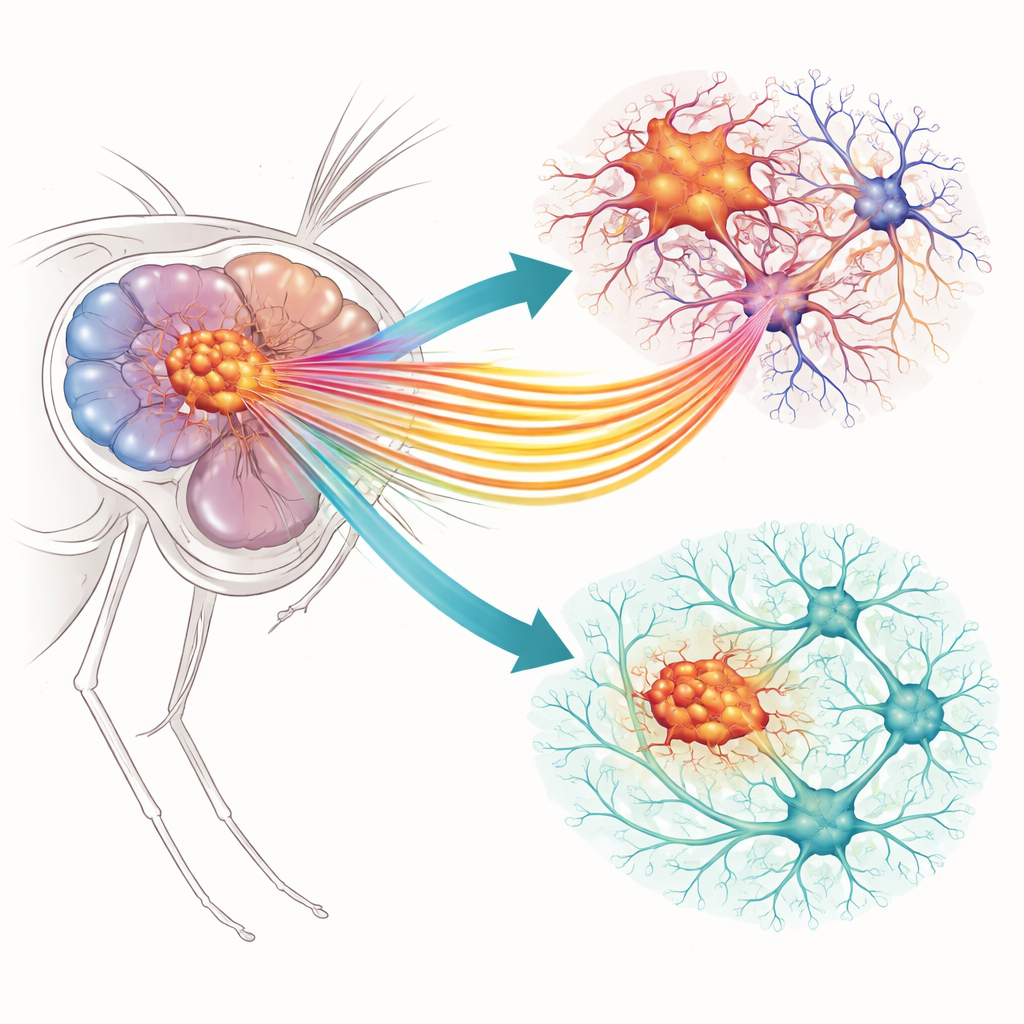
Dos puertas diminutas con grandes consecuencias
Los investigadores se centraron en dos canales iónicos específicos en las células gliales tumorales, las células de soporte del cerebro que se han vuelto perjudiciales. Uno, llamado Slo, permite la salida de iones potasio de la célula cuando los niveles de calcio aumentan. El otro, Ca-α1T, es un canal de calcio que deja entrar iones de calcio cuando se activa la membrana celular. Sus homólogos próximos en mamíferos ya se han relacionado con el glioblastoma humano en cultivos celulares, pero su comportamiento dentro de una red cerebral viva era menos claro. Usando un modelo de mosca bien establecido en el que las células gliales presentan mutaciones similares al cáncer en vías de crecimiento (EGFR y PI3K), el equipo pudo comparar cerebros normales con los que contienen tumores y estudiar cómo afecta a la conducta tumoral reducir la actividad de cada canal.
Reducir el volumen del crecimiento tumoral
Primero, los científicos confirmaron que ambos canales están presentes en las células gliales de cerebros sanos y con tumores en moscas. Ca-α1T mostró niveles algo más altos en las células tumorales, mientras que los niveles de Slo eran similares en la glía normal y en la glía con glioma. Luego usaron herramientas genéticas dirigidas (interferencia por RNA) para disminuir la cantidad de cada canal únicamente en las células gliales. En moscas con gliomas, reducir Slo o Ca-α1T disminuyó drásticamente el número de células gliales tumorales y redujo la red de membrana glial hinchada que normalmente se extiende profundamente en el tejido cerebral. Mediciones de un reporter de actividad de calcio revelaron que las células del glioma muestran normalmente una señalización de calcio notablemente elevada, pero esta hiperactividad volvió a niveles cercanos a la normalidad cuando se silenció cualquiera de los dos canales. Al mismo tiempo, los marcadores de dos grandes vías pro-crecimiento, ERK y PI3K, también se redujeron, lo que muestra que estos canales de membrana ayudan a alimentar la maquinaria interna de crecimiento del tumor.
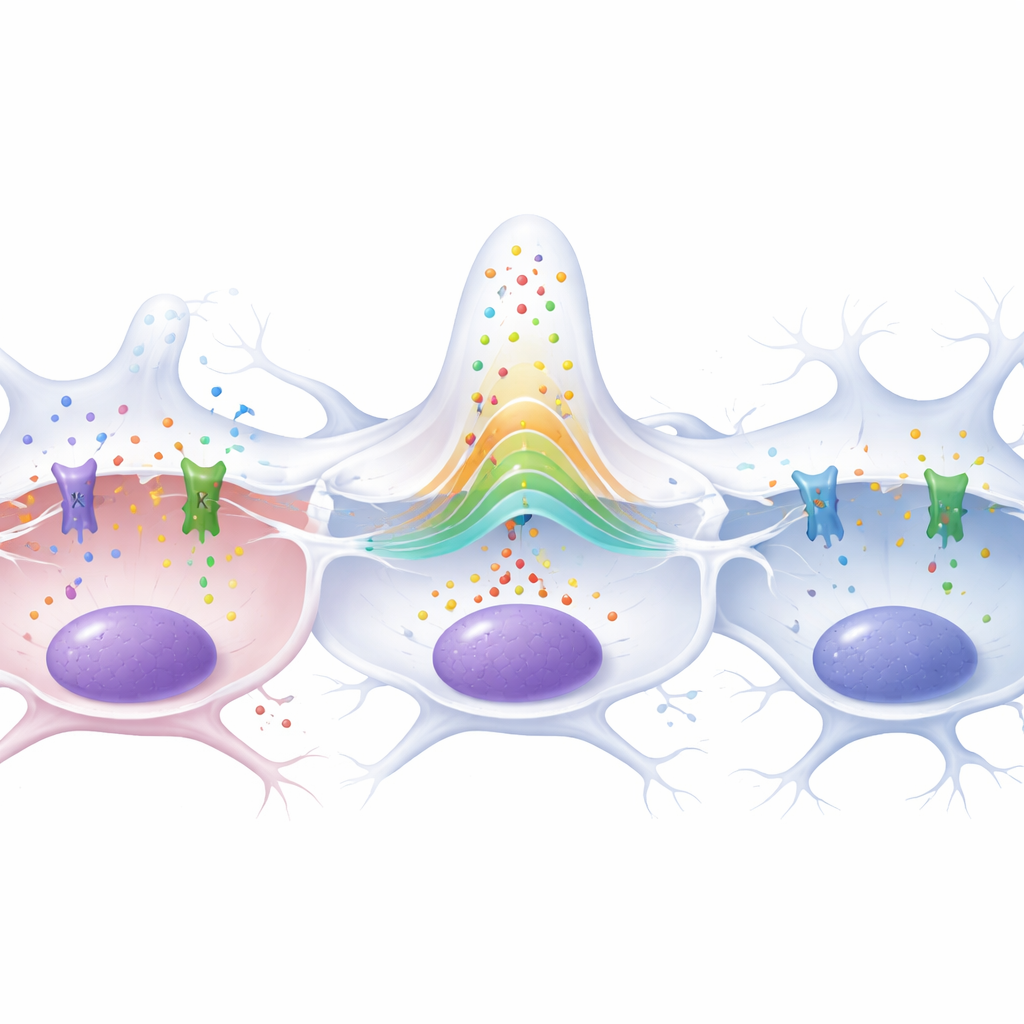
Protección de neuronas y extensión de la vida en moscas
Aunque ambos canales impulsaban la proliferación, no tuvieron efectos idénticos en el cerebro. El equipo contó sinapsis en la unión neuromuscular, una medida sensible de la salud neuronal en la mosca. Las larvas con glioma perdieron alrededor del 70 por ciento de estas sinapsis, lo que refleja una fuerte neurodegeneración inducida por el tumor. Reducir Ca-α1T no rescató esta pérdida. En contraste, disminuir Slo en la glía tumoral restauró de forma significativa el número de sinapsis hacia valores normales, lo que indica que Slo tiene un papel especial en cómo las células de glioma dañan a las neuronas. Esta diferencia quedó aún más clara en moscas adultas: los animales con gliomas murieron mucho antes que los controles sanos, pero cuando Slo se redujo en las células tumorales, sus curvas de supervivencia casi se solaparon con las de las moscas sin tumor. Disminuir Ca-α1T, en comparación, no prolongó la vida y hasta acortó la supervivencia en moscas sanas.
Reconfiguración del metabolismo y de la comunicación química
Para ver cómo estos canales remodelan el comportamiento de las células tumorales a nivel génico, los autores realizaron secuenciación de RNA en cabezas de mosca. Los cerebros tumorales mostraron cambios amplios en el metabolismo y en la señalización sináptica, incluidos aumentos en el uso de carbohidratos y en la comunicación basada en glutamato, ambos rasgos distintivos de gliomas agresivos. Apagar Ca-α1T atenuó principalmente genes implicados en la degradación y el almacenamiento de azúcares, incluidas enzimas vinculadas al “efecto Warburg”, en el que las células tumorales dependen en gran medida de un metabolismo de la glucosa alterado. Reducir Slo, por otro lado, disminuyó de forma selectiva genes que codifican subunidades clave de receptores de glutamato y moléculas de adhesión celular que ayudan a las células de glioma a formar y estabilizar conexiones con neuronas. Uno de estos, similar a los receptores de glutamato tipo AMPA humanos, se ha relacionado previamente con el sobrecrecimiento tumoral y malos resultados, mientras que otro refleja una proteína sináptica humana asociada a peor supervivencia cuando está sobreactivada.
Qué significa esto para futuras terapias contra el cáncer cerebral
En conjunto, el estudio demuestra que tanto los canales Slo como Ca-α1T actúan como amplificadores de señales de crecimiento dependientes de calcio en las células de glioma, ayudándolas a multiplicarse, extender largos tubos de membrana y mantener activadas potentes vías de crecimiento. Sin embargo, solo Slo emerge como una palanca doble que no solo frena la expansión tumoral sino que también protege a las neuronas y prolonga la vida de los animales con tumor. Al vincular a Slo con la comunicación sináptica anormal y la señalización por glutamato, el trabajo señala a los parientes humanos de este canal como objetivos especialmente prometedores: bloquearlos podría debilitar el tumor, cortar su diálogo dañino con las neuronas y mejorar la función cerebral. Aunque las moscas de la fruta están lejos de los pacientes, su maquinaria molecular compartida las convierte en una guía valiosa para saber qué canales y vías merecen una atención más cercana en futuras terapias del glioblastoma.
Cita: Alza, L., Montes-Labrador, P., Megías, D. et al. Pro-tumoral Ca2+ signaling is dependent on Slowpoke and Ca-α1T channels in Drosophila melanogaster glioma. Sci Rep 16, 12297 (2026). https://doi.org/10.1038/s41598-026-42712-8
Palabras clave: glioblastoma, señalización de calcio, canales iónicos, receptores de glutamato, tumores cerebrales