Clear Sky Science · ar
إشارات Ca2+ المساعدة للورم تعتمد على قناتي Slowpoke وCa-α1T في ورم الغليوما لدى ذبابة الفاكهة Drosophila melanogaster
لماذا تتواصل أورام الدماغ مع الجهاز العصبي
الورم الأرومي الدبقي، وهو شكل قاتل من سرطان الدماغ، لا ينمو بمعزل عن محيطه. إنه يندمج في توصيلات الدماغ نفسها، ويختطف الإشارات الطبيعية لتغذية انتشاره وإلحاق الضرر بالخلايا العصبية المجاورة. تستخدم هذه الدراسة ذبابة الفاكهة، Drosophila melanogaster، للكشف عن كيفية مساهمة مسامٍ صغيرة في أغشية الخلايا، تُعرف بقنوات الأيونات، في تضخيم إشارات الكالسيوم الداخلية للخلايا الورمية التي تدفع النمو وإعادة تشكيل الاتصالات وتقصير العمر في نهاية المطاف. من خلال تحديد القنوات الأكثر أهمية، يقترح العمل طرقًا جديدة لإبطاء الأورام الدماغية العدوانية في حيوانات أكثر تعقيدًا، بما في ذلك البشر.
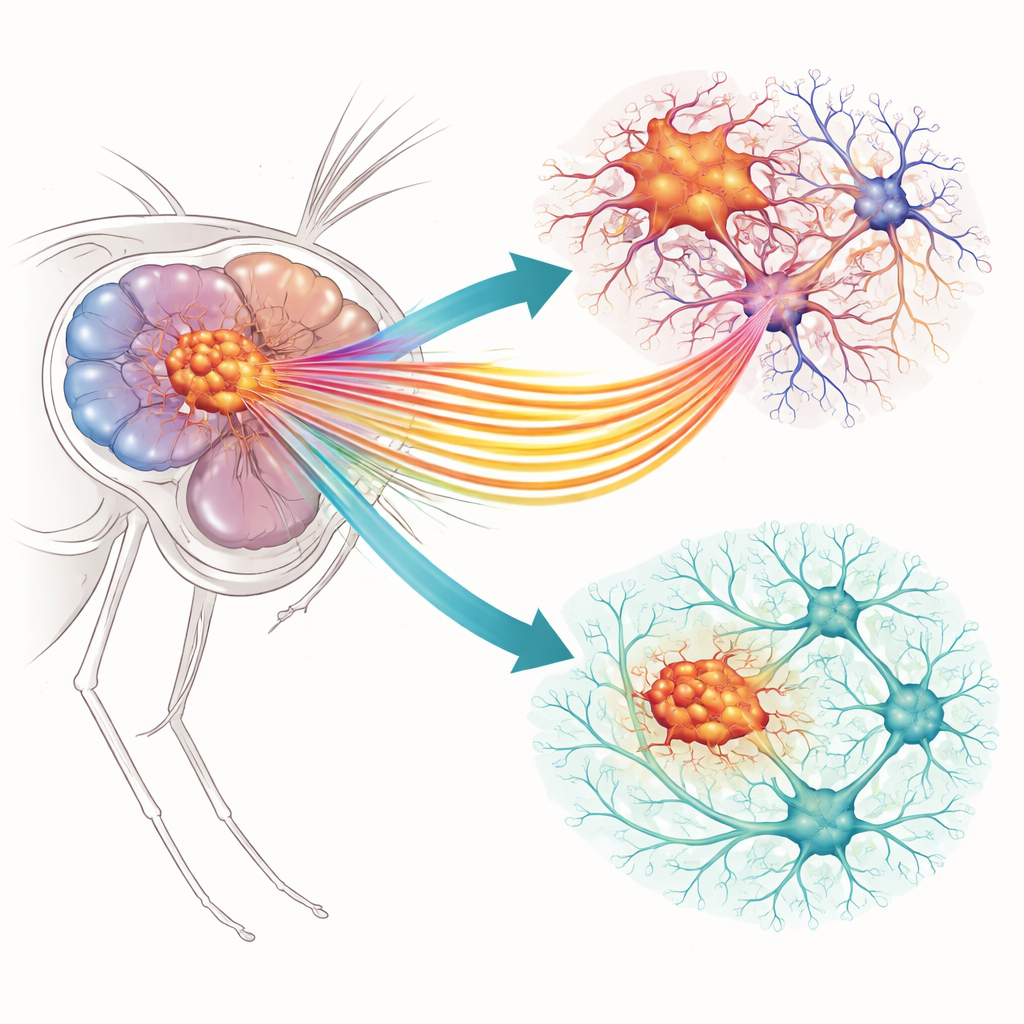
بوابتان صغيرتان بتبعات كبيرة
ركز الباحثون على قناتي أيونات محددتين في خلايا الغليا الورمية، وهي خلايا دعم الدماغ التي تحولت إلى خبيثة. الأولى، المسماة Slo، تسمح لأيونات البوتاسيوم بالخروج من الخلية عندما ترتفع مستويات الكالسيوم. والثانية، Ca-α1T، هي قناة كالسيوم تسمح بدخول أيونات الكالسيوم عند تنشيط غشاء الخلية. نظيرات هذه القنوات في الثدييات ارتبطت بالفعل بالورم الأرومي الدبقي في زراعة الخلايا البشرية، لكن سلوكها داخل شبكة الدماغ الحية كان أقل وضوحًا. باستخدام نموذج ذبابي راسخ حيث تحمل خلايا الغليا طفرات شبيهة بالسرطان في مسارات النمو (EGFR وPI3K)، تمكن الفريق من مقارنة الأدمغة الطبيعية بأدمغة حاملة للأورام والاستفهام كيف يؤثر خفض نشاط كل قناة على سلوك الورم والجهاز العصبي المحيط.
خفض مستوى صوت نمو الورم
أولًا، أكد العلماء أن كلا القناتين موجودتان في خلايا الغليا في أدمغة الذباب السليمة والحاملة للورم. أظهرت Ca-α1T مستويات أعلى قليلًا في الخلايا الورمية، بينما كانت مستويات Slo متشابهة في الغليا العادية والورمية. ثم استخدموا أدوات جينية مستهدفة (تداخل الحمض النووي الريبي) لتقليل كمية كل قناة في خلايا الغليا فقط. في الذباب الحامل للأورام، قلل خفض أي من Slo أو Ca-α1T بشكل حاد من عدد خلايا الغليا الورمية وصغّر شبكة الأغشية المتضخمة للخلايا الغليالية التي تمتد عادة عميقًا داخل نسيج الدماغ. كشفت قياسات مؤشر نشاط الكالسيوم أن خلايا الغليوما تظهر عادة نشاطًا كالسيوميًّا مرتفعًا بشكل ملحوظ، لكن هذه النشاطية المفرطة انخفضت إلى مستويات قريبة من الطبيعي عندما تم كبح أي من القناتين. وفي الوقت نفسه، انخفضت مؤشرات مسارين رئيسيين يقودان النمو، ERK وPI3K، ما يدل على أن هذه القنوات الغشائية تساعد في تغذية الدارات الداخلية لنمو الورم.
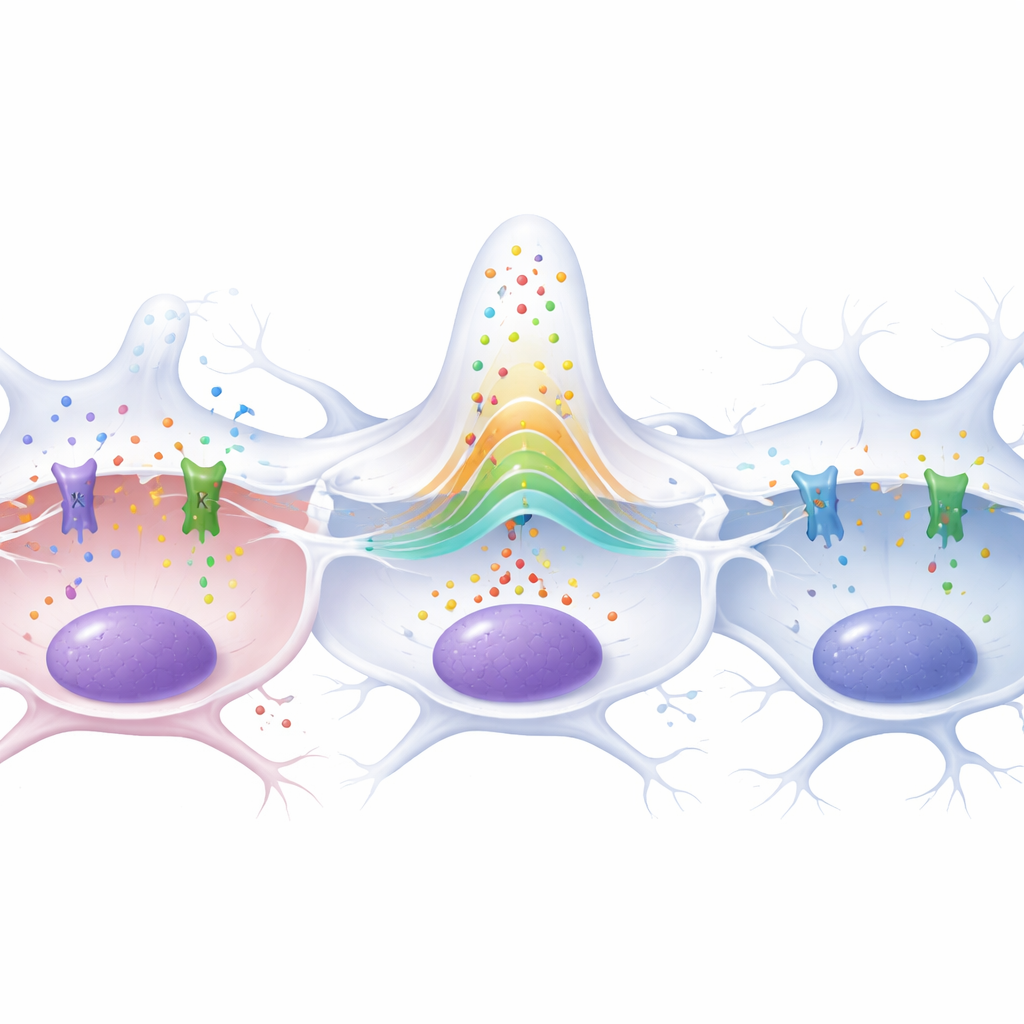
حماية الخلايا العصبية وإطالة العمر لدى الذباب
مع أن كلتا القناتين ساعدتا في تحفيز التكاثر، إلا أنهما لم تتركا نفس الأثر على الدماغ. قام الفريق بعدّ المشابك عند الوصلة العصبية العضلية، وهو مقياس حساس لصحة الخلايا العصبية في الذبابة. فقدت يرقات حاملة للغليوما نحو 70 بالمئة من هذه المشابك، ما يعكس تنكّس عصبي كبير سببته الأورام. لم ينجح خفض Ca-α1T في إنقاذ هذا الفقدان. بالمقابل، أدى تقليل Slo في غليا الورم إلى استعادة عدد المشابك بشكل ملحوظ باتجاه الطبيعي، مما يشير إلى أن لـSlo دورًا خاصًا في كيفية إلحاق خلايا الغليوما الضرر بالخلايا العصبية. تبلور هذا الاختلاف أكثر في الذباب البالغ: فالحيوانات الحاملة للأورام ماتت في وقت أبكر بكثير من الشواهد السليمة، لكن عندما خُفض Slo في خلايا الورم، تقاربت منحنيات النجاة لديها مع منحنيات الذباب غير الحامل للأورام. أما خفض Ca-α1T، بالمقارنة، فلم يطِل العمر بل قلّل البقاء حتى في الذباب السليم.
إعادة توصيل الأيض والتواصل الكيميائي
لمعرفة كيف تعيد هذه القنوات تشكيل سلوك الخلايا الورمية على مستوى الجينات، أجرى المؤلفون تسلسلًا للـRNA على رؤوس الذباب. أظهرت أدمغة الأورام تغييرات واسعة في الأيض والإشارات المشبكية، بما في ذلك زيادة النشاط في استخدام الكربوهيدرات والتواصل المعتمد على الغلوتاميت، وهما علامتان مميزتان للأورام الأرومية العدوانية. أدى كبح Ca-α1T أساسًا إلى إضعاف الجينات المشاركة في تحطيم السكر وتخزينه، بما في ذلك إنزيمات مرتبطة بتأثير واربورغ، حيث تعتمد الخلايا السرطانية اعتمادًا كبيرًا على تماثل استقلاب الجلوكوز. أما تقليل Slo، فخَفَّض انتقائيًا الجينات التي تشفر وحدات فرعية رئيسية من مستقبلات الغلوتاميت وجزيئات التصاق خلوية تساعد خلايا الغليوما على تشكيل وتثبيت الروابط مع الخلايا العصبية. واحد من هذه الجينات، الشبيه بمستقبلات AMPA البشرية للغلوتاميت، ارتبط سابقًا بفرط نمو الورم ونتائج سيئة، بينما يناظر آخر بروتينًا مشبكيًا بشريًا يرتبط بتدهور البقاء عند فرطه في النشاط.
ما الذي يعنيه هذا لعلاجات سرطان الدماغ المستقبلية
بشكل عام، تُظهر الدراسة أن كلًا من قناتي Slo وCa-α1T تعملان كمضخمات للإشارات المعتمدة على الكالسيوم في خلايا الغليوما، مما يساعدها على التكاثر، وإطالة أنابيب غشائية طويلة، وإبقاء مسارات النمو القوية مفعلة. ومع ذلك، يبرز Slo كرافعة مزدوجة لا تبطئ توسع الورم فحسب، بل تحمي أيضًا الخلايا العصبية وتطيل عمر الحيوانات الحاملة للورم. من خلال ربط Slo بالتواصل المشبكي الشاذ وإشارات الغلوتاميت، يشير العمل إلى أن نظائر هذه القناة لدى البشر تعد أهدافًا واعدة بشكل خاص: قد يؤدي حجبها إلى إضعاف الورم، وقطع حواره الضار مع الخلايا العصبية، وتحسين وظيفة الدماغ. وعلى الرغم من أن ذباب الفاكهة يبعد كثيرًا عن المرضى، فإن اشتراكه في الآليات الجزيئية يجعل منه دليلًا قيّمًا لتحديد القنوات والمسارات التي تستدعي أقرب اهتمام في علاجات الورم الأرومي الدبقي المستقبلية.
الاستشهاد: Alza, L., Montes-Labrador, P., Megías, D. et al. Pro-tumoral Ca2+ signaling is dependent on Slowpoke and Ca-α1T channels in Drosophila melanogaster glioma. Sci Rep 16, 12297 (2026). https://doi.org/10.1038/s41598-026-42712-8
الكلمات المفتاحية: الورم الأرومي الدبقي, الإشارات الكلسية, قنوات الأيونات, مستقبلات الغلوتاميت, أورام الدماغ