Clear Sky Science · sv
Pro-tumoral Ca2+-signalering är beroende av Slowpoke och Ca-α1T-kanaler i Drosophila melanogaster-gliom
Varför hjärntumörer kommunicerar med nervsystemet
Glioblastom, en dödlig form av hjärncancer, växer inte isolerat. Det väver in sig i hjärnans egna ledningsnät och kapar normala signaler för att driva sin spridning och skada intilliggande neuroner. Den här studien använder bananflugan, Drosophila melanogaster, för att ta reda på hur små porer i cellmembran — så kallade jonkanaler — hjälper tumörceller att förstärka interna kalciumsignaler som främjar tillväxt, omformar deras förbindelser och i slutänden förkortar livslängden. Genom att peka ut vilka kanaler som spelar störst roll föreslår arbetet nya vägar för att bromsa aggressiva hjärntumörer i mer komplexa djur, inklusive människor.
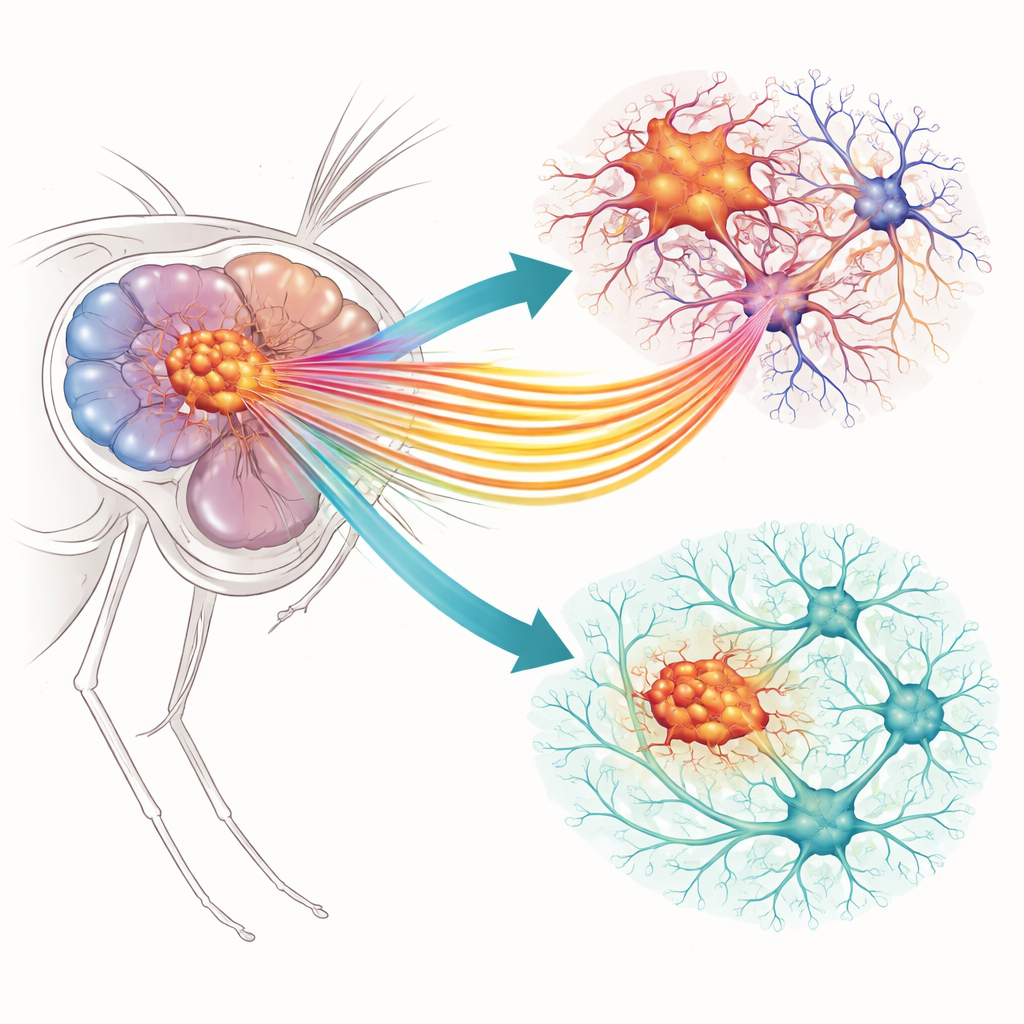
Två små portar med stora konsekvenser
Forskarna fokuserade på två specifika jonkanaler i gliala tumörceller, hjärnans stödjeceller som gått ur kontroll. Den ena, kallad Slo, släpper ut kaliumjoner ur cellen när kalciumnivåerna stiger. Den andra, Ca-α1T, är en kalciumkanal som tillåter kalciumjoner att komma in när cellmembranet aktiveras. Deras nära motsvarigheter hos däggdjur har redan kopplats till mänskligt glioblastom i cellkulturer, men deras beteende i ett levande hjärnnätverk var mindre tydligt. Med en väletablerad flugmodell där gliala celler bär cancerlika mutationen i tillväxtvägar (EGFR och PI3K) kunde teamet jämföra normala hjärnor med tumörbärande och undersöka hur nedreglering av varje kanal påverkade tumörbeteendet och det omgivande nervsystemet.
Sänka volymen på tumörtillväxten
Först bekräftade forskarna att båda kanalerna finns i gliala celler i friska och tumörbärande flughjärnor. Ca-α1T visade något högre nivåer i tumörceller, medan Slo-nivåerna var liknande i normala och gliomglia. De använde sedan riktade genetiska verktyg (RNA-interferens) för att minska mängden av varje kanal endast i gliala celler. I flugor med gliom minskade både Slo och Ca-α1T kraftigt antalet tumörgliala celler och krympte det svullna gliala membrannätverket som normalt går djupt in i hjärnvävnaden. Mätningar med en kalcium-aktivitetsrapportör visade att gliomceller normalt uppvisar markant förhöjd kalciumsignalering, men denna hyperaktivitet föll tillbaka till nära normala nivåer när antingen kanal tystades. Samtidigt minskade även markörer för två stora tillväxtdrivande vägar, ERK och PI3K, vilket visar att dessa membrankanaler hjälper till att mata tumörens interna tillväxtkretsar.
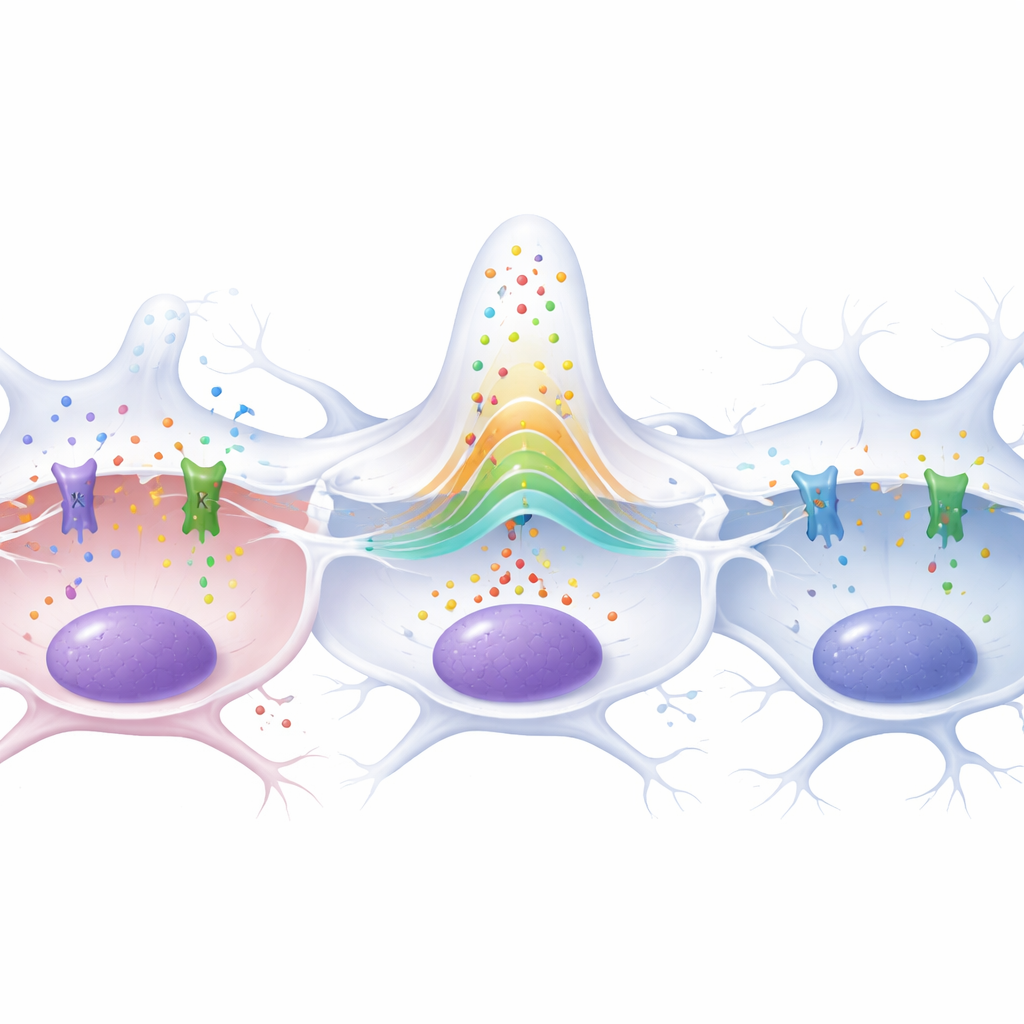
Skydda neuroner och förlänga livet hos flugor
Även om båda kanalerna bidrog till proliferation hade de inte identiska effekter på hjärnan. Teamet räknade synapser vid neuromuskulära kontakten, ett känsligt mått på neuronhälsa hos flugan. Larver med gliom förlorade cirka 70 procent av dessa synapser, vilket speglar stark tumörinducerad neurodegeneration. Att minska Ca-α1T återställde inte denna förlust. Däremot återställde nedreglering av Slo i tumörglia signifikant synapsantalet mot det normala, vilket indikerar att Slo har en särskild roll i hur gliomceller skadar neuroner. Denna skillnad blev ännu tydligare hos vuxna flugor: djur med gliom dog mycket tidigare än friska kontroller, men när Slo reducerades i tumörcellerna låg deras överlevnadskurvor nästan ihop med icke-tumörflugor. Att sänka Ca-α1T förlängde däremot inte livslängden och förkortade till och med överlevnaden hos friska flugor.
Omkoppling av metabolism och kemisk kommunikation
För att se hur dessa kanaler omformar tumörcellernas beteende på gennivå utförde författarna RNA-sekvensering på flughuvuden. Tumörhjärnor visade breda skift i metabolism och synaptisk signalering, inklusive ökad aktivitet i kolhydratanvändning och glutamatbaserad kommunikation — båda kännetecken för aggressiva gliom. Att dämpa Ca-α1T påverkade främst gener involverade i sockernedbrytning och lagring, inklusive enzymer kopplade till "Warburg-effekten", där cancerceller i hög grad förlitar sig på förändrad glukosmetabolism. Att minska Slo, däremot, sänkte selektivt gener som kodar för viktiga glutamatreceptorsubenheter och cell-adhesionsmolekyler som hjälper gliomceller att bilda och stabilisera förbindelser med neuroner. En av dessa, lik en human AMPA-typ glutamatreceptor, har tidigare kopplats till tumöröverväxt och dåliga utfall, medan en annan speglar ett mänskligt synaptiskt protein som är förknippat med sämre överlevnad när det är överaktivt.
Vad detta betyder för framtida behandlingar mot hjärncancer
Sammanfattningsvis visar studien att både Slo- och Ca-α1T-kanaler fungerar som förstärkare av kalciumberoende tillväxtsignaler i gliomceller, vilket hjälper dem att multiplicera, förlänga långa membranrör och hålla kraftfulla tillväxtvägar aktiverade. Endast Slo framträder dock som en dubbelspak som inte bara bromsar tumörexpansion utan också skyddar neuroner och förlänger livet hos tumörbärande djur. Genom att knyta Slo till onormal synaptisk kommunikation och glutamatsignalering pekar arbetet på kanalens mänskliga släktingar som särskilt lovande mål: att blockera dem kan försvaga tumören, skära av dess skadliga dialog med neuroner och förbättra hjärnfunktionen. Medan bananflugor är långt ifrån patienter gör deras delade molekylära maskineri dem till en värdefull vägvisare för vilka kanaler och vägar som förtjänar närmast uppmärksamhet i framtida glioblastombehandlingar.
Citering: Alza, L., Montes-Labrador, P., Megías, D. et al. Pro-tumoral Ca2+ signaling is dependent on Slowpoke and Ca-α1T channels in Drosophila melanogaster glioma. Sci Rep 16, 12297 (2026). https://doi.org/10.1038/s41598-026-42712-8
Nyckelord: glioblastom, kalciumsignalering, jonkanaler, glutamatreceptorer, hjärntumörer