Clear Sky Science · zh
一个分数阶疫苗模型用于根据真实数据分析天花猴痘(Mpox)I 与 II 分支的动态
这为何关系到日常健康
猴痘(Mpox)曾主要在非洲部分地区零星出现,但近来成为全球关注的焦点。现在流行两种不同形式或分支:一种更严重,另一种较轻但传播广泛。本研究提出了一个具有重大公共卫生意义的实际问题:在疫苗有限且人与动物之间传播复杂的情况下,我们能否用数学来理解猴痘的传播方式,以及疫苗接种能否最终将其控制住?
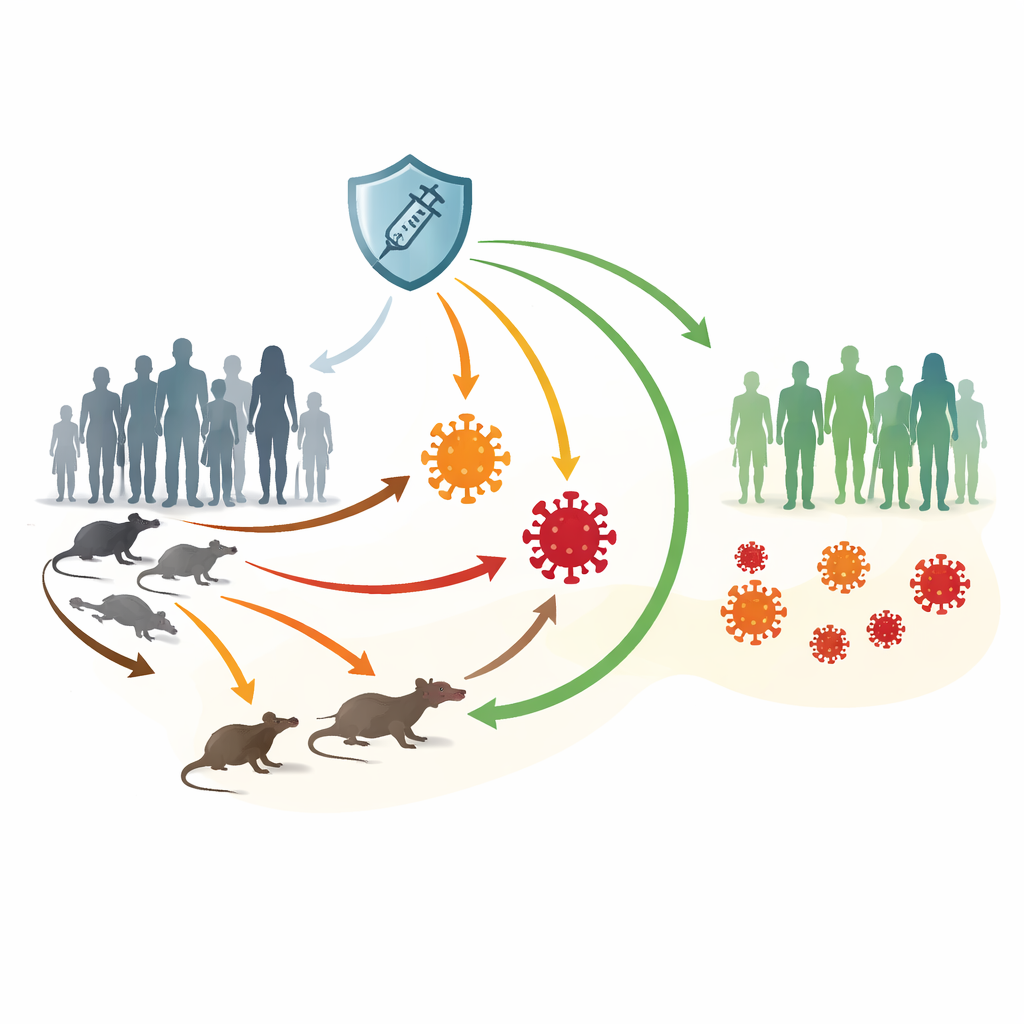
两种病毒与多条传播路径
研究者关注猴痘病毒的 I 分支与 II 分支。I 分支在一些非洲国家仍然常见,能引起更严重的疾病和更高的死亡率。II 分支导致了 2022 年的全球暴发,通常症状较轻但通过密切和亲密接触广泛传播,尤其在特定高风险人群中。猴痘可以在人与啮齿动物之间互相传播,并在动物群体中潜伏循环,这使得消除更为困难。诸如 JYNNEOS 的疫苗可提供强有力的保护,但全球供应不均且免疫可能随时间减弱。
把猴痘转化为人与动物的流动模型
为了解开这种复杂性,作者构建了一个分舱模型,用以追踪个体在不同健康状态之间的流动。人群从易感开始,可接种提供暂时但强保护的疫苗,接触感染后成为暴露者,然后发展为感染 I 或 II 分支的病例。有些人需要住院治疗,而另一些则直接康复。与此同时,啮齿动物被分为健康组和感染组。模型中的箭头表示所有主要传播途径:人传人、动物传人、人传动物及动物传动物。该框架使团队得以检验接触频率、疫苗接种和免疫丧失变化如何在人人与动物群体中产生连锁反应。
给数学加入记忆
作者没有仅使用标准方程(这些方程假定感染与康复遵循简单均匀的时间线),而是采用了分数阶方法。通俗地说,这给模型加入了内在的“记忆”:过去的事件会以渐进的方式持续影响当前的感染水平。这更贴近真实暴发情形,其中潜伏期、康复和行为在个体之间差异很大。团队先写出传统版本的模型,然后把它扩展到分数阶框架,并证明其解在生物学上是合理的(不存在负数人口或无限发散)且在数学上良态且唯一。
模型对传播与控制的启示
研究者使用 2025 年 1 月至 7 月的美国 II 分支病例数据拟合模型并估计基础再生数——即在完全易感人群中一名感染者平均能产生的新感染数。他们得到约 1.33 的值,意味着每例可产生多于一例的新感染,病毒因此能够持续存在。他们还推导出考虑免疫接种后的“疫苗再生数”。理论上当此值降至 1 以下时,无感染状态变为稳定。然而,模型同时揭示了一种称为后向分岔(backward bifurcation)的现象:即便再生数被轻微压低至 1 以下,猴痘仍可能以低但稳定的水平持续存在,尤其在存在多条传播路线和免疫衰减时。
哪些调节杆最关键
为了看哪些因素对传播影响最大,团队在合理范围内改变参数(如接触率和动物死亡率),并测量再生数的响应。分析显示,感染与易感啮齿动物之间的频繁接触,以及啮齿动物与人之间的接触,会显著提高传播;而啮齿动物种群更快的自然更新则有助于抑制传播。两种分支之间的人传人接触以及感染啮齿动物与人的接触也起主要作用。相比之下,一些临床细节,如具体的住院率和康复率,对病毒持续存在的总体能力影响较小。
这对猴痘控制的意义
研究结论是,疫苗接种在降低猴痘病例和住院人数方面可以发挥重要作用,尤其在覆盖率高且免疫得以维持时,但它并非一把万能钥匙。由于病毒可在动物中隐匿且存在后向分岔,微小的改进可能不足以消除风险:需要强有力且持续的努力。换言之,应把在高风险人群中广泛接种疫苗与减少密切接触传播的措施以及在可行时处理动物宿主的工作结合起来。该研究还表明,具有现实记忆特征的模型更能匹配真实病例数据,能够帮助卫生机构制定策略以防止猴痘重新出现,而不是仅仅应对下一次暴发。
引用: Khan, M.A., DarAssi, M.H., Tasqeeruddin, S. et al. A fractional-order vaccination model to analyze the dynamics of Mpox Clade I and II with real data. Sci Rep 16, 11093 (2026). https://doi.org/10.1038/s41598-026-41453-y
关键词: 猴痘, 疫苗接种, 数学建模, 人畜共患病, 分数阶微积分