Clear Sky Science · ru
Фракционная модель вакцинации для анализа динамики двух кладов осповидной инфекции (Mpox) с использованием реальных данных
Почему это важно для повседневного здравоохранения
Mpox, ранее редкий вирус, встречавшийся главным образом в отдельных регионах Африки, недавно вышел на первые полосы мировых новостей. Сейчас циркулируют два разных варианта — клады: один более тяжёлый, другой мягче, но широко распространён. В этом исследовании ставится практический вопрос с серьёзными последствиями для общественного здравоохранения: имея ограниченные запасы вакцин и сложные пути передачи между людьми и животными, можно ли с помощью математики понять, как распространяется mpox и может ли вакцинация в конечном счёте взять его под контроль?
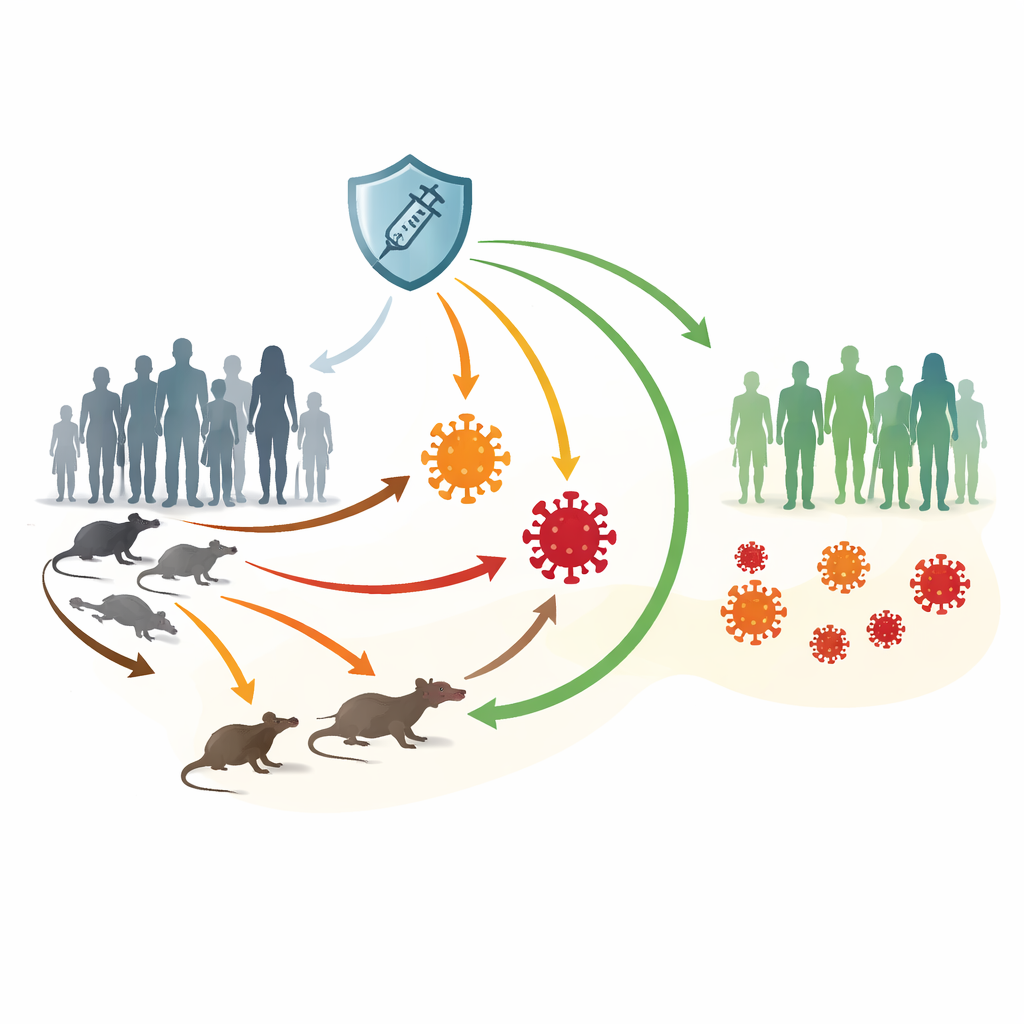
Два типа вируса и множество путей передачи
Авторы сосредотачиваются на Кладе I и Кладе II вируса mpox. Клад I, который всё ещё распространён в некоторых африканских странах, вызывает более тяжёлое заболевание и более высокую смертность. Клад II, ответственный за глобальную вспышку 2022 года, обычно протекает легче, но широко распространялся через тесный и интимный контакт, особенно в отдельных группах повышенного риска. Mpox может переходить от людей к грызунам и обратно и тихо циркулировать в популяциях животных, что затрудняет его ликвидацию. Вакцины, такие как JYNNEOS, обеспечивают сильную защиту, но их доступность неравномерна в разных странах, а иммунитет с течением времени может ослабевать.
Преобразование mpox в поток людей и животных
Чтобы распутать эту сложность, авторы строят компартментную модель, отслеживающую переходы индивидов между состояниями здоровья. Люди начинают как восприимчивые, могут получить вакцину, дающую временную, но сильную защиту, затем при контакте с инфекцией становятся экспонированными и дальше переходят в состояние болезни с Кладом I или Кладом II. Некоторые требуют госпитализации, тогда как другие выздоравливают напрямую. Параллельно грызуны разделены на здоровые и инфицированные группы. Стрелки в модели представляют все основные пути передачи: человек—человек, животное—человек, человек—животное и животное—животное. Эта схема позволяет команде проверять, как изменения в контактах, вакцинации и утрате иммунитета отражаются на динамике как человеческих, так и животных сообществ.
Добавление памяти в математику
Вместо использования только стандартных уравнений, предполагающих, что заражения и выздоровления происходят по простым, однородным расписаниям, авторы применяют подход фракционного порядка. Проще говоря, это добавляет встроенную «память» в модель: прошлые события продолжают постепенно влиять на текущее число инфекций. Это лучше отражает реальные вспышки, где инкубационные сроки, восстановление и поведение сильно варьируются между людьми. Команда сначала формулирует традиционную версию модели, затем расширяет её до фракционного формализма и доказывает, что её решения остаются биологически реалистичными (без отрицательных популяций и бесконтрольного взрыва в бесконечность) и математически корректными и уникальными.
Что модель говорит о распространении и контроле
Используя данные США по случаям Клада II с января по июль 2025 года, исследователи подгоняют свою модель и оценивают базовое репродукционное число — среднее число новых инфекций, вызываемых одним инфицированным человеком в полностью восприимчивой популяции. Они получают значение около 1.33, что означает, что каждое заболевание порождает более одного нового случая и вирус может сохраняться. Авторы также выводят «репродукционное число с учётом вакцинации», которое включает эффект иммунизации. Если это число опускается ниже единицы, теоретически состояние без инфекции становится устойчивым. Однако модель также выявляет явление, называемое обратным бифуркацией: даже если репродукционное число немного опустится ниже единицы, mpox может всё ещё сохраняться на низком, но стабильном уровне, особенно при наличии множества путей передачи и ослабления иммунитета.
Какие рычаги наиболее важны
Чтобы выяснить, какие факторы сильнее всего влияют на распространение, команда варьирует параметры, такие как частота контактов и смертность животных, в реалистичных пределах и измеряет реакцию репродукционного числа. В этом анализе частые контакты между инфицированными и восприимчивыми грызунами, а также между грызунами и людьми сильно увеличивают передачу, тогда как более быстрый естественный оборот в популяциях грызунов помогает её подавлять. Человеко-человеческие контакты в обоих кладах и контакты между инфицированными грызунами и людьми также играют значительную роль. Напротив, некоторые клинические детали, такие как точные показатели госпитализации и выздоровления, оказываются менее значимыми для общей способности вируса сохраняться.
Что это значит для контроля mpox
В исследовании делается вывод, что вакцинация может значительно сократить число случаев mpox и госпитализаций, особенно при высоком охвате и поддержании иммунитета, но она не является магическим выключателем. Поскольку вирус может скрываться в животных и из-за эффекта обратной бифуркации, небольших улучшений может быть недостаточно: нужны решительные и продолжительные усилия. В практических терминах это означает сочетание широкой вакцинации в группах повышенного риска с мерами, снижающими передачу при тесных контактах, и, там где возможно, управлением животными резервуарами. Работа также показывает, что реалистичные модели с учётом «памяти» лучше согласуются с реальными данными по случаям и могут помочь службам здравоохранения планировать стратегии, которые предотвращают повторное появление mpox, а не просто реагируют на следующую вспышку.
Цитирование: Khan, M.A., DarAssi, M.H., Tasqeeruddin, S. et al. A fractional-order vaccination model to analyze the dynamics of Mpox Clade I and II with real data. Sci Rep 16, 11093 (2026). https://doi.org/10.1038/s41598-026-41453-y
Ключевые слова: mpox, вакцинация, математическое моделирование, зоонозное заболевание, фракциональное исчисление