Clear Sky Science · fr
Un modèle de vaccination d’ordre fractionnaire pour analyser la dynamique des clades I et II du mpox avec des données réelles
Pourquoi cela compte pour la santé quotidienne
Le mpox, auparavant un virus rare surtout observé dans certaines régions d’Afrique, a récemment fait la une au niveau mondial. Deux formes distinctes, ou clades, circulent désormais : l’une plus sévère, l’autre plus bénigne mais répandue. Cette étude pose une question pratique aux grandes conséquences pour la santé publique : avec des vaccins limités et une transmission complexe entre humains et animaux, peut-on utiliser les mathématiques pour comprendre comment le mpox se propage et comment la vaccination pourrait enfin le contrôler ?
Deux types de virus et de nombreux modes de propagation
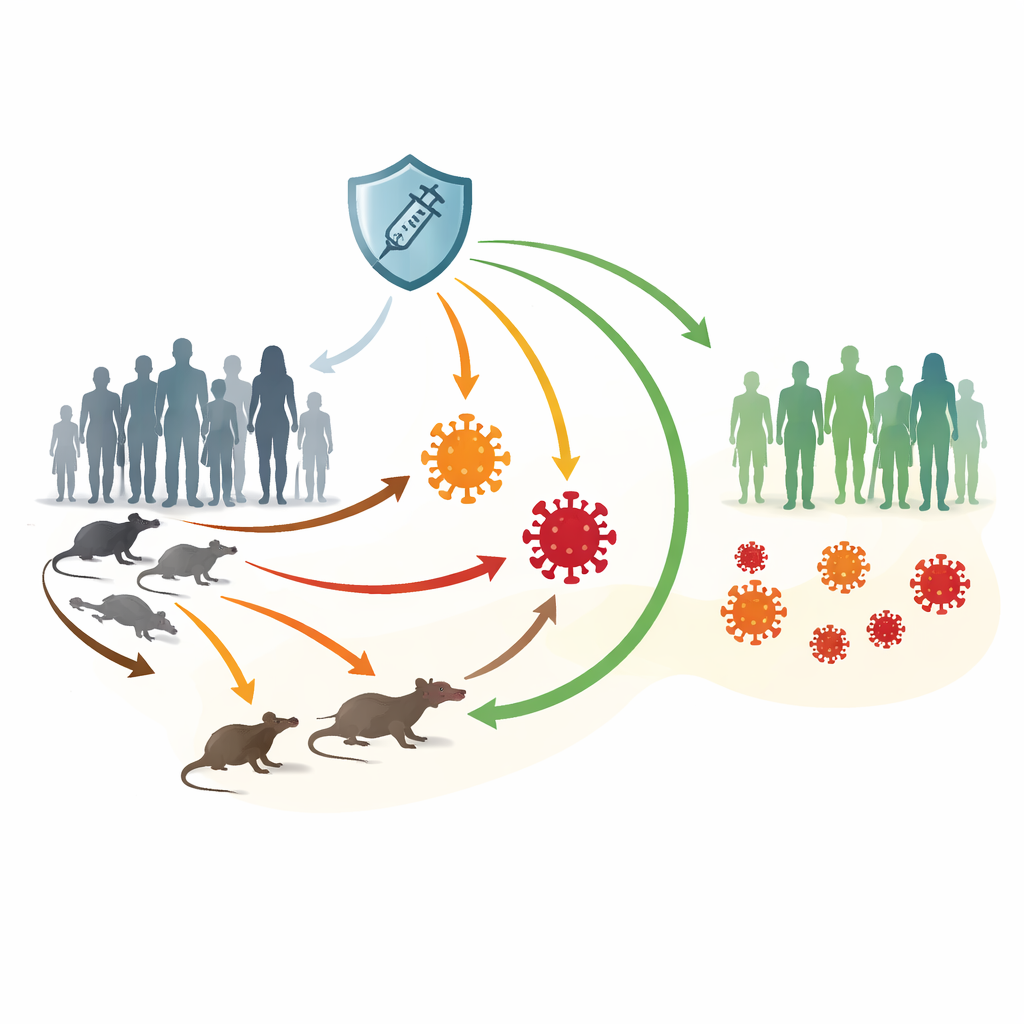
Les auteurs se concentrent sur les clades I et II du virus mpox. Le clade I, encore courant dans certains pays africains, provoque des formes plus graves et des taux de mortalité plus élevés. Le clade II, responsable de l’épidémie mondiale de 2022, est généralement plus léger mais s’est largement propagé par des contacts étroits et intimes, notamment au sein de certaines populations à risque. Le mpox peut passer entre humains et rongeurs et circuler discrètement dans les populations animales, ce qui complique son éradication. Des vaccins comme JYNNEOS offrent une forte protection, mais les approvisionnements sont inégaux dans le monde et l’immunité peut s’estomper avec le temps.
Transformer le mpox en flux d’humains et d’animaux
Pour démêler cette complexité, les chercheurs bâtissent un modèle compartimental qui suit les déplacements des individus entre états de santé. Les personnes commencent comme susceptibles, peuvent recevoir un vaccin qui offre une protection temporaire mais efficace, être exposées après un contact infectieux, puis évoluer vers une maladie due soit au clade I soit au clade II. Certaines nécessitent des soins hospitaliers, tandis que d’autres récupèrent directement. Parallèlement, les rongeurs sont divisés en groupes sains et infectés. Les flèches du modèle représentent tous les principaux chemins de transmission : humain→humain, animal→humain, humain→animal et animal→animal. Ce cadre permet à l’équipe de tester comment les changements de contacts, de vaccination et de perte d’immunité se propagent à la fois dans les communautés humaines et animales.
Ajouter de la mémoire aux équations
Plutôt que d’utiliser uniquement des équations classiques, qui supposent que les infections et les guérisons suivent des durées simples et uniformes, les auteurs adoptent une approche d’ordre fractionnaire. En termes simples, cela ajoute une « mémoire » intrinsèque au modèle : les événements passés continuent d’influencer les niveaux d’infection actuels de façon graduelle. Cela reflète mieux les épidémies réelles, où les temps d’incubation, les rétablissements et les comportements varient largement d’un individu à l’autre. L’équipe écrit d’abord une version traditionnelle du modèle, puis l’étend au cadre fractionnaire et démontre que ses solutions restent biologiquement réalistes (pas de populations négatives, pas d’explosions vers l’infini) et sont mathématiquement bien posées et uniques.
Ce que dit le modèle sur la propagation et le contrôle
En utilisant des données américaines sur les cas de clade II de janvier à juillet 2025, les chercheurs ajustent leur modèle et estiment le nombre reproductif de base — le nombre moyen de nouvelles infections causées par une personne infectée dans une population entièrement susceptible. Ils trouvent une valeur d’environ 1,33, ce qui signifie que chaque cas engendre plus d’un nouveau cas et que le virus peut persister. Ils dérivent également un « nombre reproductif vaccinal » qui prend en compte l’immunisation. Si cette valeur descend en dessous de un, l’état sans infection devient théoriquement stable. Cependant, le modèle révèle aussi un phénomène appelé bifurcation inverse : même si le nombre reproductif est légèrement inférieur à un, le mpox peut persister à des niveaux faibles mais stables, surtout lorsque coexistent plusieurs voies de transmission et un affaiblissement de l’immunité.
Quels leviers ont le plus d’impact
Pour savoir quels facteurs influencent le plus la propagation, l’équipe fait varier des paramètres tels que les taux de contact et la mortalité animale sur des plages réalistes et mesure la réaction du nombre reproductif. Dans cette analyse, des contacts fréquents entre rongeurs infectés et susceptibles, et entre rongeurs et humains, augmentent fortement la transmission, tandis qu’un renouvellement naturel plus rapide des populations de rongeurs contribue à la réduire. Les contacts humain→humain pour les deux clades, ainsi que les contacts entre rongeurs infectés et personnes, jouent aussi un rôle majeur. En revanche, certains détails cliniques, comme les taux exacts d’hospitalisation et de rétablissement, comptent moins pour la capacité globale du virus à persister.
Ce que cela signifie pour le contrôle du mpox
L’étude conclut que la vaccination peut réduire sensiblement les cas de mpox et les hospitalisations, en particulier lorsque la couverture est élevée et que l’immunité est entretenue, mais ce n’est pas un interrupteur magique. Parce que le virus peut se cacher chez les animaux et à cause de la bifurcation inverse, de petites améliorations peuvent ne pas suffire : des efforts forts et soutenus sont nécessaires. Concrètement, cela signifie combiner une vaccination étendue dans les groupes à haut risque avec des mesures qui réduisent la transmission par contacts rapprochés et, lorsque c’est possible, s’attaquer aux réservoirs animaux. Ce travail montre aussi que des modèles réalistes et sensibles à la mémoire peuvent mieux coller aux données réelles et aider les agences de santé à planifier des stratégies visant à empêcher la réémergence du mpox, plutôt que de simplement courir après la prochaine flambée.
Citation: Khan, M.A., DarAssi, M.H., Tasqeeruddin, S. et al. A fractional-order vaccination model to analyze the dynamics of Mpox Clade I and II with real data. Sci Rep 16, 11093 (2026). https://doi.org/10.1038/s41598-026-41453-y
Mots-clés: mpox, vaccination, modélisation mathématique, maladie zoonotique, calcul fractionnaire