Clear Sky Science · de
Ein Impfmodell mit fraktionalem Ordnungsglied zur Analyse der Dynamik von Mpox Klade I und II anhand realer Daten
Warum das für die Gesundheit im Alltag wichtig ist
Mpox, früher ein seltenes Virus, das überwiegend in Teilen Afrikas vorkam, hat kürzlich weltweit Schlagzeilen gemacht. Zwei unterschiedliche Formen, oder Kladen, zirkulieren nun: eine schwerere und eine mildere, aber weit verbreitete. Diese Studie stellt eine praktische Frage mit großen gesundheitspolitischen Folgen: Mit begrenzten Impfstoffen und komplexer Übertragung zwischen Menschen und Tieren — können wir die Verbreitung von Mpox durch Mathematik verstehen und einschätzen, ob Impfungen das Problem dauerhaft unter Kontrolle bringen können?
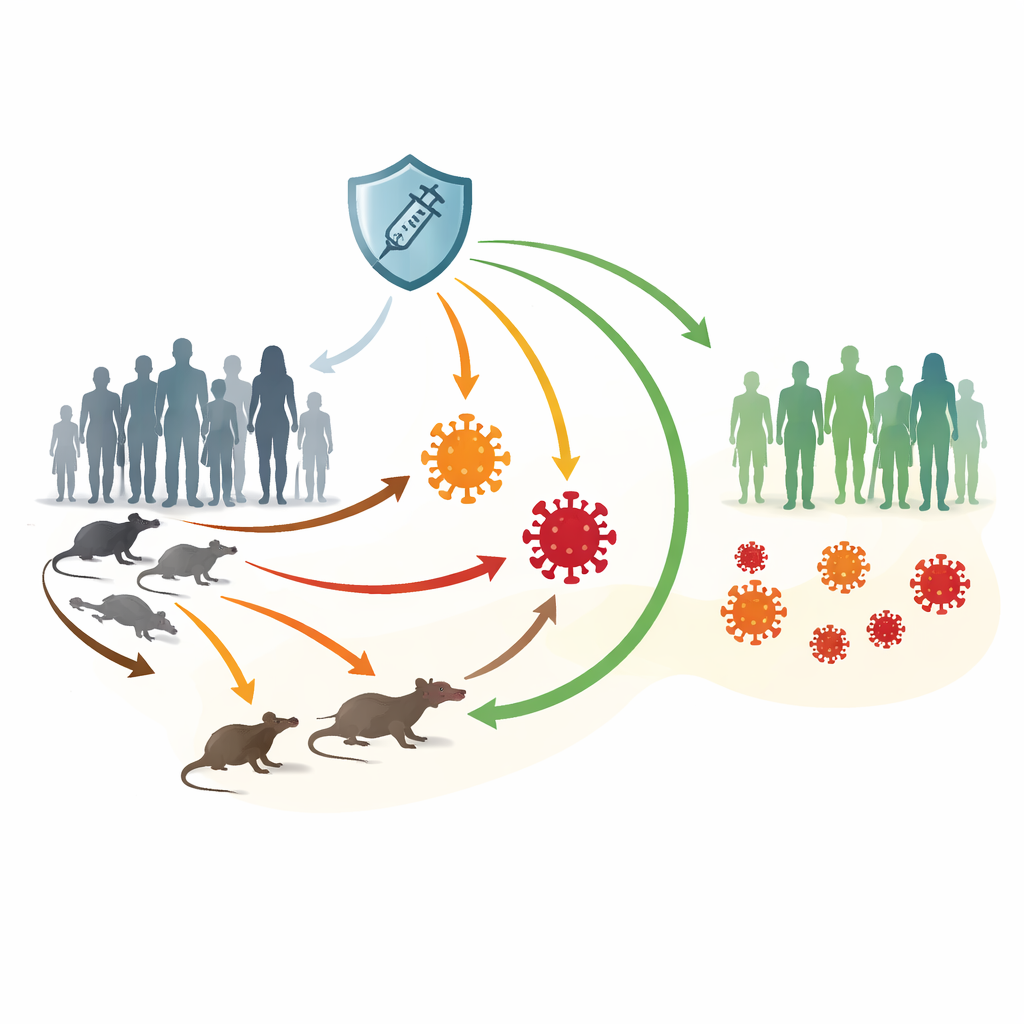
Zwei Virustypen und viele Übertragungswege
Die Forscher konzentrieren sich auf Klade I und Klade II des Mpox-Virus. Klade I, die in einigen afrikanischen Ländern weiterhin verbreitet ist, verursacht schwerere Erkrankungen und höhere Sterblichkeitsraten. Klade II, verantwortlich für den globalen Ausbruch 2022, verläuft meist milder, hat sich jedoch besonders durch engen, intimen Kontakt weit ausgebreitet, vor allem in bestimmten Risikogruppen. Mpox kann zwischen Menschen und Nagetieren springen und unauffällig in Tierpopulationen zirkulieren, was die Ausrottung erschwert. Impfstoffe wie JYNNEOS bieten starken Schutz, aber die Versorgung ist weltweit ungleich und die Immunität kann im Laufe der Zeit nachlassen.
Mpox als Fluss von Menschen und Tieren darstellen
Um diese Komplexität zu entwirren, entwickeln die Autorinnen und Autoren ein Kompartimentmodell, das verfolgt, wie Individuen zwischen Gesundheitszuständen wechseln. Menschen beginnen als empfänglich, können eine Impfung erhalten, die vorübergehend aber starken Schutz bietet, werden nach Kontakt exponiert und entwickeln dann eine Erkrankung mit entweder Klade I oder Klade II. Einige benötigen stationäre Versorgung, andere genesen direkt. Gleichzeitig werden Nagetiere in gesunde und infizierte Gruppen unterteilt. Pfeile im Modell stellen alle wichtigen Übertragungswege dar: Mensch-zu-Mensch, Tier-zu-Mensch, Mensch-zu-Tier und Tier-zu-Tier. Dieses Gerüst erlaubt dem Team, zu testen, wie Änderungen bei Kontakten, Impfungen und Immunitätsverlust sich in menschlichen und tierischen Gemeinschaften auswirken.
Erinnerung in die Mathematik einbauen
Anstatt nur Standardgleichungen zu verwenden, die annehmen, dass Infektionen und Genesungen einfachen, einheitlichen Zeitabläufen folgen, nutzen die Autoren einen fraktionalen Ansatz. Einfach gesagt fügt das Modell eine eingebaute „Erinnerung“ hinzu: Vergangene Ereignisse beeinflussen die aktuellen Infektionszahlen in gradueller Weise. Das spiegelt reale Ausbrüche besser wider, bei denen Inkubationszeiten, Genesungsverläufe und Verhalten stark zwischen Individuen variieren. Das Team formuliert zunächst eine traditionelle Version des Modells, erweitert es dann auf den fraktionalen Rahmen und beweist, dass die Lösungen biologisch realistisch bleiben (keine negativen Populationen, keine Explosionen gegen Unendlich) und mathematisch wohlverhalten und eindeutig sind.
Was das Modell über Ausbreitung und Kontrolle aussagt
Anhand von US-Daten zu Klade-II-Mpox-Fällen von Januar bis Juli 2025 passen die Forscher ihr Modell an und schätzen die grundlegende Reproduktionszahl — die durchschnittliche Anzahl neuer Infektionen, die eine infizierte Person in einer vollständig empfänglichen Population verursacht. Sie finden einen Wert von etwa 1,33, was bedeutet, dass jeder Fall mehr als einen neuen Fall erzeugt und das Virus persistieren kann. Zudem leiten sie eine „Impf-Reproduktionszahl“ ab, die Immunisierung berücksichtigt. Fällt dieser Wert unter eins, wird der infektionsfreie Zustand theoretisch stabil. Das Modell zeigt jedoch auch ein Phänomen namens rückwärtige Bifurkation: Selbst wenn die Reproduktionszahl leicht unter eins gedrückt wird, kann Mpox auf niedrigem, aber stabilem Niveau weiterbestehen — besonders wenn mehrere Übertragungswege und nachlassende Immunität vorhanden sind.
Welche Stellhebel am wichtigsten sind
Um zu sehen, welche Faktoren die Ausbreitung am stärksten beeinflussen, variiert das Team Parameter wie Kontakt- und Tiersterblichkeitsraten über realistische Bereiche und misst, wie die Reproduktionszahl reagiert. In dieser Analyse erhöht häufiger Kontakt zwischen infizierten und empfänglichen Nagetieren sowie zwischen Nagetieren und Menschen die Übertragung stark, während eine schnellere natürliche Erneuerung in Nagetierpopulationen sie dämpft. Mensch-zu-Mensch-Kontakte in beiden Kladen und Kontakte zwischen infizierten Nagetieren und Menschen spielen ebenfalls eine große Rolle. Dagegen sind einige klinische Details, wie genaue Hospitalisierungs- und Genesungsraten, weniger entscheidend für die allgemeine Fähigkeit des Virus zu persistieren.
Was das für die Mpox-Bekämpfung bedeutet
Die Studie kommt zu dem Schluss, dass Impfungen Mpox-Fälle und Hospitalisierungen erheblich reduzieren können, besonders bei hoher Abdeckung und langfristiger Aufrechterhaltung der Immunität, aber sie sind kein magischer Aus-Schalter. Weil das Virus in Tieren verbleiben kann und wegen der rückwärtigen Bifurkation reichen kleine Verbesserungen möglicherweise nicht aus: Starke, anhaltende Anstrengungen sind nötig. Konkret bedeutet das, breit angelegte Impfungen in Hochrisikogruppen mit Maßnahmen zu kombinieren, die Übertragungen durch engen Kontakt verringern, und nach Möglichkeit Tierreservoire anzugehen. Die Arbeit zeigt außerdem, dass realistische, erinnerungsfähige Modelle reale Falldaten besser abbilden und Gesundheitsbehörden helfen können, Strategien zu planen, die ein Wiederauftreten von Mpox verhindern, statt nur dem nächsten Ausbruch hinterherzujagen.
Zitation: Khan, M.A., DarAssi, M.H., Tasqeeruddin, S. et al. A fractional-order vaccination model to analyze the dynamics of Mpox Clade I and II with real data. Sci Rep 16, 11093 (2026). https://doi.org/10.1038/s41598-026-41453-y
Schlüsselwörter: mpox, Impfung, mathematische Modellierung, zoonotische Krankheit, fraktionale Analysis