Clear Sky Science · nl
Een vaccinatiemodel van fractieorde om de dynamiek van Mpox Clade I en II met echte gegevens te analyseren
Waarom dit van belang is voor de dagelijkse gezondheid
Mpox, ooit een zeldzaam virus dat vooral in delen van Afrika voorkwam, haalde recent wereldnieuws. Er circuleren nu twee onderscheiden vormen, of clades: één ernstiger en één mildere maar wijdverbreide. Deze studie stelt een praktische vraag met grote gevolgen voor de volksgezondheid: gegeven beperkte vaccins en complexe transmissie tussen mensen en dieren, kunnen we wiskunde gebruiken om te begrijpen hoe mpox zich verspreidt en of vaccinatie het uiteindelijk onder controle kan krijgen?
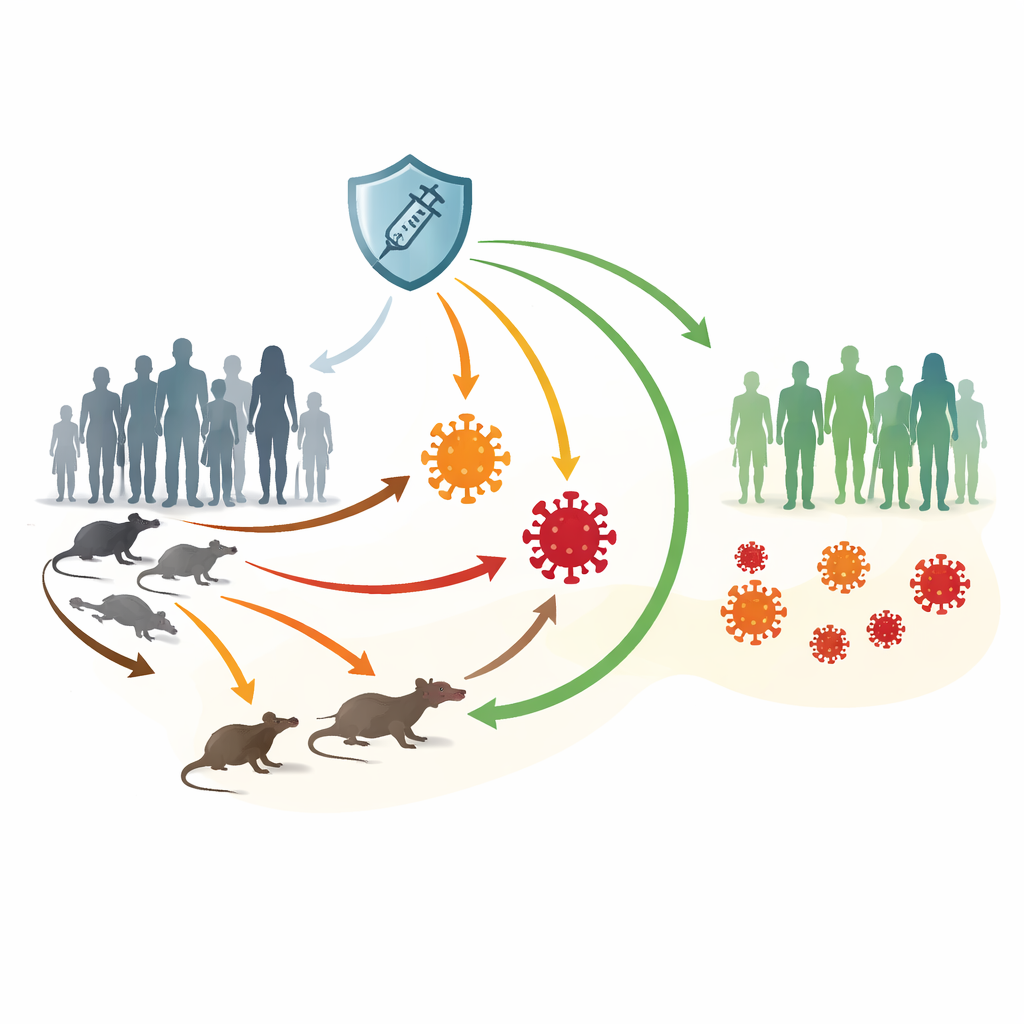
Twee typen virus en vele verspreidingspaden
De onderzoekers richten zich op Clade I en Clade II van het mpox‑virus. Clade I, nog steeds algemeen in sommige Afrikaanse landen, veroorzaakt ernstigere ziekte en hogere sterfte. Clade II, verantwoordelijk voor de wereldwijde uitbraak van 2022, is meestal milder maar heeft zich wijd verspreid via nauw en intiem contact, vooral binnen bepaalde risicogroepen. Mpox kan overspringen tussen mensen en knaagdieren en stilletjes circuleren in dierpopulaties, wat uitroeiing bemoeilijkt. Vaccins zoals JYNNEOS bieden sterke bescherming, maar de voorraden zijn ongelijk verdeeld en de immuniteit kan na verloop van tijd afnemen.
Mpvx omzetten in stromen van mensen en dieren
Om deze complexiteit te ontwarren bouwen de auteurs een compartimentsmodel dat volgt hoe individuen tussen gezondheidstoestanden bewegen. Mensen beginnen als vatbaar, kunnen een vaccin krijgen dat tijdelijke maar sterke bescherming biedt, worden na contact met een infectie blootgesteld en ontwikkelen vervolgens ziekte met ofwel Clade I of Clade II. Sommigen hebben ziekenhuiszorg nodig, anderen herstellen direct. Tegelijkertijd worden knaagdieren verdeeld in gezonde en geïnfecteerde groepen. Pijlen in het model geven alle belangrijke verspreidingsroutes aan: mens‑naar‑mens, dier‑naar‑mens, mens‑naar‑dier en dier‑naar‑dier. Dit raamwerk stelt het team in staat te testen hoe veranderingen in contactpatronen, vaccinatie en verlies van immuniteit doorwerken in zowel menselijke als dierlijke gemeenschappen.
Geheugen toevoegen aan de wiskunde
In plaats van alleen standaardvergelijkingen te gebruiken, die veronderstellen dat infecties en herstel eenvoudige, uniforme tijdlijnen volgen, gebruiken de auteurs een aanpak met fractieorde. Simpel gezegd voegt dit een ingebouwd “geheugen” aan het model toe: gebeurtenissen uit het verleden blijven op een geleidelijke manier invloed uitoefenen op het huidige infectieniveau. Dat weerspiegelt uitbraken beter, waar incubatietijden, herstel en gedrag sterk kunnen variëren tussen individuen. Het team schrijft eerst een traditionele versie van het model en breidt die vervolgens uit naar het fractieorde‑kader, waarbij ze aantonen dat de oplossingen biologisch realistisch blijven (geen negatieve populaties, geen oncontroleerbare explosies naar oneindig) en wiskundig goedgedrag en uniekheid bezitten.
Wat het model zegt over verspreiding en beheersing
Met behulp van Amerikaanse gegevens over Clade II‑mpoxgevallen van januari tot juli 2025 passen de onderzoekers hun model aan en schatten ze het basisreproductiegetal — het gemiddelde aantal nieuwe infecties veroorzaakt door één geïnfecteerde persoon in een geheel vatbare bevolking. Ze vinden een waarde van ongeveer 1,33, wat betekent dat elk geval meer dan één nieuw geval voortbrengt en het virus kan blijven bestaan. Ze leiden ook een “vaccinatie‑reproductiegetal” af dat rekening houdt met immunisatie. Als deze waarde onder één zakt, wordt de infectievrije toestand theoretisch stabiel. Het model onthult echter ook een verschijnsel dat achterwaartse bifurcatie wordt genoemd: zelfs als het reproductiegetal iets onder één wordt gedrukt, kan mpox toch op lage maar stabiele niveaus blijven bestaan, vooral wanneer meerdere transmissieroutes en afnemende immuniteit aanwezig zijn.
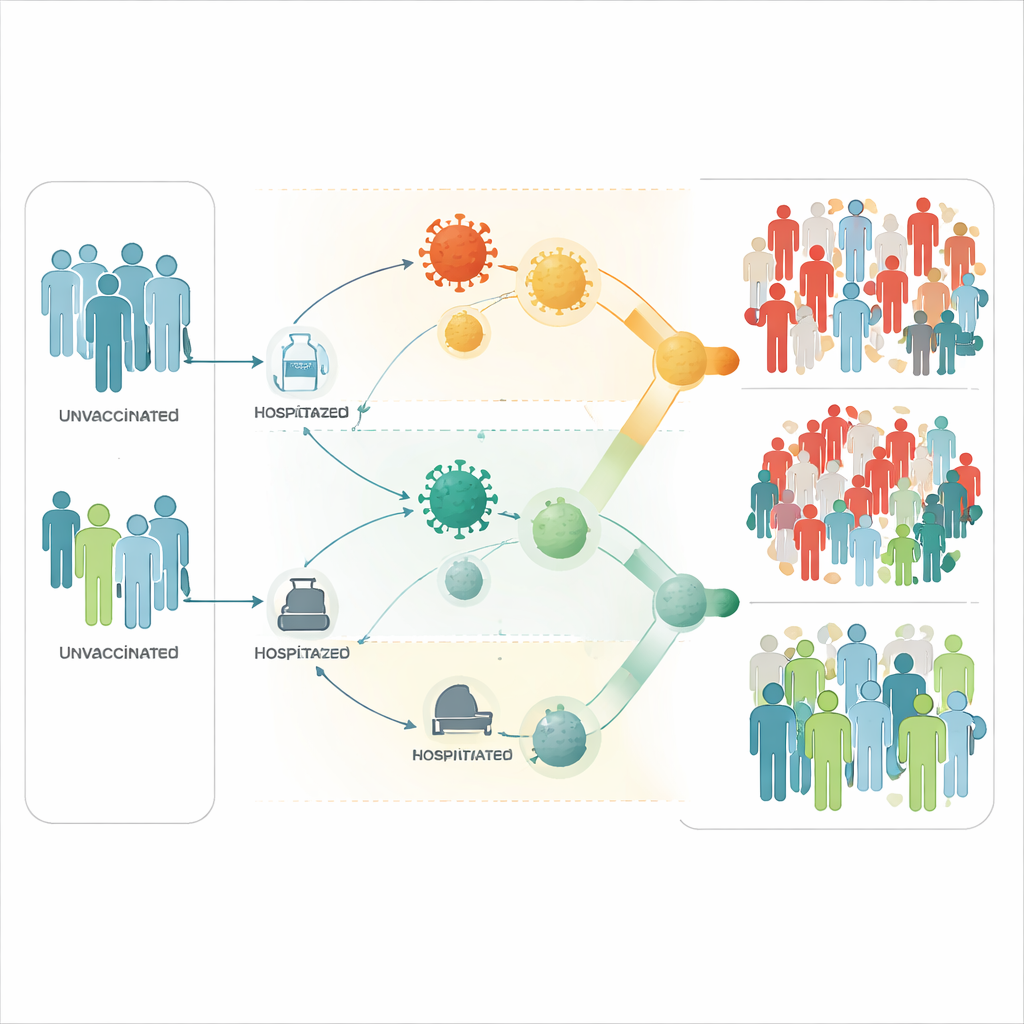
Welke hefbomen het meest tellen
Om te zien welke factoren de verspreiding het sterkst beïnvloeden, varieert het team parameters zoals contactfrequenties en sterftecijfers van dieren over realistische bereiken en meet hoe het reproductiegetal reageert. In deze analyse vergroot frequent contact tussen geïnfecteerde en vatbare knaagdieren, en tussen knaagdieren en mensen, de transmissie sterk, terwijl een snellere natuurlijke omloopsnelheid in knaagdierpopulaties helpt deze te onderdrukken. Mens‑naar‑menscontact bij beide clades, en contacten tussen geïnfecteerde knaagdieren en mensen, spelen ook een belangrijke rol. Daarentegen zijn sommige klinische details, zoals exacte ziekenhuisopnames en herstelpercentages, minder bepalend voor het algemene vermogen van het virus om te blijven bestaan.
Wat dit betekent voor mpox‑bestrijding
De studie concludeert dat vaccinatie het aantal mpox‑gevallen en ziekenhuisopnames aanzienlijk kan verminderen, vooral wanneer de dekking hoog is en de immuniteit behouden blijft, maar dat het geen magische uitknop is. Omdat het virus zich in dieren kan verbergen en vanwege achterwaartse bifurcatie, zijn kleine verbeteringen mogelijk niet voldoende: sterke, aanhoudende inspanningen zijn nodig. In de praktijk betekent dat het combineren van brede vaccinatie binnen risicogroepen met maatregelen die overdracht door nauw contact verminderen en, waar mogelijk, aanpak van dierlijke reservoirs. Het werk toont ook aan dat realistische, geheugenbewuste modellen beter bij echte casusdata kunnen passen en gezondheidsinstanties kunnen helpen strategieën te plannen die mpox doen terugdringen in plaats van steeds de volgende uitbraak na te jagen.
Bronvermelding: Khan, M.A., DarAssi, M.H., Tasqeeruddin, S. et al. A fractional-order vaccination model to analyze the dynamics of Mpox Clade I and II with real data. Sci Rep 16, 11093 (2026). https://doi.org/10.1038/s41598-026-41453-y
Trefwoorden: mpox, vaccinatie, wiskundige modellering, zoönose, fractale calculus