Clear Sky Science · zh
结直肠癌中B细胞向IgD⁻CD27⁻IgG⁺亚群的免疫表型倾斜及代谢减弱
为何机体自有防御在结肠癌中会失灵
结直肠癌不仅仅是失控细胞的堆积;它是一个复杂的群落,肿瘤细胞与免疫细胞持续相互作用。B细胞是这些免疫细胞的一类,更常因产生抗体并帮助抵抗感染而为人所知。本研究探讨了B细胞进入结肠肿瘤环境后会发生什么,揭示其中许多B细胞在功能和能量方面都被削弱。理解免疫反应这一被掩盖的面向,最终可能帮助医生设计出能将这些细胞重新激活以对抗癌症的疗法。
揭示肿瘤内一种异常的B细胞转变
研究者首先将来自同一患者的结直肠癌组织中的B细胞与邻近正常肠道组织中的B细胞进行了比较。在健康的肠道组织中,大多数B细胞处于活跃的、产生抗体的阶段。然而在肿瘤内部,呈现出截然不同的格局:一种被称为“双阴性”B细胞(缺失两种典型表面标志)的异常亚型成为占优势的群体。此类细胞在慢性感染和某些自身免疫病中会扩增,通常表现出疲惫或衰竭的特征。在肿瘤样本中,这些双阴性B细胞也表现出与健康功能相关的表面蛋白表达降低,进一步支持它们处于功能衰竭状态的观点。
从保护性抗体到另一种反应
在健康肠道中,B细胞通常产生IgA抗体,帮助保护肠道黏膜并与常驻微生物保持平衡。而在肿瘤环境中,作者发现主导的B细胞亚群从IgA转向IgG抗体。这种抗体构成的改变表明局部环境将B细胞从其正常的屏障保护角色推向更与炎症相关的反应。然而,当研究团队用通常促使B细胞成为成熟的抗体分泌细胞的刺激信号刺激取自肿瘤的B细胞时,这些细胞的反应明显不如来自健康组织的B细胞。综合这些观察结果,显示结直肠肿瘤中存在相当数量的B细胞被重新定向并在一定程度上被失能。
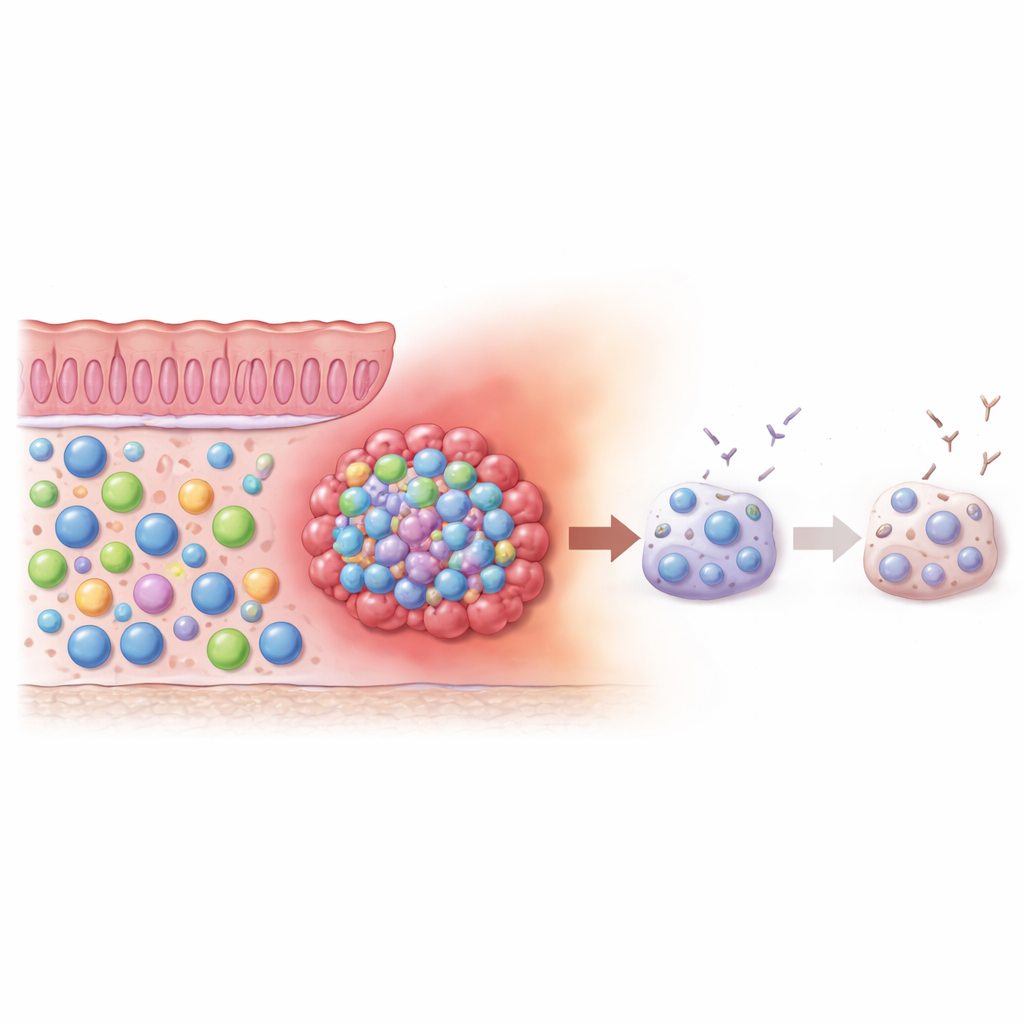
沉寂的引擎:肿瘤中的低活性B细胞
由于细胞行为与细胞如何利用能量密切相关,研究者接着检查了肿瘤内B细胞的代谢。他们测量了蛋白质合成和线粒体活性,这些是细胞“被激活”程度的常见指标。令人意外的是,肿瘤中的双阴性B细胞在代谢上显得安静,更像处于休眠状态的B细胞而非高度活跃的防御细胞。这种低速状态为它们难以成熟为强效抗体分泌细胞提供了合理解释。它们内部的“引擎”似乎被调低,提示肿瘤环境可能将其推向一种迟缓且效果较差的状态。
肿瘤迷你器官如何重塑B细胞的燃料利用
为探究肿瘤组织如何产生这种效应,团队采用了小鼠模型。他们从正常肠道和化学诱导的结肠肿瘤中培养出三维“类器官”,然后将这些结构与健康小鼠B细胞共同培养。暴露于肿瘤类器官的B细胞分裂减少,产生的抗体分泌细胞也比单独培养或与健康类器官共培养的更少。当研究者描绘关键代谢通路时,发现接近肿瘤类器官的B细胞逐渐失去高效摄取葡萄糖的能力,并表现出糖酵解降低——这种快速燃烧糖类的途径常常为免疫反应提供能量。与此同时,这些细胞对线粒体的依赖增加,但其线粒体功能随时间下降,表现为膜电位降低、耗氧量减少以及产生能量的能力下降。
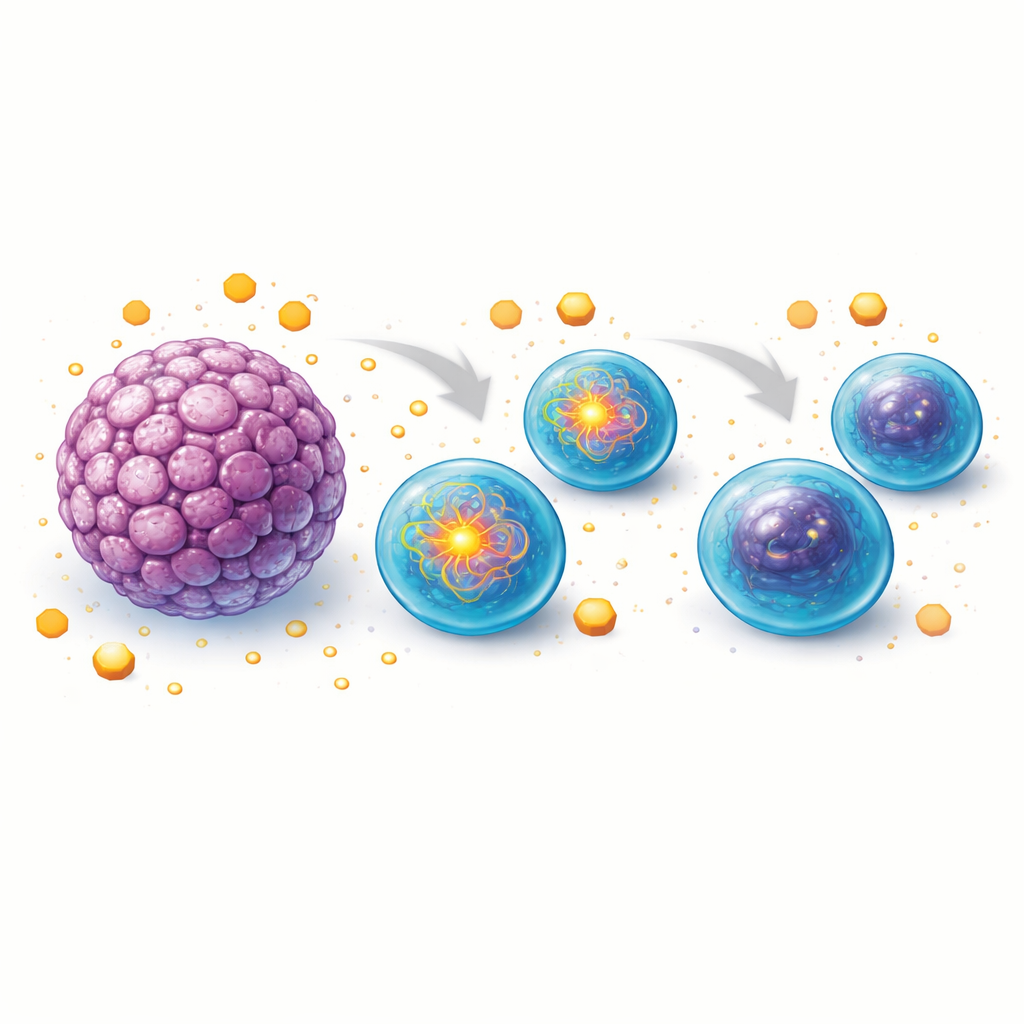
断裂的燃料线路与疲惫的免疫战士
进一步分析显示,与肿瘤类器官共培养的B细胞对脂肪酸的摄取也减少,且产生用于利用脂肪作为燃料的酶的水平更低。这意味着两个主要能量来源——糖类与脂肪——都受到了损害。因此,尽管B细胞对线粒体的依赖性增加,但它们缺乏维持线粒体高效能量生产所需的燃料与功能组件。由此呈现的图景是:B细胞在肿瘤环境中最初试图提高活性,却在营养竞争和肿瘤来源因子逐步侵蚀其代谢能力时陷入停滞。
这对未来癌症治疗意味着什么
简而言之,本研究显示结直肠肿瘤中的许多B细胞被逼入一种耗竭、低能量的状态。它们改变了偏好的抗体类型,丧失了完全成熟的能力,并被肿瘤环境逐步破坏其燃料系统。对非专业读者而言,关键结论是:癌症不仅通过直接抑制来削弱免疫系统,还可通过切断或误导其能量供应来使其失能。通过描绘这些变化,这项工作为可能恢复或重编程B细胞代谢的治疗策略打开了大门,目标是将这些疲惫的细胞重新变为对抗结直肠癌的活跃盟友。
引用: Martinis, E., Tonon, S., Valeri, V. et al. Immunophenotypic skewing of B cells toward IgD⁻CD27⁻IgG⁺ subtype and metabolic attenuation in colorectal cancer. Sci Rep 16, 11403 (2026). https://doi.org/10.1038/s41598-026-41446-x
关键词: 结直肠癌, B细胞, 肿瘤微环境, 免疫代谢, 癌症免疫治疗