Clear Sky Science · ar
انحراف النمط الظاهري للخلايا البائية نحو النمط الفرعي IgD⁻CD27⁻IgG⁺ وتراجع التمثيل الغذائي في سرطان القولون والمستقيم
لماذا قد تفشل دفاعات الجسم نفسها في سرطان القولون
سرطان القولون والمستقيم ليس مجرد كتلة من الخلايا المنحرفة؛ بل هو مجتمع معقد تتفاعل فيه خلايا الورم والخلايا المناعية باستمرار. من بين هذه الخلايا المناعية توجد الخلايا البائية، المعروفة بدورها في تكوين الأجسام المضادة ومساعدتنا في مقاومة العدوى. تستكشف هذه الدراسة ما يحدث للخلايا البائية عندما تدخل بيئة الورم في القولون، كاشفة أن العديد منها يصبح مثقلاً وظيفياً وطاقوياً. قد تساعد معرفة هذا الجانب الخفي للاستجابة المناعية الأطباء لاحقاً على تصميم علاجات تُعيد هذه الخلايا إلى ساحة المعركة ضد السرطان.
كشف تحول غير مألوف للخلايا البائية داخل الأورام
بدأ الباحثون بمقارنة الخلايا البائية الموجودة في أنسجة سرطان القولون والمستقيم مع تلك الموجودة في الأمعاء الطبيعية المجاورة من نفس المرضى. في نسيج الأمعاء السليم، كانت غالبية الخلايا البائية في مراحل نشطة وتنتج الأجسام المضادة. داخل الأورام، ظهرت صورة مختلفة جداً: أصبح نمط فرعي غير اعتيادي يُسمى الخلايا البائية "سلبية الزوج" (تفتقر إلى علامتين سطحتين نمطيتين) المجموعة المهيمنة. هذه الخلايا، النادرة عادة، تُعرف بتوسعها خلال العدوى المزمنة وبعض الأمراض المناعية الذاتية، حيث تظهر غالباً علامات الإرهاق أو الاستنفاد. في عينات الأورام، أظهرت هذه الخلايا السلبية الزوج مستويات منخفضة من بروتين سطحي مرتبط بالوظيفة السليمة، مما يعزز فكرة أنها في حالة متعبة.
من الأجسام المضادة الواقية إلى استجابة مغايرة
في الأمعاء السليمة، تنتج الخلايا البائية عادة أجساماً مناعية من نوع IgA التي تحمي بطانة القناة الهضمية وتحافظ على التوازن مع الميكروبيوتا المقيمة. في بيئة الورم، وجد المؤلفون أن الأنماط الفرعية السائدة للخلايا البائية انحرفت بعيداً عن IgA ونحو الأجسام المضادة من نوع IgG. يشير هذا التغير في توازن الأجسام المضادة إلى أن البيئة المحلية تدفع الخلايا البائية بعيداً عن دورها الطبيعي في حماية الحاجز ونحو استجابة مرتبطة بالالتهاب. ومع ذلك، عندما حفّز الفريق الخلايا البائية المأخوذة من الورم بإشارات تدفعها عادةً لتصبح مصانع للأجسام المضادة، استجابت هذه الخلايا بشكل ضعيف مقارنة بالخلايا البائية من النسيج السليم. تشير هذه الملاحظات مجتمعة إلى وجود تجمع كبير من الخلايا البائية في أورام القولون والمستقيم قد تم توجيهه ثم تعطيله جزئياً.
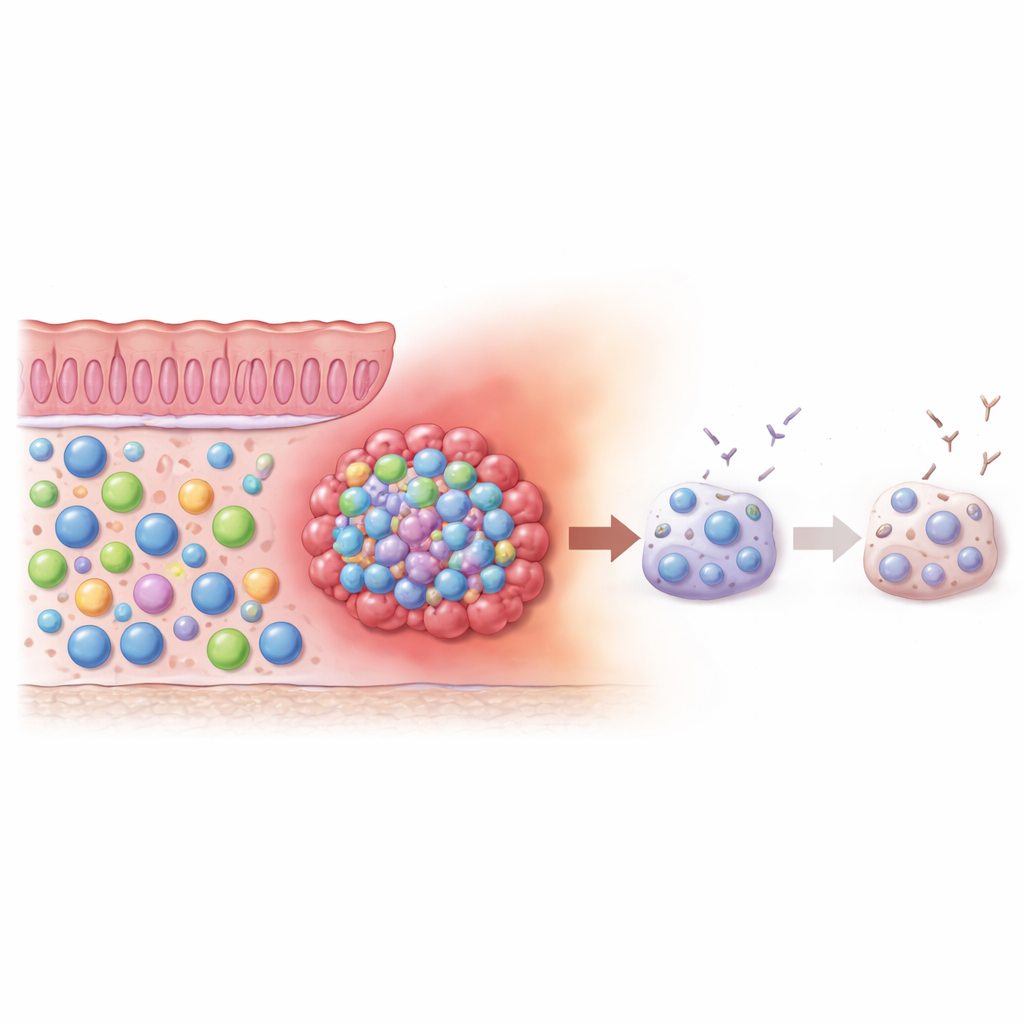
محركات صامتة: الخلايا البائية منخفضة النشاط داخل الورم
بما أن سلوك الخلايا مرتبط ارتباطاً وثيقاً بكيفية استخدامها للطاقة، فحص الباحثون بعد ذلك تمثيل الخلايا البائية داخل الأورام. قاسوا تخليق البروتين ونشاط الميتوكوندريا، وهي مقاييس شائعة لمدى "تنشيط" الخلية. بشكل مفاجئ، بدت الخلايا البائية السلبية الزوج داخل الأورام خاملة تمثيلياً، أشبه بالخلايا البائية القاعدة بدلاً من المدافعين النشطين. يقدم هذا النمط منخفض النشاط تفسيراً معقولاً لسبب صعوبة نضوجها إلى خلايا مُفرزة للأجسام المضادة بقوة. بدلاً من تغذية هجوم مناعي قوي، تبدو محركاتها الداخلية مضبوطة على وضع منخفض، مما يوحي بأن بيئة الورم قد تدفعها إلى حالة بطء وأقل فعالية.
كيف تعيد "عضويات" الورم الصغيرة توصيل وقود الخلايا البائية
لاستقصاء كيف تُحدث أنسجة الورم هذا التأثير، لجأ الفريق إلى نماذج فأرية. نما الباحثون "أورجنيدات" ثلاثية الأبعاد من الأمعاء الطبيعية ومن أورام القولون المحفزة كيميائياً، ثم شاركوا هذه البُنى مع خلايا بائية فأرية صحية في ثقافة مشتركة. انقسمت الخلايا البائية المعرضة لأورجنيدات الورم أقل وأنتجت خلايا مُفرزة للأجسام المضادة أقل من تلك المزروعة وحدها أو مع أورجنيدات سليمة. عندما حلل الباحثون المسارات الأيضية الرئيسية، وجدوا أن الخلايا البائية بجوار أورجنيدات الورم فقدت تدريجياً قدرتها على امتصاص الجلوكوز بكفاءة وأظهرت تراجعاً في التحلل السكري (glycolysis)، وهو المسار السريع لحرق السكر الذي يغذي غالباً الاستجابات المناعية. وفي الوقت نفسه، أصبحت هذه الخلايا أكثر اعتماداً على الميتوكوندريا، إلا أن آلية الميتوكوندريا نفسها انخفضت مع الزمن، مع هبوط في الجهد الغشائي، وانخفاض استهلاك الأكسجين، وتراجع في قدرة إنتاج الطاقة.
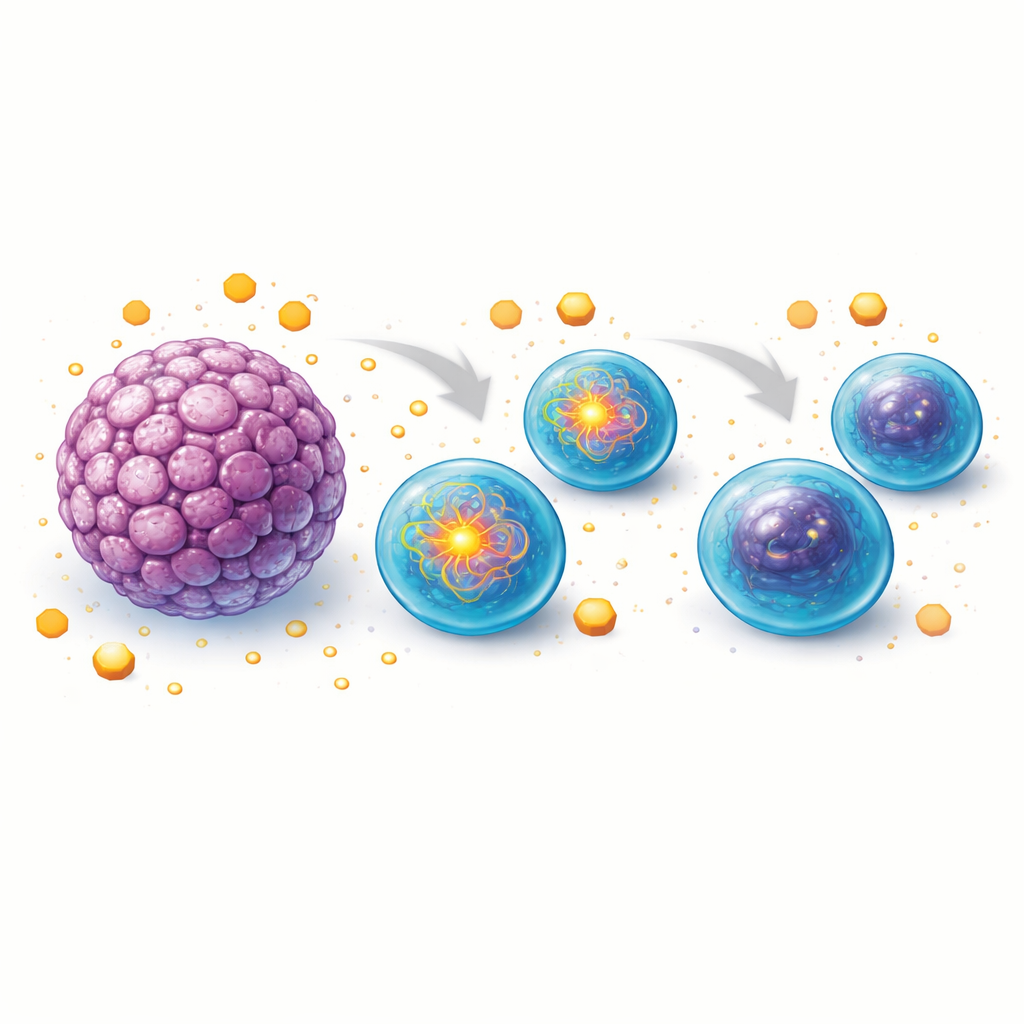
خطوط وقود مكسورة وجنود مناعيون متعبون
أظهر تحليل إضافي أن الخلايا البائية المشتركة مع أورجنيدات الورم امتصت أيضاً أحماضاً دهنية أقل وأنتجت مستويات أدنى من الإنزيمات اللازمة لاستخدام الدهون كوقود. يعني هذا أن مصدري طاقة رئيسيين — السكريات والدهون — تعرضا للتعطيل معاً. نتيجة لذلك، بينما بدا أن الخلايا البائية أصبحت أكثر اعتماداً على الميتوكوندريا، إلا أنها افتقرت إلى الوقود والمكونات الوظيفية اللازمة للحفاظ على إنتاج طاقة ميكروكوندري عالي السرعة. الصورة الناشئة هي لخلايا بائية تحاول في البداية زيادة نشاطها في بيئة الورم، لكنها تتعثر مع تزايد المنافسة على المغذيات وعوامل مشتقة من الورم تقوّض قدرتها الأيضية.
ماذا يعني هذا للعلاجات المستقبلية للسرطان
ببساطة، تُظهر هذه الدراسة أن العديد من الخلايا البائية داخل أورام القولون والمستقيم تُدفع إلى وضع مستنفد ومنخفض الطاقة. تغير أنواع الأجسام المضادة التي تفضلها، وتفقد قدرتها على النضوج الكامل، ويتعرض نظام وقودها للتخريب التدريجي بواسطة محيط الورم. بالنسبة لغير المتخصصين، الخلاصة الأساسية هي أن السرطان يمكن أن يعطل أجزاء من الجهاز المناعي ليس فقط من خلال القمع المباشر، بل أيضاً عن طريق قطع أو تحويل إمدادات الطاقة الخاصة بهم. من خلال رسم خريطة هذه التغيرات، تفتح هذه الأعمال الباب أمام علاجات محتملة تستعيد أو تعيد توصيل تمثيل الخلايا البائية، بهدف تحويل هذه الخلايا المتعبة مرة أخرى إلى حلفاء نشطين في معركة الجسم ضد سرطان القولون والمستقيم.
الاستشهاد: Martinis, E., Tonon, S., Valeri, V. et al. Immunophenotypic skewing of B cells toward IgD⁻CD27⁻IgG⁺ subtype and metabolic attenuation in colorectal cancer. Sci Rep 16, 11403 (2026). https://doi.org/10.1038/s41598-026-41446-x
الكلمات المفتاحية: سرطان القولون والمستقيم, الخلايا البائية, البيئة المجهرية للورم, تمثيل غذائي مناعي, مناعة السرطان العلاجية