Clear Sky Science · es
Sesgo inmunofenotípico de los linfocitos B hacia el subtipo IgD⁻CD27⁻IgG⁺ y atenuación metabólica en el cáncer colorrectal
Por qué los propios defensores del cuerpo pueden fallar en el cáncer de colon
El cáncer colorrectal no es solo una masa de células descontroladas; es una comunidad compleja donde las células tumorales y las inmunitarias interactúan constantemente. Entre estas células inmunitarias están los linfocitos B, más conocidos por producir anticuerpos y ayudarnos a combatir infecciones. Este estudio explora qué les ocurre a los linfocitos B cuando entran en el microambiente de un tumor de colon, revelando que muchos de ellos se vuelven tanto funcional como energéticamente debilitados. Comprender este lado oculto de la respuesta inmune podría, con el tiempo, ayudar a los médicos a diseñar tratamientos que reactivasen a estas células para que vuelvan a combatir el cáncer.
Descubriendo un extraño cambio de linfocitos B dentro de los tumores
Los investigadores empezaron comparando los linfocitos B encontrados en tejido de cáncer colorrectal con los del intestino normal adyacente de los mismos pacientes. En el tejido intestinal sano, la mayoría de los linfocitos B estaban en etapas activas productoras de anticuerpos. Dentro de los tumores, sin embargo, emergió un patrón muy distinto: un subtipo inusual llamado linfocitos B “doble negativos” (que carecen de dos marcadores de superficie típicos) se convirtió en el grupo dominante. Normalmente raros, se sabe que estos linfocitos se expanden durante infecciones crónicas y en algunas enfermedades autoinmunes, donde con frecuencia muestran signos de estar agotados. En las muestras tumorales, estos linfocitos B doble negativos también mostraron niveles bajos de una proteína de superficie asociada a la función saludable, reforzando la idea de que estaban en un estado fatigado.
De anticuerpos protectores a una respuesta distinta
En el intestino sano, los linfocitos B suelen producir anticuerpos IgA, que ayudan a proteger la mucosa intestinal y a mantener la convivencia con la microbiota residente. En el contexto tumoral, los autores encontraron que los subgrupos dominantes de linfocitos B cambiaron alejándose de IgA y hacia anticuerpos IgG. Este desequilibrio de anticuerpos sugiere que el entorno local impulsa a los linfocitos B a abandonar su papel protector de barrera y a inclinarse hacia una respuesta más vinculada con la inflamación. Aun así, cuando el equipo estimuló linfocitos B extraídos del tumor con señales que normalmente los convierten en fábricas plenas de anticuerpos, estas células respondieron de forma pobre en comparación con los linfocitos B del tejido sano. En conjunto, estas observaciones apuntan a una reserva considerable de linfocitos B en los tumores colorrectales que han sido redirigidos y luego en parte desactivados.
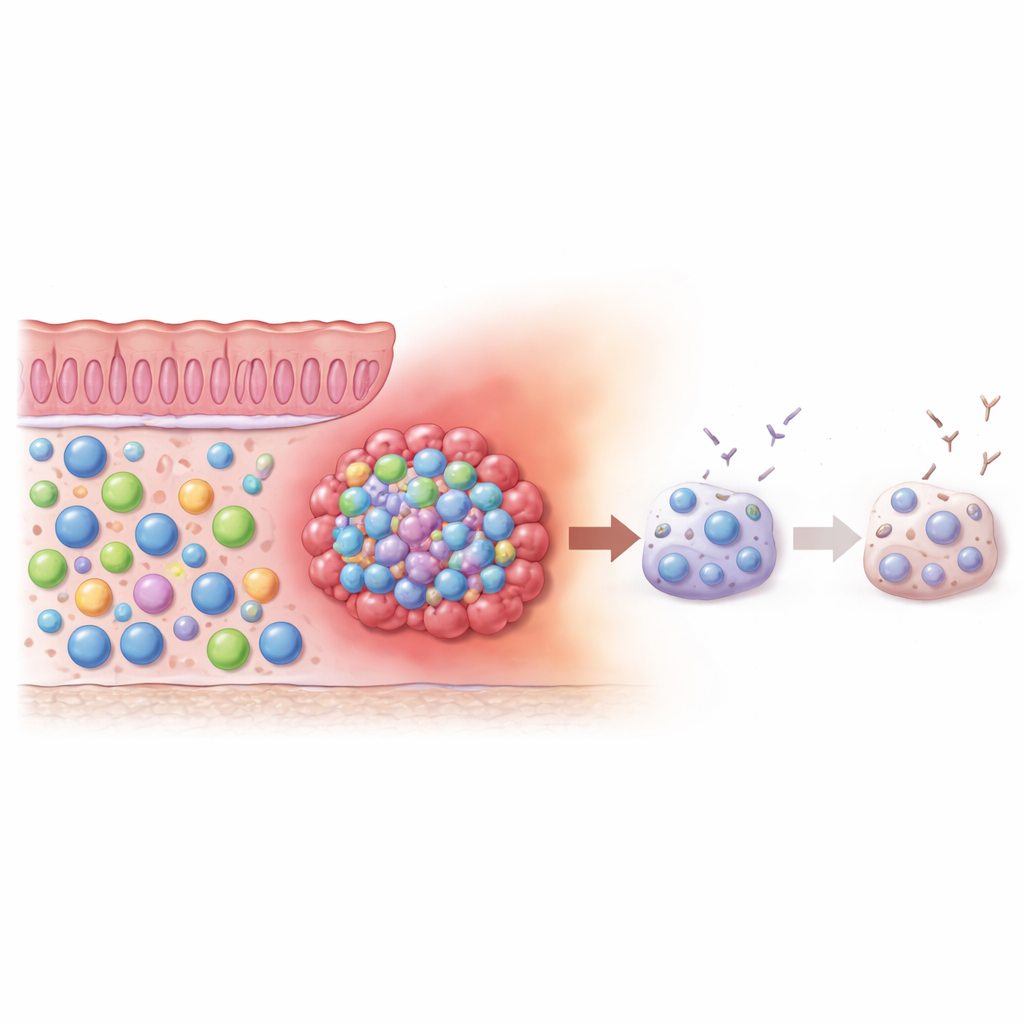
Motores silenciosos: linfocitos B de baja actividad en el tumor
Dado que el comportamiento celular está estrechamente ligado a cómo las células usan la energía, los investigadores examinaron a continuación el metabolismo de los linfocitos B dentro de los tumores. Midieron la síntesis de proteínas y la actividad mitocondrial, lecturas habituales de cuán “activada” está una célula. Sorprendentemente, los linfocitos B doble negativos en los tumores mostraron un perfil metabólico tranquilo, semejante al de linfocitos B en reposo más que al de defensores altamente activos. Este perfil de baja marcha ofrece una explicación plausible de por qué les cuesta madurar en células secretoras de anticuerpos robustas. En lugar de impulsar un ataque inmune vigoroso, sus motores internos parecen estar ajustados a la baja, lo que sugiere que el entorno tumoral podría estar empujándolos a un estado lento y menos eficaz.
Cómo los mini-órganos tumorales reprograman el uso de combustible de los linfocitos B
Para investigar cómo el tejido tumoral crea este efecto, el equipo recurrió a modelos de ratón. Cultivaron “organoides” tridimensionales a partir de intestino normal y de tumores de colon inducidos químicamente, y luego co-cultivaron estas estructuras con linfocitos B sanos de ratón. Los linfocitos B expuestos a organoides tumorales se dividieron menos y produjeron menos células secretoras de anticuerpos que los cultivados solos o con organoides sanos. Cuando los investigadores perfilaban vías metabólicas clave, hallaron que los linfocitos B próximos a los organoides tumorales perdían gradualmente su capacidad de captar glucosa de manera eficiente y mostraban una reducción de la glucólisis, la vía rápida de quema de azúcares que a menudo impulsa las respuestas inmunes. Al mismo tiempo, las células se volvieron más dependientes de sus mitocondrias, pero la maquinaria mitocondrial declinó con el tiempo, con menor potencial de membrana, consumo de oxígeno reducido y disminución de la capacidad para producir energía.
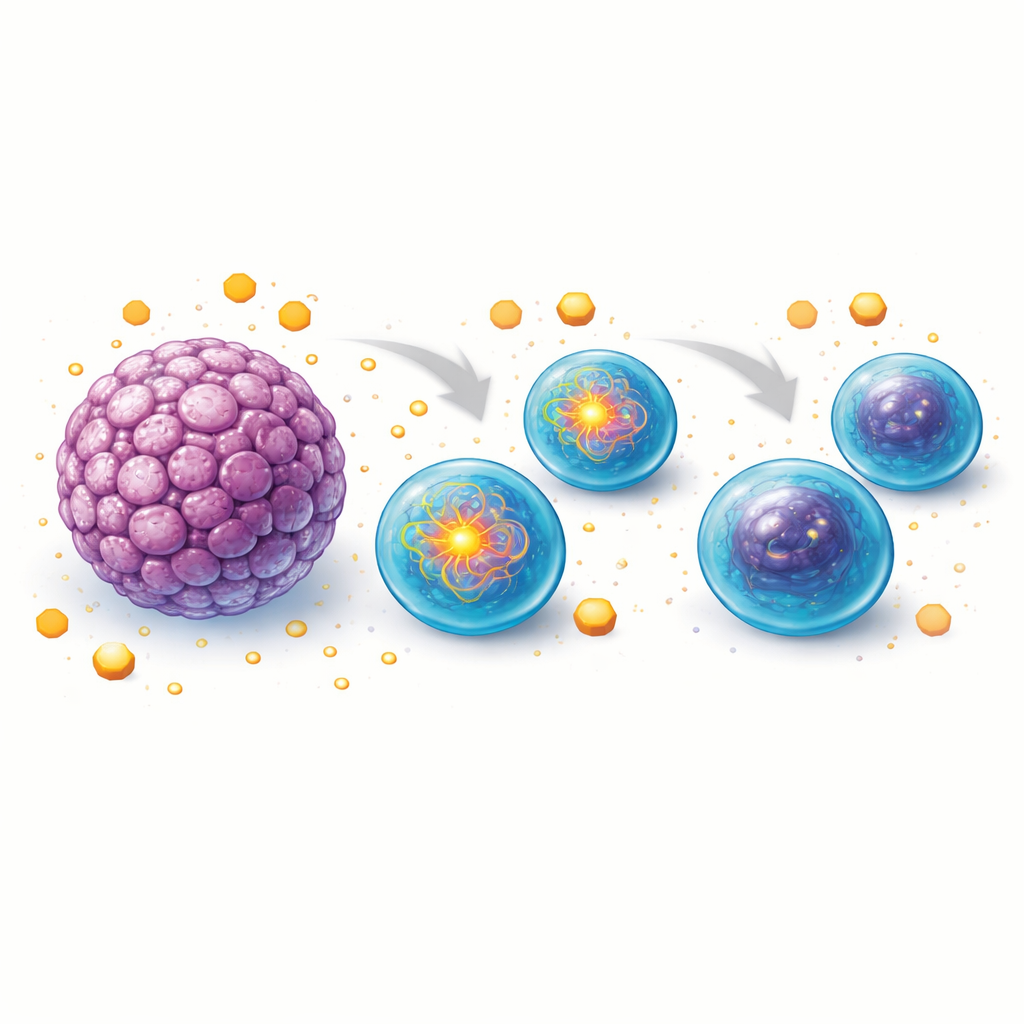
Canales de combustible rotos y soldados inmunes cansados
Un análisis adicional mostró que los linfocitos B co-cultivados con organoides tumorales también captaban menos ácidos grasos y producían niveles más bajos de enzimas necesarias para utilizar las grasas como combustible. Esto significaba que dos fuentes energéticas principales—azúcares y grasas—quedaban comprometidas. Como resultado, aunque los linfocitos B parecían cada vez más dependientes de las mitocondrias, carecían del combustible necesario y de los componentes funcionales para mantener la producción mitocondrial de energía a plena velocidad. El panorama que surge es el de linfocitos B que inicialmente intentan aumentar su actividad en el entorno tumoral, pero se quedan atascados a medida que la competencia por nutrientes y los factores derivados del tumor erosionan su capacidad metabólica.
Qué significa esto para futuros tratamientos contra el cáncer
En términos sencillos, este estudio muestra que muchos linfocitos B dentro de los tumores colorrectales son empujados a un modo agotado y de baja energía. Cambian los tipos de anticuerpos que favorecen, pierden la capacidad de madurar plenamente y ven cómo su sistema energético queda progresivamente saboteado por el entorno tumoral. Para los no especialistas, la conclusión principal es que el cáncer puede desarmar partes del sistema inmune no solo mediante supresión directa, sino también cortando o desviando su suministro de energía. Al mapear estos cambios, el trabajo abre la puerta a terapias potenciales que restauren o reprogramen el metabolismo de los linfocitos B, con el objetivo de convertir a estas células cansadas en aliados activos en la lucha del organismo contra el cáncer colorrectal.
Cita: Martinis, E., Tonon, S., Valeri, V. et al. Immunophenotypic skewing of B cells toward IgD⁻CD27⁻IgG⁺ subtype and metabolic attenuation in colorectal cancer. Sci Rep 16, 11403 (2026). https://doi.org/10.1038/s41598-026-41446-x
Palabras clave: cáncer colorrectal, linfocitos B, microambiente tumoral, metabolismo inmune, inmunoterapia contra el cáncer