Clear Sky Science · it
Deviazione immunofenotipica delle cellule B verso il sottotipo IgD⁻CD27⁻IgG⁺ e attenuazione metabolica nel carcinoma colorettale
Perché i difensori dell’organismo possono vacillare nel cancro del colon
Il carcinoma colorettale non è soltanto una massa di cellule impazzite; è una comunità complessa in cui cellule tumorali e cellule immunitarie interagiscono continuamente. Tra queste cellule immunitarie ci sono le cellule B, meglio conosciute per la produzione di anticorpi e il loro ruolo nella difesa dalle infezioni. Questo studio esplora cosa accade alle cellule B quando entrano nell’ambiente di un tumore del colon, rivelando che molte di esse diventano indebolite sia funzionalmente sia dal punto di vista energetico. Comprendere questo lato nascosto della risposta immunitaria potrebbe in futuro aiutare i medici a progettare terapie che spingano queste cellule a tornare a combattere il cancro.
Scoprire uno strano spostamento delle cellule B all’interno dei tumori
I ricercatori hanno iniziato confrontando le cellule B presenti nei tessuti del carcinoma colorettale con quelle dell’intestino normale vicino, prelevate dagli stessi pazienti. Nel tessuto intestinale sano, la maggior parte delle cellule B si trovava in fasi attive, produttive di anticorpi. All’interno dei tumori, tuttavia, è emerso uno schema molto diverso: un sottotipo insolito chiamato cellule B “doppio-negativo” (prive di due marcatori di superficie tipici) è diventato il gruppo dominante. Normalmente rare, queste cellule sono note per espandersi durante infezioni croniche e in alcune malattie autoimmuni, dove spesso mostrano segni di esaurimento. Nei campioni tumorali, queste cellule B doppio-negative mostravano anche bassi livelli di una proteina di superficie associata alla funzione sana, rafforzando l’idea che si trovassero in uno stato affaticato.
Da anticorpi protettivi a una risposta diversa
Nell’intestino sano, le cellule B producono di norma anticorpi IgA, che proteggono la mucosa intestinale e mantengono l’equilibrio con il microbiota residente. Nelle aree tumorali, gli autori hanno osservato che i sottogruppi dominanti di cellule B si spostavano lontano da IgA verso anticorpi IgG. Questo cambiamento nell’equilibrio degli anticorpi suggerisce che l’ambiente locale spinga le cellule B lontano dal loro ruolo barriera-protettivo verso una risposta più associata all’infiammazione. Eppure, quando il team ha stimolato le cellule B prelevate dal tumore con segnali che normalmente le inducono a diventare vere e proprie fabbriche di anticorpi, queste cellule hanno risposto male rispetto alle cellule B del tessuto sano. Nel loro insieme, queste osservazioni indicano la presenza di un consistente pool di cellule B nei tumori colorettali che sono state riconvertite e in seguito in parte disabilitate.
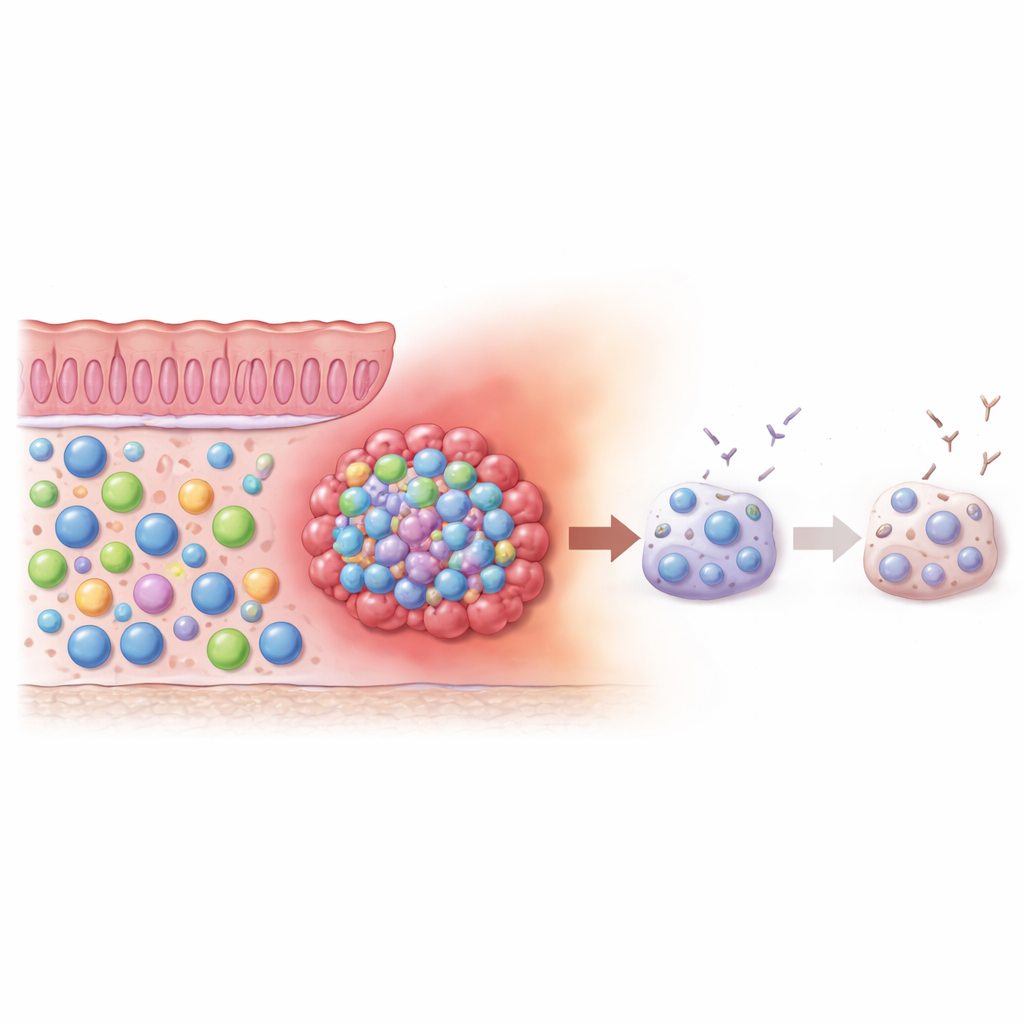
Motori silenziosi: cellule B a bassa attività nel tumore
Poiché il comportamento cellulare è strettamente legato a come le cellule usano l’energia, i ricercatori hanno poi esaminato il metabolismo delle cellule B all’interno dei tumori. Hanno misurato la sintesi proteica e l’attività mitocondriale, indicatori comuni di quanto una cellula sia “attivata”. Sorprendentemente, le cellule B doppio-negative nei tumori apparivano metabolicamente silenti, più simili a cellule B quiescenti che a difensori altamente attivi. Questo profilo a bassa marcia offre una spiegazione plausibile del perché fatichino a maturare in efficaci cellule produttrici di anticorpi. Invece di alimentare un attacco immunitario vigoroso, i loro “motori” interni appaiono regolati al ribasso, suggerendo che l’ambiente tumorale possa spingerle in uno stato più lento e meno efficace.
Come i mini-organi tumorali riconfigurano l’uso del carburante delle cellule B
Per indagare come il tessuto tumorale generi questo effetto, il team ha utilizzato modelli murini. Hanno coltivato organoidi tridimensionali dall’intestino normale e da tumori del colon indotti chimicamente, quindi hanno co-coltivato queste strutture con cellule B di topo sane. Le cellule B esposte agli organoidi tumorali si dividevano meno e producevano meno cellule secernenti anticorpi rispetto a quelle coltivate da sole o con organoidi sani. Quando i ricercatori hanno profilato le principali vie metaboliche, hanno riscontrato che le cellule B in prossimità degli organoidi tumorali perdevano progressivamente la capacità di assumere glucosio in modo efficiente e mostravano una glicolisi ridotta, la via rapida di bruciamento degli zuccheri che spesso alimenta le risposte immunitarie. Allo stesso tempo, le cellule diventavano più dipendenti dai mitocondri, ma la loro macchina mitocondriale declinava nel tempo, con potenziale di membrana ridotto, consumo di ossigeno diminuito e capacità energetica ridotta.
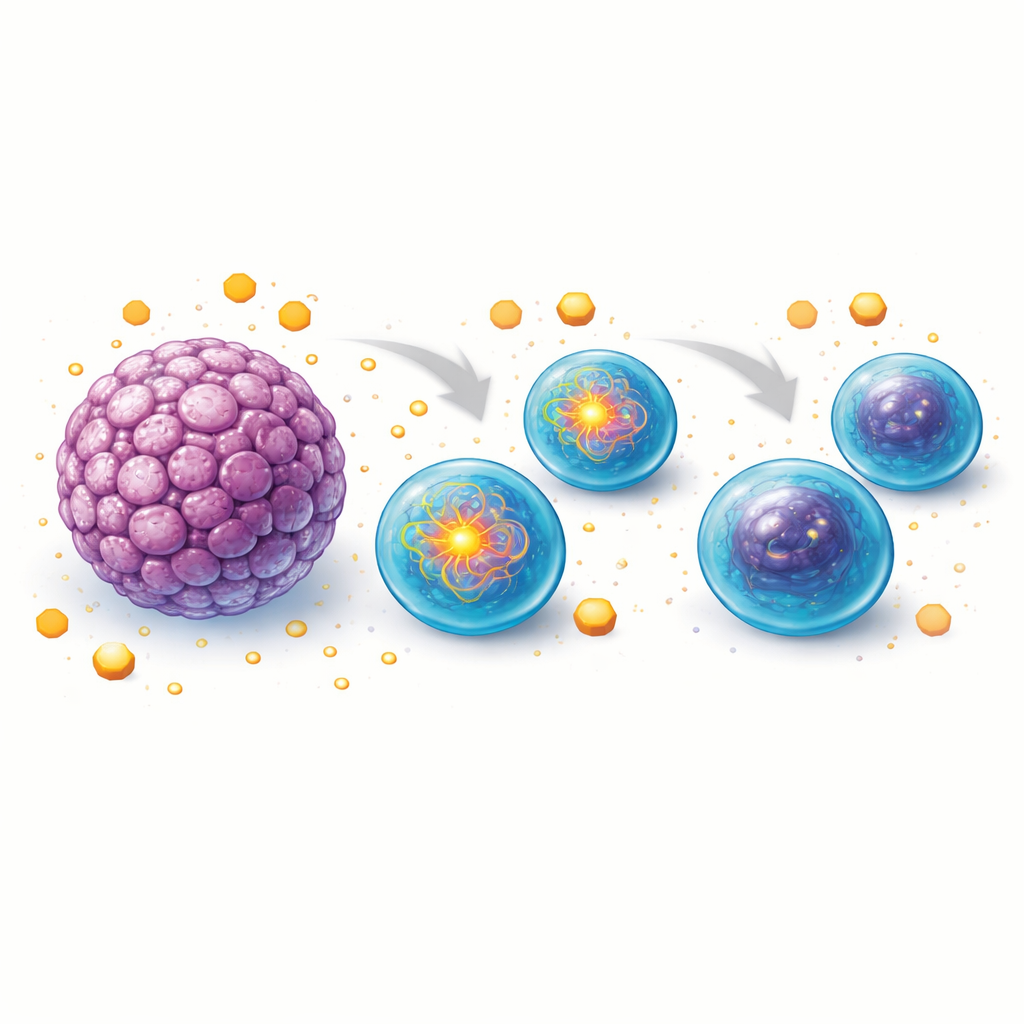
Tubi del carburante interrotti e soldati immunitari stanchi
Analisi ulteriori hanno mostrato che le cellule B co-coltivate con organoidi tumorali assumevano anche meno acidi grassi e producevano livelli inferiori di enzimi necessari per usare i grassi come combustibile. Ciò significava che due fonti energetiche principali — zuccheri e grassi — erano entrambe compromesse. Di conseguenza, sebbene le cellule B sembrassero sempre più dipendenti dai mitocondri, mancavano del carburante necessario e dei componenti funzionali per mantenere la produzione energetica mitocondriale a pieno regime. Il quadro che emerge è di cellule B che inizialmente cercano di aumentare la propria attività nell’ambiente tumorale, per poi incepparsi man mano che la competizione per i nutrienti e i fattori derivati dal tumore erodono la loro capacità metabolica.
Cosa significa per i futuri trattamenti contro il cancro
Simplificando, questo studio mostra che molte cellule B all’interno dei tumori colorettali vengono spinte in una modalità esausta e a basso consumo energetico. Cambiano i tipi di anticorpi che prediligono, perdono la capacità di maturare pienamente e vedono progressivamente sabotati i loro sistemi energetici dall’ambiente tumorale. Per i non specialisti, il punto chiave è che il cancro può disarmare parti del sistema immunitario non solo attraverso la soppressione diretta, ma anche interrompendo o deviando la loro fornitura di energia. Mappando questi cambiamenti, il lavoro apre la strada a terapie potenziali che ripristinino o rimettano a punto il metabolismo delle cellule B, con l’obiettivo di trasformare queste cellule stanche in alleate attive nella lotta dell’organismo contro il carcinoma colorettale.
Citazione: Martinis, E., Tonon, S., Valeri, V. et al. Immunophenotypic skewing of B cells toward IgD⁻CD27⁻IgG⁺ subtype and metabolic attenuation in colorectal cancer. Sci Rep 16, 11403 (2026). https://doi.org/10.1038/s41598-026-41446-x
Parole chiave: carcinoma colorettale, cellule B, microambiente tumorale, metabolismo immunitario, immunoterapia del cancro