Clear Sky Science · de
Immunophenotypische Verschiebung von B‑Zellen hin zum IgD⁻CD27⁻IgG⁺ Subtyp und metabolische Abschwächung beim Kolorektalkarzinom
Warum die körpereigenen Verteidiger beim Darmkrebs nachlassen können
Kolorektales Karzinom ist nicht einfach nur ein Haufen entgleister Zellen; es ist eine komplexe Gemeinschaft, in der Tumorzellen und Immunzellen ständig miteinander interagieren. Zu diesen Immunzellen zählen B‑Zellen, die vor allem für die Antikörperproduktion bekannt sind und uns helfen, Infektionen zu bekämpfen. Diese Studie untersucht, was mit B‑Zellen geschieht, wenn sie in die Umgebung eines Darmtumors eintreten, und zeigt, dass viele von ihnen sowohl funktionell als auch energetisch geschwächt werden. Das Verständnis dieser bislang wenig beachteten Seite der Immunantwort könnte helfen, Therapien zu entwickeln, die diese Zellen wieder dazu bringen, gegen den Krebs zu kämpfen.
Aufdeckung einer ungewöhnlichen B‑Zell‑Verschiebung in Tumoren
Die Forscher begannen damit, B‑Zellen aus kolorektalem Tumorgewebe mit denen aus nahegelegenem, gesundem Darmgewebe derselben Patienten zu vergleichen. Im gesunden Darmgewebe befanden sich die meisten B‑Zellen in aktiven, antikörperproduzierenden Stadien. Im Tumor zeigte sich jedoch ein ganz anderes Bild: Ein ungewöhnlicher Subtyp, die sogenannten „double‑negative“ B‑Zellen (ohne zwei typische Oberflächenmarker), wurde zur dominanten Gruppe. Diese normalerweise seltenen Zellen sind bekannt dafür, sich bei chronischen Infektionen und einigen Autoimmunerkrankungen zu vergrößern, wobei sie oft Erschöpfungserscheinungen zeigen. In den Tumorproben zeigten diese double‑negative B‑Zellen ebenfalls niedrige Werte eines Oberflächenproteins, das mit gesunder Funktion assoziiert ist, was die Vorstellung unterstreicht, dass sie in einem erschöpften Zustand sind.
Von schützenden Antikörpern zu einer veränderten Reaktion
Im gesunden Darm produzieren B‑Zellen typischerweise IgA‑Antikörper, die die Darmoberfläche schützen und das Gleichgewicht mit der dortigen Mikrobiota wahren. Im Tumor fanden die Autoren jedoch einen Subtypenwechsel weg von IgA hin zu IgG‑Antikörpern. Dieses veränderte Antikörpergleichgewicht deutet darauf hin, dass die lokale Umgebung die B‑Zellen aus ihrer normalen barriereschützenden Rolle in eine stärker entzündungsbezogene Reaktion lenkt. Dennoch reagierten B‑Zellen aus Tumorgewebe, wenn man sie mit Signalen stimulierte, die normalerweise zur vollen Antikörperproduktion führen, deutlich schlechter als B‑Zellen aus gesundem Gewebe. Zusammengenommen deuten diese Beobachtungen auf einen beträchtlichen Pool von B‑Zellen in kolorektalen Tumoren hin, die umgelenkt und teilweise funktionsunfähig gemacht worden sind.
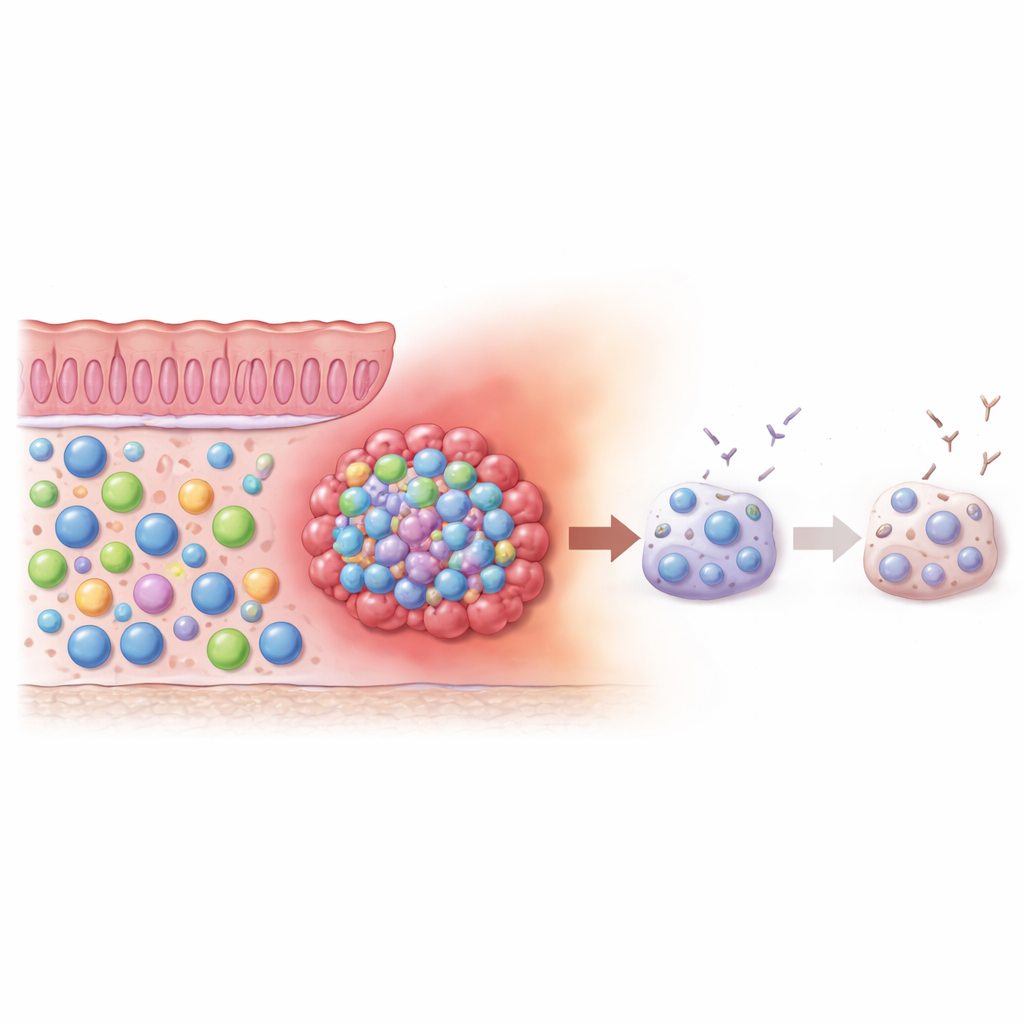
Stille Motoren: niedrigaktive B‑Zellen im Tumor
Da das Verhalten von Zellen eng mit ihrer Energienutzung verknüpft ist, untersuchten die Forscher als Nächstes den Stoffwechsel der B‑Zellen innerhalb der Tumoren. Sie maßen Proteinsynthese und mitochondriale Aktivität, gängige Indikatoren dafür, wie „aktiviert“ eine Zelle ist. Überraschenderweise wirkten die double‑negativen B‑Zellen im Tumor metabolisch ruhig und ähnelten eher ruhenden B‑Zellen als hochaktiven Verteidigern. Dieses gedämpfte Profil liefert eine nachvollziehbare Erklärung dafür, warum sie Mühe haben, sich zu kräftigen antikörperproduzierenden Zellen zu entwickeln. Statt eine kräftige Immunantwort anzutreiben, scheinen ihre inneren Motoren zurückgeschaltet zu sein, was darauf hindeutet, dass die Tumorumgebung sie in einen trägen, weniger effektiven Zustand drängen könnte.
Wie Tumor‑Mini‑Organoide die Brennstoffnutzung von B‑Zellen umlenken
Um zu untersuchen, wie Tumorgewebe diesen Effekt hervorruft, nutzte das Team Mausmodelle. Sie züchteten dreidimensionale „Organoide“ aus normalem Darmgewebe und aus chemisch induzierten Darmtumoren und ko‑kultivierten diese Strukturen mit gesunden Maus‑B‑Zellen. B‑Zellen, die Tumor‑Organoiden ausgesetzt waren, teilten sich weniger und produzierten weniger antikörperabsondernde Zellen als B‑Zellen, die allein oder mit gesunden Organoiden kultiviert wurden. Als die Forscher zentrale Stoffwechselwege analysierten, stellten sie fest, dass B‑Zellen in der Nähe von Tumor‑Organoiden allmählich ihre Fähigkeit verloren, Glukose effizient aufzunehmen, und eine reduzierte Glykolyse zeigten — die schnelle Zuckerverbrennungsstrecke, die Immunreaktionen oft antreibt. Gleichzeitig wurden die Zellen abhängiger von ihren Mitochondrien, doch deren Funktion nahm mit der Zeit ab: verminderte Membranpotenziale, reduzierte Sauerstoffaufnahme und eine verminderte Fähigkeit zur Energieproduktion.
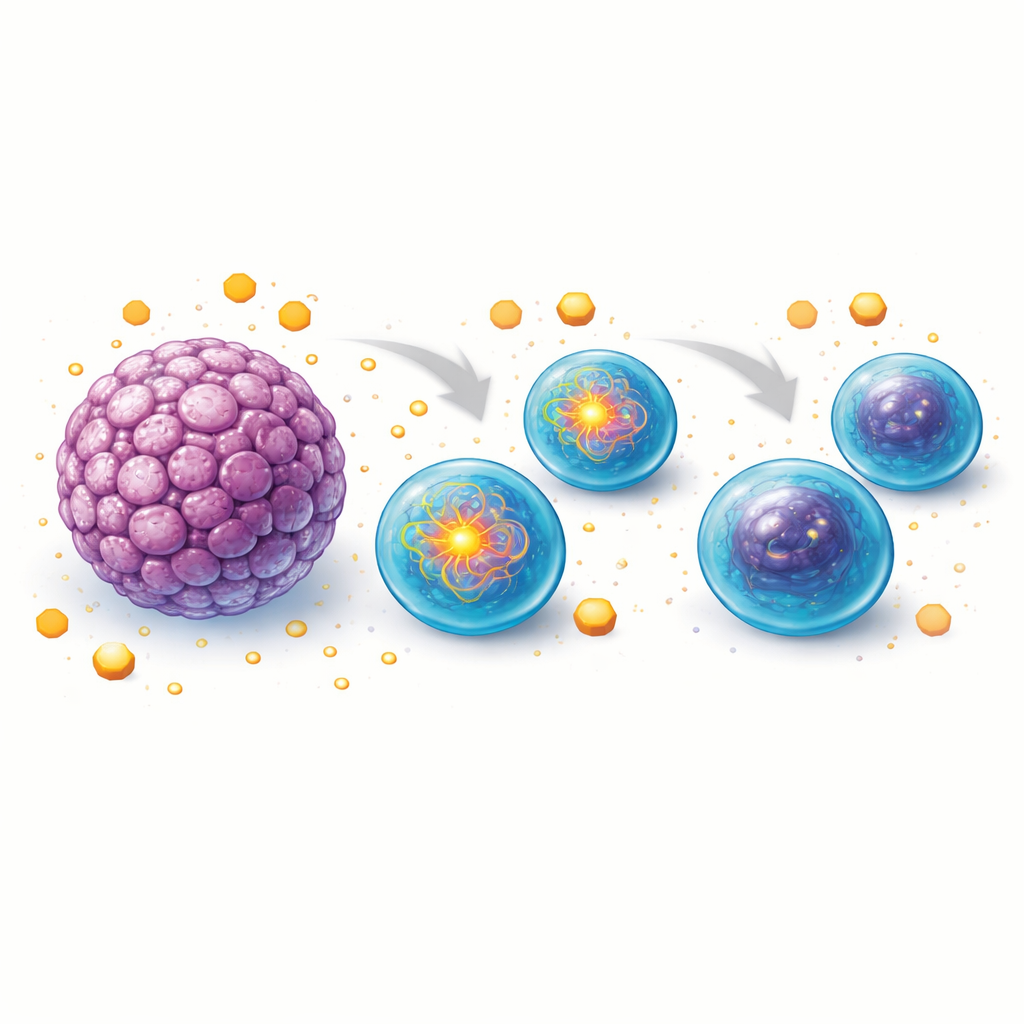
Kaputte Treibstoffleitungen und ermüdete Immunsoldaten
Weitere Analysen zeigten, dass B‑Zellen, die mit Tumor‑Organoiden ko‑kultiviert wurden, auch weniger Fettsäuren aufnahmen und geringere Mengen an Enzymen produzierten, die erforderlich sind, um Fette als Brennstoff zu nutzen. Das bedeutete, dass zwei wichtige Energiequellen — Zucker und Fette — gleichermaßen beeinträchtigt waren. Infolgedessen wirkten die B‑Zellen zwar zunehmend mitochondrienabhängig, es fehlte ihnen jedoch sowohl an Brennstoff als auch an funktionalen Komponenten, um die mitochondriale Energieproduktion auf hohem Niveau aufrechtzuerhalten. Das entstehende Bild ist das einer B‑Zell‑Population, die zunächst versucht, ihre Aktivität in der Tumorumgebung hochzufahren, aber ins Stocken gerät, während Nährstoffkonkurrenz und tumorabgeleitete Faktoren ihre metabolische Leistungsfähigkeit untergraben.
Was das für zukünftige Krebstherapien bedeutet
Kurz gesagt zeigt diese Arbeit, dass viele B‑Zellen in kolorektalen Tumoren in einen erschöpften, energiearmen Modus gedrängt werden. Sie ändern die bevorzugten Antikörpertypen, verlieren ihre Fähigkeit zur vollständigen Reifung und haben ihre Energiesysteme schrittweise durch die Tumorumgebung sabotiert. Für nicht‑Fachleute ist die zentrale Erkenntnis, dass Krebs Teile des Immunsystems nicht nur durch direkte Unterdrückung handlungsunfähig machen kann, sondern auch durch das Abschneiden oder Fehlleiten ihrer Energieversorgung. Durch die Kartierung dieser Veränderungen öffnet die Studie die Tür zu potenziellen Therapien, die den Metabolismus von B‑Zellen wiederherstellen oder umprogrammieren, mit dem Ziel, diese erschöpften Zellen wieder zu aktiven Verbündeten im Kampf des Körpers gegen kolorektalen Krebs zu machen.
Zitation: Martinis, E., Tonon, S., Valeri, V. et al. Immunophenotypic skewing of B cells toward IgD⁻CD27⁻IgG⁺ subtype and metabolic attenuation in colorectal cancer. Sci Rep 16, 11403 (2026). https://doi.org/10.1038/s41598-026-41446-x
Schlüsselwörter: Kolorektalkarzinom, B‑Zellen, Tumormikroumgebung, Immunmetabolismus, Krebsimmuntherapie