Clear Sky Science · zh
新型吲哚连接的1,2,4-三唑衍生物:作为双重FAK抑制剂与诱导凋亡剂以体外靶向三阴性乳腺癌的存活与迁移
这项研究对患者的重要性
三阴性乳腺癌是最难治疗的乳腺癌类型之一,因为它缺乏许多现有药物所针对的激素受体。患者常面临疾病侵袭性强、选择有限以及化疗副作用大的情况。本研究探索了一种不同策略:开发一类新型小分子,旨在关闭癌细胞内关键的生存开关并促使其自我毁灭,同时尽可能减少对健康细胞的伤害。
以新方式打击侵袭性癌症
研究者将注意力集中在倾向于早期扩散并对常规疗法耐受的三阴性乳腺癌上。这类肿瘤常依赖一种称为粘着斑激酶(FAK)的蛋白,FAK帮助癌细胞黏附、移动并在应激情况下存活。当FAK过度活跃时,肿瘤变得更具侵袭性且更难以消灭。由于目前尚无广泛应用的针对该癌种的靶向药物,阻断FAK已成为减缓肿瘤生长并阻止其扩散的有吸引力的策略。
设计量身定制的癌症拮抗剂
为针对FAK,团队合成了一组由两种化学基元构成的新分子:吲哚和1,2,4-三唑。通过不同方式连接和排列这些片段,他们得到若干相关化合物,并在两种乳腺癌细胞系与正常人成纤维细胞上进行测试。三个候选物(标记为3c、4c和5c)在以较低剂量抑制癌细胞生长同时对正常细胞毒性较低方面表现突出。其中,化合物4c(含两个通过三唑骨架连接的吲哚环)显示出最有希望的特性。 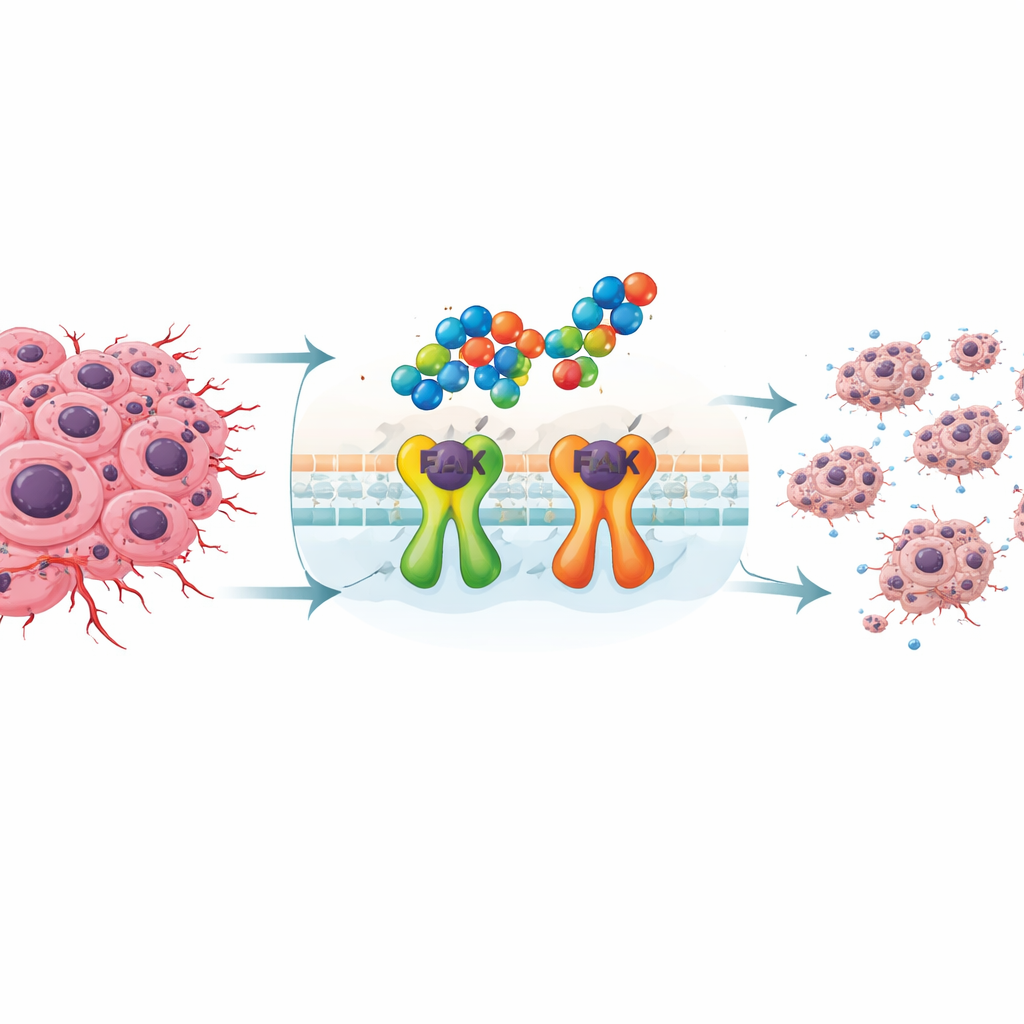
减缓生长、阻断迁移并触发细胞自毁
实验室测试表明,这些新化合物不仅仅是减慢癌细胞分裂。在划痕“伤口”实验中,即在细胞单层上制造一条间隙并观察细胞闭合速度,3c、4c和5c均显著延缓了两种乳腺癌细胞系的迁移。4c还使癌细胞在细胞周期的特定检查点停滞:它使一株乳腺癌细胞系(MCF‑7)在DNA复制阶段停滞,而另一株三阴性细胞系(MDA‑MB‑231)在分裂前被阻断,限制了它们的增殖能力。当团队检测程序性细胞死亡标志时,发现4c在三阴性细胞中尤为有效,几乎使约91%的细胞进入凋亡,而伴随的坏死很少,这种模式在疗法上通常更为理想。
打击癌细胞的生存开关
为理解这些分子如何发挥作用,研究者测量了关键基因和蛋白的变化。在三阴性细胞中,4c显著降低了编码FAK的基因活性,并将FAK蛋白水平降低约61%,几乎可与用于比较的已知FAK抑制药相媲美。与此同时,4c降低了保护细胞免于死亡的信号,例如BCL2和趋化因子CCL5,并增强了促死信号如caspase‑3。由于FAK和CCL5也与癌细胞的迁移及免疫逃逸相关,它们的抑制有助解释实验中观察到的强烈抗迁移与促凋亡效应。基于计算的对接研究也支持这一观点,显示4c能紧密嵌入FAK的活性口袋并形成多重稳定接触,符合对该酶的直接抑制机制。
早期安全性迹象与后续步骤
在任何候选药物进入临床试验之前,必须评估其安全性。团队对小鼠给予单次4c剂量并观察两天。在最低测得剂量(每公斤体重12.5毫克)下,动物未表现出明显的痛苦迹象,肝脏与肾脏组织在显微镜下大体完好。较高剂量开始引起更明显的组织损伤和生化应激迹象,表明剂量选择需谨慎。额外的吸收、代谢与毒性计算模型显示,与某些现有抗癌药物相比,4c具有相对有利的性质,但潜在的肝脏影响与心脏相关风险仍需密切监测。 
这对未来治疗的可能意义
简而言之,这项工作确定了一种新小分子4c,它既能阻断三阴性乳腺癌细胞的关键生存通路,又能积极促使它们进入有序的自我毁灭,同时减缓其迁移与扩散能力。尽管研究仍处于早期的临床前阶段,且仍需在动物肿瘤模型和长期安全性研究中进行大量测试,4c为针对这一最具挑战性的乳腺癌类型开辟了一类新型靶向治疗的有希望蓝图。
引用: Abd El Salam, H.A., Abu-Shahba, N., Ibrahim Fouad, G. et al. New indole-linked 1,2,4-triazole derivatives as dual FAK inhibitors and apoptosis inducers targeting survival and migration in triple-negative breast cancer in-vitro. Sci Rep 16, 13134 (2026). https://doi.org/10.1038/s41598-026-41032-1
关键词: 三阴性乳腺癌, 粘着斑激酶, 靶向治疗, 程序性细胞死亡(凋亡), 小分子抑制剂