Clear Sky Science · sv
Nya indol‑kopplade 1,2,4‑triazolderivat som dubbla FAK‑hämmare och apoptosinducerare som riktar in sig på överlevnad och migration vid trippelnegativ bröstcancer in vitro
Varför denna forskning är betydelsefull för patienter
Trippelnegativ bröstcancer är en av de svåraste formerna av bröstcancer att behandla eftersom den saknar de hormonreceptorer som många moderna läkemedel riktar sig mot. Patienter möter ofta en aggressiv sjukdom, begränsade behandlingsalternativ och tuff cytostatika. Denna studie undersöker en annan taktik: en ny familj små molekyler designade för att stänga av en viktig överlevnadsknapp inne i cancerceller och driva dem till självdestruktion, samtidigt som friska celler i möjligaste mån skonas.
Ett nytt sätt att slå mot en aggressiv cancer
Forskarna fokuserade på trippelnegativ bröstcancer, som tenderar att sprida sig tidigt och visa motstånd mot standardbehandlingar. Dessa tumörer förlitar sig ofta på ett protein kallat fokal adhesionskinas, eller FAK, som hjälper cancerceller att fästa, röra sig och överleva i stressiga förhållanden. När FAK är överaktivt blir tumörer mer invasiva och svårare att döda. Eftersom det fortfarande saknas allmänt använda riktade läkemedel för denna cancerform har blockering av FAK blivit en attraktiv strategi för att sakta tumörtillväxt och förhindra spridning.
Design av skräddarsydda cancerhämmare
För att angripa FAK syntetiserade teamet en serie nya molekyler byggda av två välkända byggstenar för kemister: indoler och 1,2,4‑triazoler. Genom att länka och arrangera dessa delar på olika sätt framställde de flera besläktade föreningar och testade dem mot två bröstcancellinjer och normala humana fibroblaster. Tre kandidater, benämnda 3c, 4c och 5c, utmärkte sig för sin förmåga att bromsa cancercellstillväxt vid relativt låga doser samtidigt som de var mindre skadliga för normala celler. Bland dem framträdde förening 4c, som innehåller två indolringar sammanlänkade via en triazolkärna, som mest lovande. 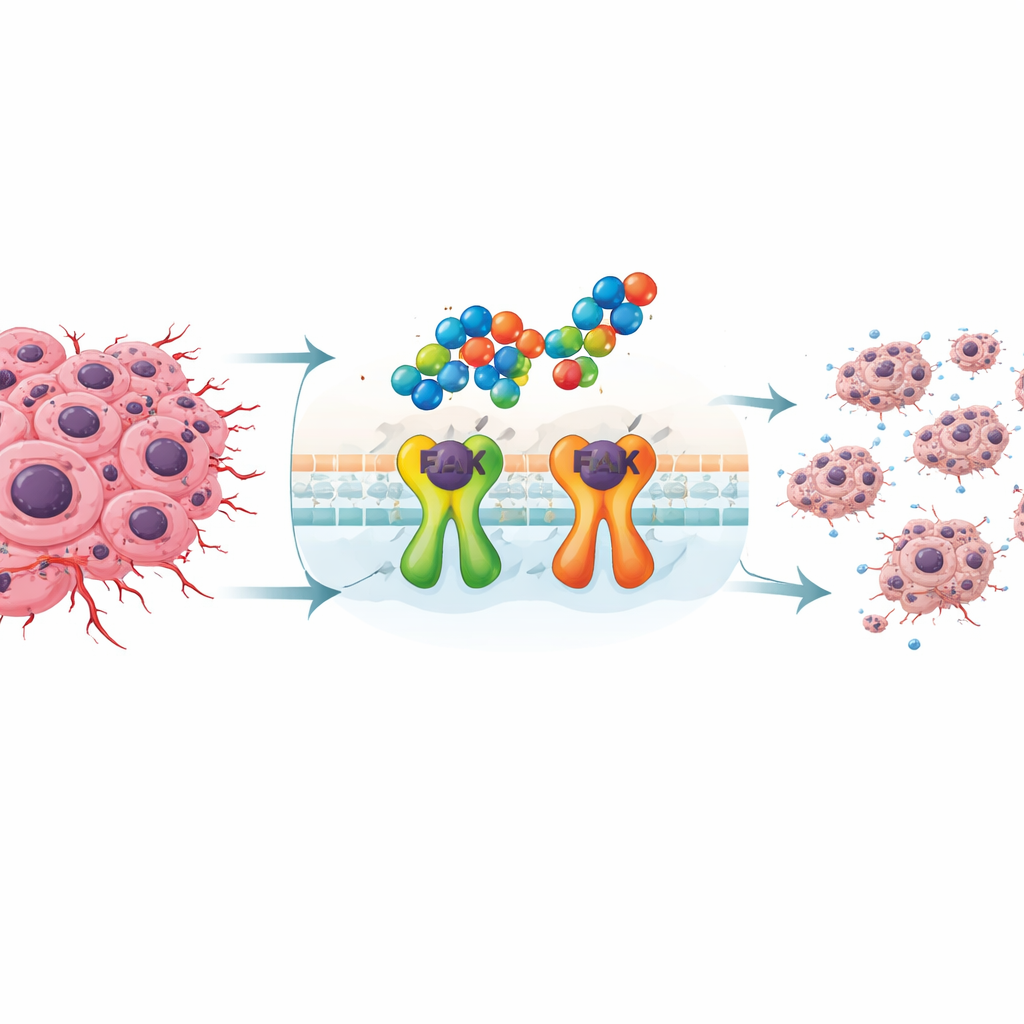
Bromsa tillväxt, blockera rörelse och utlösa celldöd
Laboratorietester visade att dessa nya föreningar gör mer än att bara sakta cancercelldelning. I så kallade scratch‑ eller ”sårläknings”experiment, där ett gap skapas i ett cellager och forskarna observerar hur snabbt cellerna kryper för att sluta det, fördröjde föreningarna 3c, 4c och 5c starkt cellrörelsen i båda bröstcancellinjerna. Förening 4c tvingade också cancerceller att stanna upp vid specifika kontrollpunkter i cellcykeln: den spärrade en bröstcancellinje (MCF‑7) i DNA‑kopieringsfasen och en annan trippelnegativ linje (MDA‑MB‑231) före delning, vilket begränsade deras förmåga att multiplicera. När teamet analyserade markörer för programmerad celldöd fann de att 4c var särskilt potent i trippelnegativa celler och drev nästan 91 % av dem in i apoptos med mycket lite kaotisk nekros, ett mönster som i allmänhet är mer önskvärt för terapi.
Slag mot cancercellens överlevnadsknapp
För att förstå hur dessa molekyler utövar sina effekter mätte forskarna förändringar i nyckelgener och proteiner. I trippelnegativa celler minskade 4c kraftigt aktiviteten hos genen som kodar för FAK och sänkte FAK‑proteinnivåerna med cirka 61 %, nästan i nivå med ett känt FAK‑blockerande läkemedel som användes som jämförelse. Samtidigt minskade 4c signaler som skyddar celler från död, såsom BCL2 och kemokinen CCL5, och ökade pro‑dödsignaler som kaspas‑3. Eftersom FAK och CCL5 också är kopplade till hur cancerceller migrerar och undviker immunsystemet hjälper deras hämning att förklara de starka anti‑migratoriska och pro‑apoptotiska effekterna som observerades i laboratoriet. Datorbaserade dockningsstudier stödde denna bild genom att visa att 4c passar tätt i FAK:s aktiva ficka och gör flera stabiliserande kontakter, vilket är förenligt med direkt hämning av enzymet.
Tidiga säkerhetssignaler och nästa steg
Innan någon kandidat kan gå vidare mot kliniska prövningar måste dess säkerhet utvärderas. Teamet gav engångsdoser av 4c till möss och följde dem i två dagar. Vid den lägsta testade dosen, 12,5 mg per kilogram kroppsvikt, visade djuren inga uppenbara tecken på påfrestning och lever‑ och njurvävnader förblev i stort sett intakta vid mikroskopisk undersökning. Högre doser började orsaka märkbara vävnadsskador och biokemiska tecken på stress, vilket indikerar att noggrann dosval kommer att vara viktigt. Ytterligare datorbaserade modeller av absorption, metabolism och toxikologi föreslog att 4c har relativt fördelaktiga egenskaper jämfört med vissa befintliga cancerläkemedel, även om potentiella leverpåverkan och hjärt‑relaterade risker behöver övervakas noggrant. 
Vad detta kan innebära för framtida behandlingar
Enkelt uttryckt identifierar detta arbete en ny liten molekyl, 4c, som både kan blockera en nyckelöverlevnads‑väg i trippelnegativa bröstcancerceller och aktivt driva dem mot ordnad självdestruktion, samtidigt som den bromsar deras förmåga att röra sig och sprida sig. Även om forskningen fortfarande är i ett tidigt, prekliniskt skede och betydligt mer testning krävs i djurtumörmodeller och långsiktiga säkerhetsstudier, ger 4c en lovande ritning för en ny klass av riktade terapier mot en av de mest utmanande formerna av bröstcancer.
Citering: Abd El Salam, H.A., Abu-Shahba, N., Ibrahim Fouad, G. et al. New indole-linked 1,2,4-triazole derivatives as dual FAK inhibitors and apoptosis inducers targeting survival and migration in triple-negative breast cancer in-vitro. Sci Rep 16, 13134 (2026). https://doi.org/10.1038/s41598-026-41032-1
Nyckelord: trippelnegativ bröstcancer, fokal adhesionskinas, målinriktad terapi, apoptos, liten molekylhämmare