Clear Sky Science · ru
Новые производные 1,2,4-триазола, связанные с индолом, как двойные ингибиторы FAK и индукторы апоптоза, нацеленные на выживание и миграцию при тройственно-негативном раке молочной железы in vitro
Почему это исследование важно для пациентов
Тройственно-негативный рак молочной железы — одна из наиболее трудных для лечения форм, поскольку у таких опухолей отсутствуют гормональные рецепторы, на которые ориентированы многие современные препараты. Пациенты нередко сталкиваются с агрессивным течением болезни, ограниченным набором вариантов лечения и тяжелой химиотерапией. В этой работе рассматривается иная тактика: новая группа малых молекул, разработанных для того, чтобы выключать ключевой «переключатель» выживания внутри раковых клеток и стимулировать их к самоуничтожению, при этом по возможности щадя нормальные клетки.
Новый способ борьбы с агрессивным раком
Исследователи сосредоточились на тройственно-негативном раке молочной железы, который имеет тенденцию рано метастазировать и сопротивляться стандартным методам лечения. Такие опухоли часто зависят от белка, называемого фокальной адгезионной киназой (FAK), который помогает раковым клеткам прикрепляться, передвигаться и выживать в стрессовых условиях. При избыточной активности FAK опухоли становятся более инвазивными и труднее поддаются уничтожению. Поскольку для этого типа рака до сих пор нет широкоприменяемых таргетных препаратов, блокирование FAK выглядит привлекательной стратегией для замедления роста опухоли и предотвращения её распространения.
Проектирование специально подобных блокаторов рака
Чтобы воздействовать на FAK, команда синтезировала набор новых молекул, основанных на двух хорошо знакомых химикам строительных блоках: индолах и 1,2,4‑триазолах. Соединяя и комбинируя эти фрагменты различными способами, они получили несколько родственных соединений и протестировали их на двух линиях клеток рака молочной железы и на нормальных фибробластах человека. Три кандидата, обозначенные как 3c, 4c и 5c, выделились своей способностью подавлять рост раковых клеток при относительно низких дозах, будучи менее токсичными для нормальных клеток. Среди них соединение 4c, содержащее две индольные группы, связанные через триазольное ядро, показало наибольший потенциал. 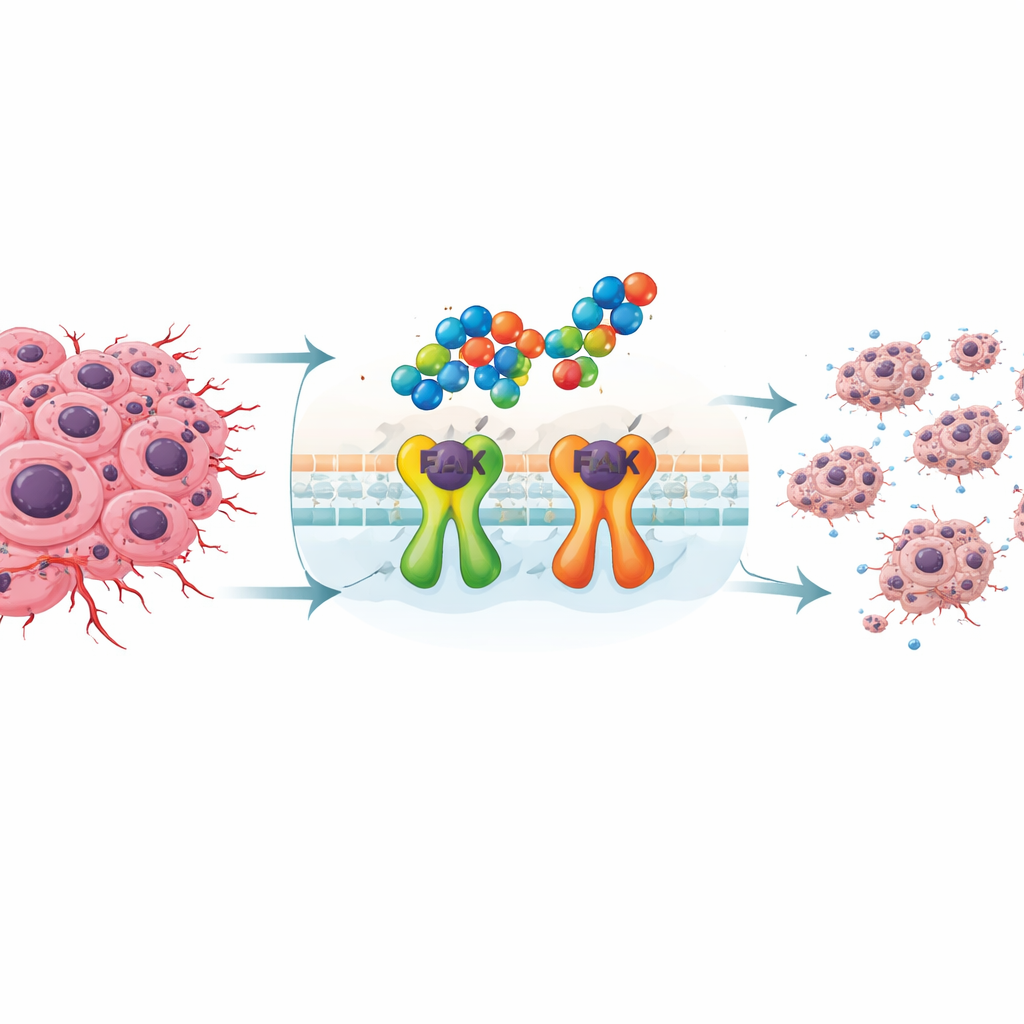
Замедление роста, блокирование миграции и запуск клеточного самоубийства
Лабораторные тесты показали, что эти новые соединения делают не только одно — не просто замедляют деление раковых клеток. В экспериментах «царапанья» (scratch), где создают зазор в монослое клеток и наблюдают, как быстро клетки закрывают его, 3c, 4c и 5c значительно задерживали миграцию в обеих клеточных линиях. Соединение 4c также заставляло раковые клетки останавливаться на определённых контрольных пунктах клеточного цикла: в одной линии молочной железы (MCF‑7) оно блокировало фазу репликации ДНК, а в тройственно-негативной линии (MDA‑MB‑231) — до деления, ограничивая их способность размножаться. При анализе маркеров программируемой клеточной гибели оказалось, что 4c особенно эффективен в тройственно-негативных клетках, выводя в апоптоз почти 91 % клеток с минимальным выражением некроза — профиль, который в общем случае предпочтительнее для терапии.
Удар по «переключателю» выживания рака
Чтобы понять механизм действия этих молекул, исследователи измеряли изменения в ключевых генах и белках. В тройственно-негативных клетках 4c резко снизил активность гена, кодирующего FAK, и уменьшил уровень белка FAK примерно на 61 %, почти достигая эффекта известного FAK‑ингибитора, использованного для сравнения. Одновременно 4c уменьшал сигналы, защищающие клетки от гибели, такие как BCL2 и хемокин CCL5, и усиливал провоцирующие смерть сигналы, например каспазу‑3. Поскольку FAK и CCL5 также связаны с миграцией раковых клеток и их уклонением от иммунного надзора, их подавление помогает объяснить выраженные антимиграционные и проапоптотические эффекты, наблюдаемые в опытах. Компьютерное докирование подтвердило эту картину, показав, что 4c плотно помещается в активный карман FAK и образует несколько стабилизирующих контактов, что согласуется с прямой ингибирующей активностью по отношению к ферменту.
Ранние признаки безопасности и дальнейшие шаги
Прежде чем любой кандидат в препараты сможет перейти к клиническим испытаниям, необходимо оценить его безопасность. Команда вводила однократные дозы 4c мышам и наблюдала их в течение двух дней. При наименьшей протестированной дозе 12,5 мг на килограмм массы тела у животных не было очевидных признаков дистресса, а ткани печени и почек в основном сохраняли нормальную структуру при микроскопическом исследовании. Более высокие дозы начали вызывать заметные повреждения тканей и биохимические признаки стресса, что указывает на необходимость тщательного подбора дозы. Дополнительные вычислительные модели абсорбции, метаболизма и токсичности показали, что 4c обладает относительно благоприятными свойствами по сравнению с некоторыми существующими противораковыми препаратами, хотя потенциальные эффекты на печень и риски, связанные с сердцем, потребуют внимательного мониторинга. 
Что это может значить для будущих методов лечения
Проще говоря, в этой работе описано новое малое молекула 4c, способное одновременно блокировать ключевой путь выживания в клетках тройственно-негативного рака молочной железы и активно направлять их к упорядоченному самоуничтожению, замедляя при этом их способность к перемещению и распространению. Хотя исследования всё ещё находятся на ранней преклинической стадии и необходимы дополнительные испытания на животных с опухолями и длительные исследования безопасности, 4c представляет собой многообещающую основу для нового класса таргетных препаратов против одной из самых сложных форм рака молочной железы.
Цитирование: Abd El Salam, H.A., Abu-Shahba, N., Ibrahim Fouad, G. et al. New indole-linked 1,2,4-triazole derivatives as dual FAK inhibitors and apoptosis inducers targeting survival and migration in triple-negative breast cancer in-vitro. Sci Rep 16, 13134 (2026). https://doi.org/10.1038/s41598-026-41032-1
Ключевые слова: тройственно-негативный рак молочной железы, фокальная адгезионная киназа, таргетная терапия, апоптоз, ингибитор малой молекулы