Clear Sky Science · pl
Nowe pochodne 1,2,4-triazolu sprzężone z indolem jako dwufunkcyjne inhibitory FAK i induktory apoptozy ukierunkowane na przeżycie i migrację w potrójnie ujemnym raku piersi in vitro
Dlaczego to badanie jest istotne dla pacjentów
Potrójnie ujemny rak piersi jest jedną z najtrudniejszych do leczenia postaci raka piersi, ponieważ brakuje w nim receptorów hormonalnych, na które ukierunkowują wiele współczesnych leków. Pacjenci często zmagają się z agresywną chorobą, ograniczonymi opcjami leczenia i uciążliwą chemioterapią. W tym badaniu zbadano inną taktykę: nową rodzinę małych cząsteczek zaprojektowanych tak, by wyłączyć kluczowy przełącznik przeżycia w komórkach nowotworowych i sprowokować ich autodestrukcję, przy jednoczesnym jak największym oszczędzaniu komórek zdrowych.
Nowy sposób ataku na agresywny nowotwór
Naukowcy skoncentrowali się na potrójnie ujemnym raku piersi, który ma skłonność do wczesnego rozprzestrzeniania się i oporności na standardowe terapie. Guzy te często polegają na białku zwanym kinazą ognisk adhezji, czyli FAK, które pomaga komórkom nowotworowym przyczepiać się, poruszać i przetrwać stresujące warunki. Gdy FAK jest nadmiernie aktywna, guzy stają się bardziej inwazyjne i trudniejsze do zniszczenia. Ponieważ wciąż nie ma powszechnie stosowanych leków celowanych dla tego typu raka, blokowanie FAK stało się atrakcyjną strategią spowalniania wzrostu guza i zatrzymywania jego rozprzestrzeniania.
Projektowanie dopasowanych blokerów raka
Aby zaatakować FAK, zespół zsyntetyzował zestaw nowych cząsteczek zbudowanych z dwóch dobrze znanych chemikom fragmentów: indoli i 1,2,4-triazoli. Łącząc i układając te elementy w różny sposób, uzyskali kilka pokrewnych związków, które następnie przetestowali przeciwko dwóm liniom komórek raka piersi oraz komórkom ludzkich fibroblastów. Trzy kandydaty, oznaczone jako 3c, 4c i 5c, wyróżniały się zdolnością do hamowania wzrostu komórek nowotworowych przy stosunkowo niskich dawkach, przy mniejszej szkodliwości dla komórek normalnych. Wśród nich związek 4c, zawierający dwie pierścienie indolowe połączone rdzeniem triazolowym, okazał się najbardziej obiecujący. 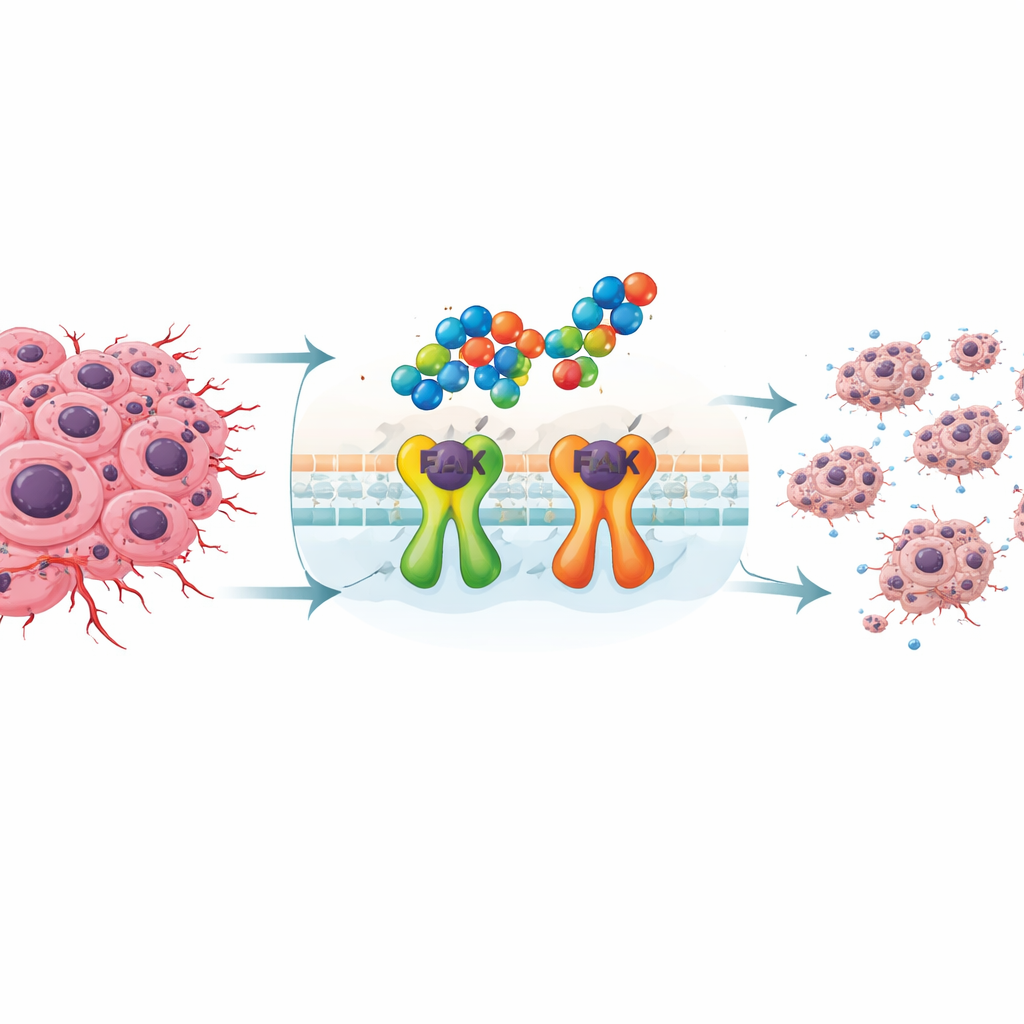
Spowalnianie wzrostu, blokowanie ruchu i wywoływanie samobójstwa komórkowego
Badania laboratoryjne wykazały, że te nowe związki robią więcej niż tylko hamować podział komórek nowotworowych. W eksperymentach typu „zadrapanie” (scratch), gdzie tworzy się przerwę w monowarstwie komórek i obserwuje, jak szybko komórki przesuwają się, by ją zamknąć, związki 3c, 4c i 5c wyraźnie opóźniały migrację w obu badanych liniach raka piersi. Związek 4c dodatkowo zatrzymywał komórki nowotworowe w określonych punktach kontrolnych cyklu komórkowego: zablokował jedną linię raka piersi (MCF-7) w fazie kopiowania DNA, a drugą potrójnie ujemną (MDA-MB-231) przed podziałem, ograniczając ich zdolność do namnażania. Przy badaniu markerów zaprogramowanej śmierci komórkowej stwierdzono, że 4c był szczególnie silny w komórkach potrójnie ujemnych, indukując apoptozę u niemal 91% z nich przy minimalnej nekrozie, co jest wzorcem zwykle bardziej pożądanym w terapii.
Atak na przełącznik przeżycia nowotworu
Aby zrozumieć mechanizm działania tych cząsteczek, badacze zmierzyli zmiany w kluczowych genach i białkach. W komórkach potrójnie ujemnych 4c wyraźnie zmniejszył aktywność genu kodującego FAK i obniżył poziom białka FAK o około 61%, niemal dorównując znanemu lekowi blokującemu FAK stosowanemu jako porównanie. Równocześnie 4c obniżał sygnały chroniące komórki przed śmiercią, takie jak BCL2 i chemokina CCL5, oraz zwiększał sygnały pro‑śmierci, na przykład kaspazę‑3. Ponieważ FAK i CCL5 są także powiązane z migracją komórek nowotworowych i unikaniem odpowiedzi immunologicznej, ich stłumienie pomaga wyjaśnić silne efekty przeciw migracji i proapoptotyczne zaobserwowane w laboratorium. Badania dokowania komputerowego potwierdziły ten obraz, pokazując, że 4c dobrze dopasowuje się do aktywnej kieszeni FAK i nawiązuje wielokrotne stabilizujące kontakty, co jest zgodne z bezpośrednią inhibicją enzymu.
Wczesne sygnały bezpieczeństwa i kolejne kroki
Zanim jakikolwiek kandydat na lek przejdzie do badań klinicznych, trzeba ocenić jego bezpieczeństwo. Zespół podał pojedyncze dawki 4c myszom i obserwował je przez dwa dni. Przy najniższej badanej dawce, 12,5 mg na kilogram masy ciała, zwierzęta nie wykazywały oczywistych objawów niepokoju, a tkanki wątroby i nerek pozostały w dużej mierze nienaruszone w badaniu mikroskopowym. Wyższe dawki zaczęły powodować zauważalne uszkodzenia tkanek i biochemiczne oznaki stresu, co wskazuje, że istotny będzie staranny dobór dawki. Dodatkowe modele komputerowe dotyczące wchłaniania, metabolizmu i toksyczności sugerowały, że 4c ma stosunkowo korzystne właściwości w porównaniu z niektórymi istniejącymi lekami przeciwnowotworowymi, chociaż potencjalne efekty wątrobowe i ryzyko związane z sercem będą wymagać ścisłego monitorowania. 
Co to może znaczyć dla przyszłych terapii
W prostych słowach, praca ta identyfikuje nową małą cząsteczkę, 4c, która jednocześnie może blokować kluczową ścieżkę przeżycia w komórkach potrójnie ujemnego raka piersi i aktywnie skłaniać je do uporządkowanej autodestrukcji, jednocześnie hamując ich zdolność do poruszania się i rozprzestrzeniania. Mimo że badania są wciąż na wczesnym, przedklinicznym etapie i wymaga się wielu dalszych testów w modelach zwierzęcych z guzami oraz długoterminowych badań bezpieczeństwa, 4c stanowi obiecujący wzorzec dla nowej klasy terapii celowanych przeciw jednym z najbardziej wymagających postaci raka piersi.
Cytowanie: Abd El Salam, H.A., Abu-Shahba, N., Ibrahim Fouad, G. et al. New indole-linked 1,2,4-triazole derivatives as dual FAK inhibitors and apoptosis inducers targeting survival and migration in triple-negative breast cancer in-vitro. Sci Rep 16, 13134 (2026). https://doi.org/10.1038/s41598-026-41032-1
Słowa kluczowe: potrójnie ujemny rak piersi, kinaza ognisk adhezji, terapia celowana, apoptoza, inhibitor małocząsteczkowy