Clear Sky Science · zh
植入的纤维蛋白凝胶招募的巨噬细胞促进受损淋巴管再生
为什么受损的引流管很重要
当身体的淋巴管在癌症手术、创伤或感染中受损时,组织中的液体无法正常排出。其结果是淋巴水肿:持续性肿胀、不适以及更高的感染风险,可能持续终生。目前尚无获批药物能可靠修复这些管道。这项研究探讨了一个简单但影响深远的想法:能否用一小块体内自身的凝血材料——纤维蛋白,引导受损的淋巴管生长回去并恢复流动?
为破裂的管道搭建临时桥梁
淋巴系统是一张收集组织中过多液体、脂肪和免疫细胞并将其送回血液循环的管网。较大的“集流”管通过节律性收缩和单向瓣膜主动将淋巴向前泵送。当这些管道被切断或切除(如在癌症治疗中清除淋巴结时常见),剩余段不一定能自行重新连接。作者推测,纤维蛋白——血液凝固时形成的天然支架——可能在被切断的集流管之间充当临时桥梁,给细胞提供可供穿越并通过生长重建连接的结构。 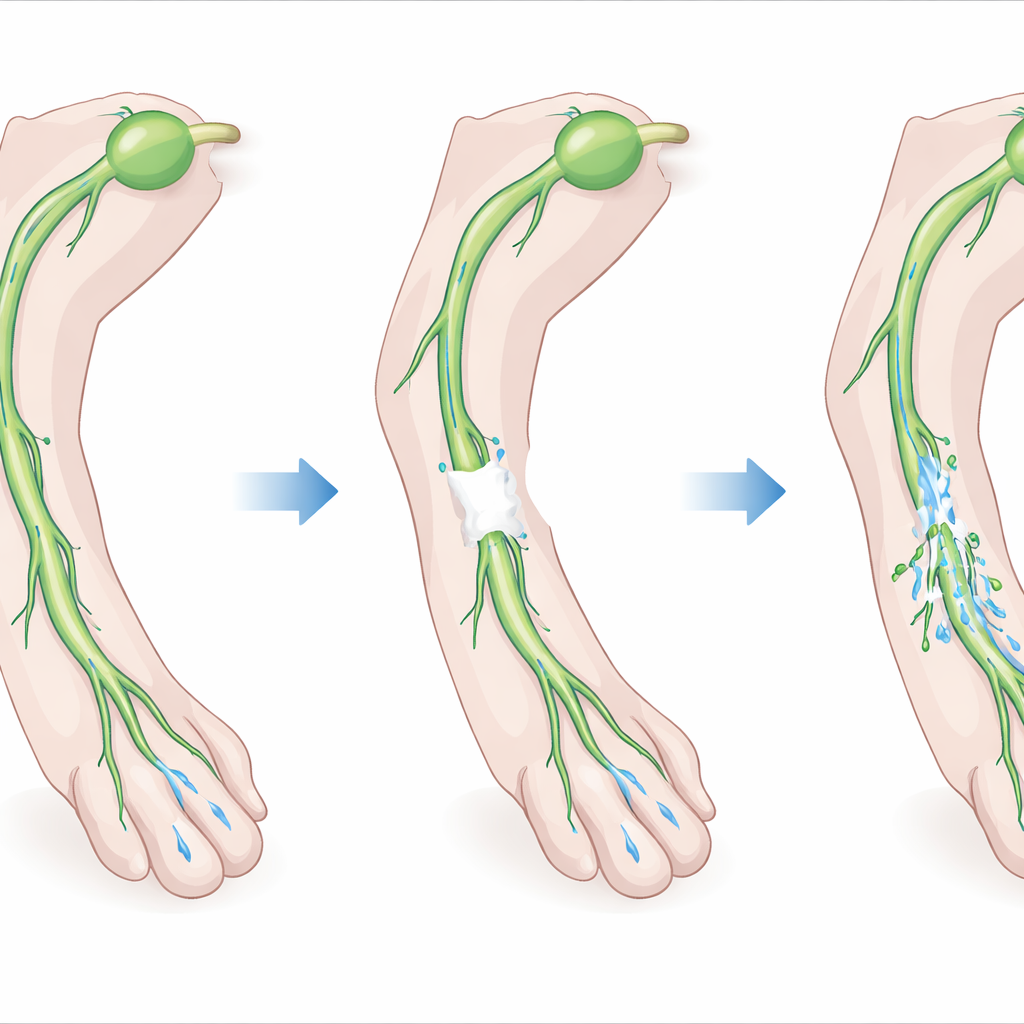
在活体组织中测试凝胶引导
为检验这一想法,研究者首先将小鼠的短段集流淋巴管培养在三维纤维蛋白凝胶中。他们发现,淋巴管向凝胶中伸出许多细长的芽状突起,这些突起由淋巴管内皮细胞及其周围的肌细胞组成。芽状生长的数量和形态高度依赖于纤维蛋白的浓度(即刚度):中等浓度产生最长且最多的突起,而过软或过硬的凝胶都限制了生长。这帮助他们选择出用于动物植入的最佳凝胶配方。
恢复受损腿部的流动
研究团队随后在小鼠后肢制造了可控损伤:切除一段长约1–2毫米的关键集流淋巴管,同时保留附近血管完整。在部分动物中,他们用纤维蛋白凝胶填补了缺口;在另一些动物中则未填充。通过近红外成像追踪注入爪部的荧光染料,他们显示出在未使用凝胶的情况下,淋巴流向主要集中过滤淋巴结的大部分快速无法恢复。而在使用凝胶的情况下,新生的淋巴芽从切端向凝胶内及通过凝胶生长,在数周内重新连接断裂段。损伤上游的泵动活性恢复,染料再次到达原来的引流淋巴结,尽管部分流动仍走替代路线——这既是修复的证据,也表明存在改道。
免疫助力与关键信号分子
纤维蛋白堵塞物不仅提供了结构:它们还吸引了免疫细胞。流式细胞术和显微镜观察显示,巨噬细胞(以及在较小程度上中性粒细胞)在围绕再生血管的凝胶中聚集。当研究者利用载有氯化柔比妥的颗粒在局部耗竭巨噬细胞并功能性禁用中性粒细胞时,淋巴芽生长和泵动恢复基本被抑制,凸显了这些细胞的重要性。组织信号蛋白的筛查显示,一种趋化因子CCL5在损伤并植入凝胶后显著上升。缺乏CCL5的小鼠在损伤上游恢复适当充盈的可能性显著降低,且早期泵动活性减少,尽管免疫细胞仍能进入该区域。这表明CCL5有助于调控这些细胞如何支持修复,而不仅仅是决定它们是否到达。
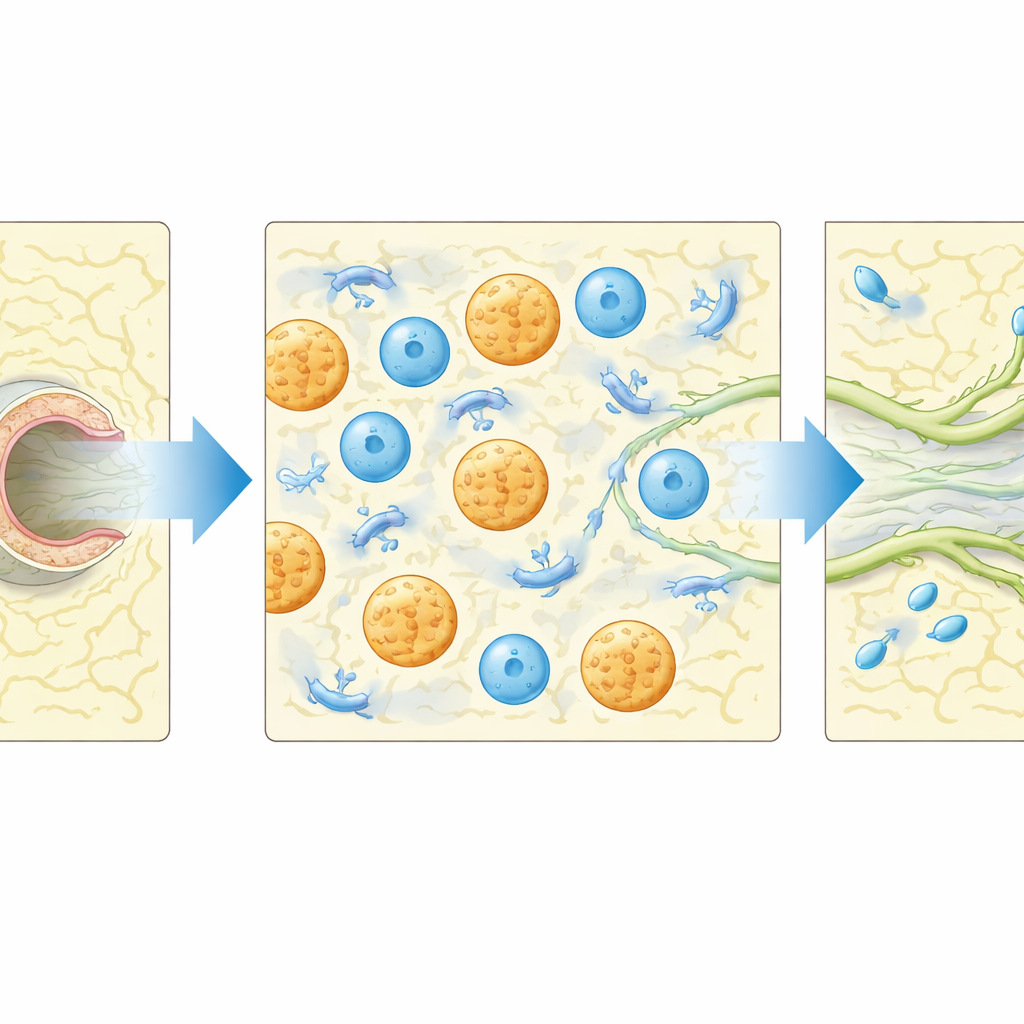
这对肿胀患者可能意味着什么
总体而言,该研究表明,精心调控的纤维蛋白凝胶可以作为受损淋巴管的引导修复工具,使其能够发芽、重新连接并恢复将液体泵送到正确淋巴结的功能。该工作还强调了机体自身的清道夫——巨噬细胞和中性粒细胞——以及信号分子CCL5在这一再生过程中的核心作用。尽管小鼠模型并不能完全模拟人类淋巴水肿,这些结果指明了未来治疗的方向:将生物材料支架与针对性的免疫信号调控相结合,以促进手术或损伤后的持久淋巴修复。
引用: Razavi, M.S., Lei, PJ., Amoozgar, Z. et al. Macrophages recruited by implanted fibrin gels promote regeneration of injured lymphatic vessels. Sci Rep 16, 14337 (2026). https://doi.org/10.1038/s41598-026-39167-2
关键词: 淋巴水肿, 淋巴再生, 纤维蛋白水凝胶, 巨噬细胞, 组织修复