Clear Sky Science · fr
Les macrophages recrutés par des gels de fibrine implantés favorisent la régénération des vaisseaux lymphatiques endommagés
Pourquoi les vaisseaux de drainage endommagés comptent
Lorsque les vaisseaux lymphatiques du corps sont endommagés lors d’une chirurgie contre le cancer, d’un traumatisme ou d’une infection, le liquide ne peut plus s’évacuer correctement des tissus. Le résultat est le lymphœdème : un gonflement chronique, une gêne et un risque accru d’infection qui peuvent durer toute la vie. À ce jour, il n’existe aucun médicament approuvé qui répare de manière fiable ces vaisseaux. Cette étude explore une idée simple aux grandes implications : un minuscule bouchon du propre matériau de coagulation du corps, la fibrine, peut‑il guider la repousse des vaisseaux lymphatiques endommagés et rétablir le flux ?
Construire un pont temporaire pour des tuyaux cassés
Le système lymphatique est un réseau de vaisseaux qui recueille l’excès de liquide, les graisses et les cellules immunitaires des tissus et les renvoie dans la circulation sanguine. Les gros vaisseaux « collecteurs » propulsent activement la lymphe vers l’avant grâce à des contractions rythmiques et des valves unidirectionnelles. Lorsque ces vaisseaux sont sectionnés ou retirés, comme c’est souvent le cas lors d’ablation de ganglions lymphatiques en oncologie, les segments restants ne se reconnectent pas toujours spontanément. Les auteurs ont émis l’hypothèse que la fibrine, l’échafaudage naturel formé lors de la coagulation sanguine, pourrait servir de pont temporaire à travers un intervalle dans un vaisseau collecteur sectionné, offrant aux cellules une structure à travers laquelle pousser pour reconstruire la connexion. 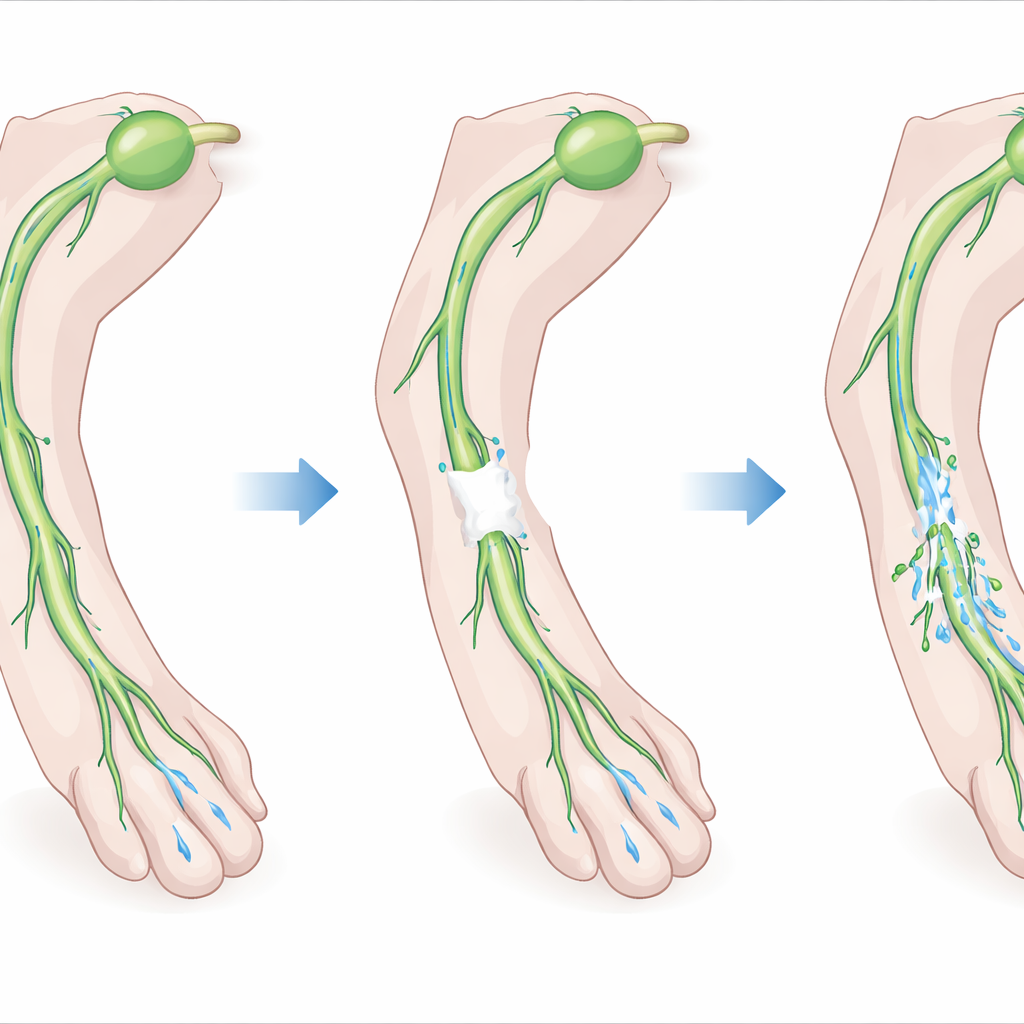
Tester un gel guide dans un tissu vivant
Pour tester cette idée, les chercheurs ont d’abord cultivé de courts segments de vaisseaux lymphatiques collecteurs de souris à l’intérieur de gels de fibrine tridimensionnels. Ils ont observé que les vaisseaux émettaient de nombreux fins bourgeons dans le gel, composés à la fois des cellules de la paroi des vaisseaux lymphatiques et de leurs cellules musculaires environnantes. La quantité et le motif du bourgeonnement dépendaient fortement de la concentration — et donc de la rigidité — de la fibrine : une concentration intermédiaire produisait les bourgeons les plus longs et les plus nombreux, tandis que des gels trop mous ou trop raides limitaient la croissance. Cela les a aidés à choisir une formulation optimale de gel à implanter chez les animaux.
Rétablir le flux dans des pattes lésées
L’équipe a ensuite réalisé une lésion contrôlée dans les membres postérieurs de souris en retirant un segment de 1 à 2 millimètres d’un vaisseau lymphatique collecteur clé, tout en laissant les vaisseaux sanguins voisins intacts. Chez certains animaux, ils ont comblé l’intervalle avec le gel de fibrine ; chez d’autres, ils ne l’ont pas fait. En utilisant l’imagerie proche infrarouge pour suivre un colorant fluorescent injecté dans la patte, ils ont montré que, sans gel, le flux lymphatique vers le ganglion lymphatique collecteur principal ne se rétablissait en grande partie pas. Avec le gel, de nouveaux bourgeons lymphatiques ont poussé depuis les extrémités sectionnées du vaisseau dans et à travers le gel, reconnectant les segments cassés en quelques semaines. L’activité de pompage en amont de la lésion est revenue, et le colorant a de nouveau atteint le ganglion lymphatique collecteur d’origine, bien que certains flux empruntent encore des voies alternatives — preuve à la fois de réparation et de dérivation.
Aides immunitaires et une molécule de signal clé
Les bouchons de fibrine ont fait plus que fournir une structure : ils ont aussi attiré des cellules immunitaires. La cytométrie en flux et la microscopie ont révélé que des macrophages, et dans une moindre mesure des neutrophiles, s’accumulaient dans le gel autour des vaisseaux en régénération. Lorsque les chercheurs ont localement déplété les macrophages et rendu les neutrophiles non fonctionnels à l’aide de particules chargées de clodronate, le bourgeonnement lymphatique et le retour du pompage ont été en grande partie supprimés, soulignant l’importance de ces cellules. Un inventaire des protéines de signalisation tissulaire a montré qu’une molécule, la chimiokine CCL5, augmentait fortement après la lésion associée à l’implantation du gel. Les souris dépourvues de CCL5 étaient significativement moins susceptibles de retrouver un remplissage correct du vaisseau en amont de la lésion, et leur activité de pompage précoce était réduite, même si les cellules immunitaires pouvaient toujours pénétrer dans la zone. Cela suggère que CCL5 aide à réguler la manière dont ces cellules soutiennent la réparation, pas seulement leur arrivée. 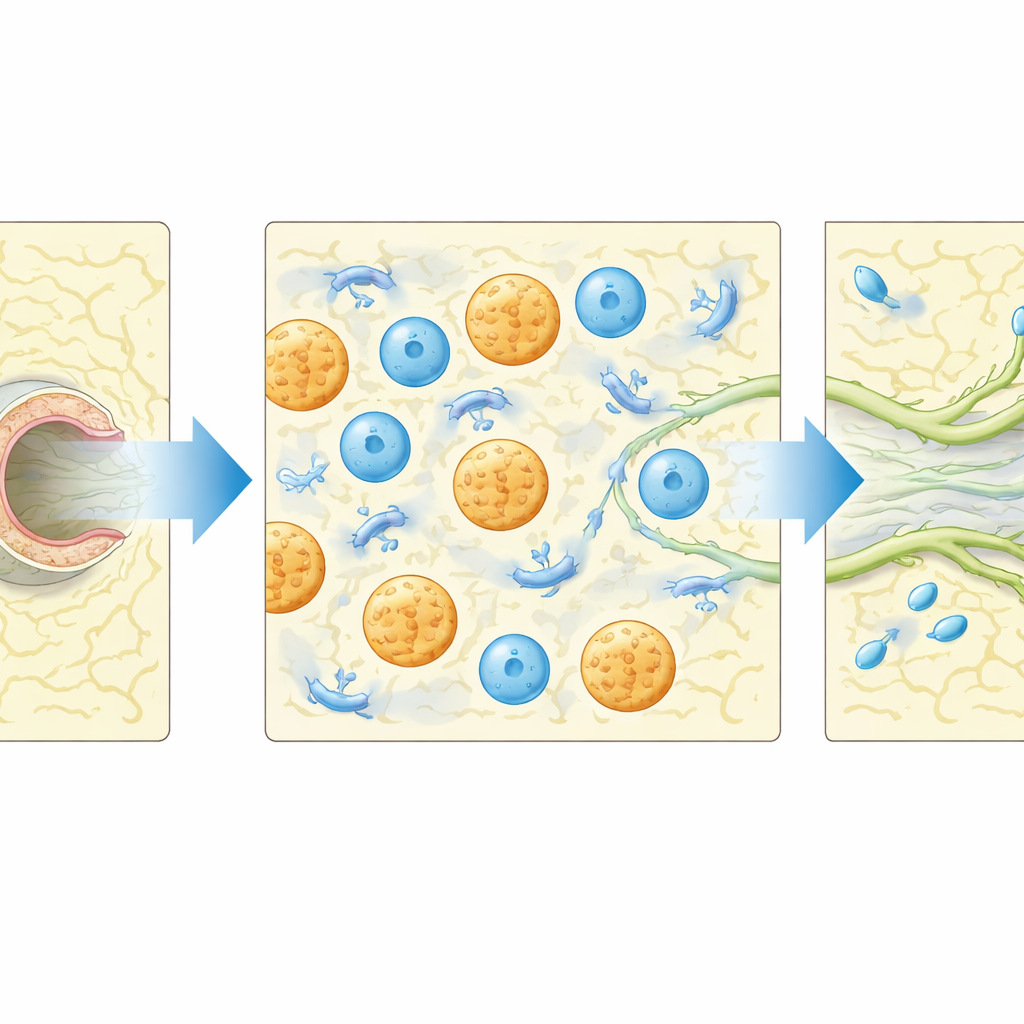
Ce que cela pourrait signifier pour les personnes atteintes de gonflement
Globalement, l’étude montre qu’un gel de fibrine finement ajusté peut agir comme une trousse de réparation guidée pour les vaisseaux lymphatiques endommagés, leur permettant de bourgeonner, de se reconnecter et de reprendre la pompe du liquide vers le ganglion lymphatique approprié. Les travaux soulignent également que l’équipe de nettoyage naturelle du corps — macrophages et neutrophiles — et la molécule de signalisation CCL5 sont centrales dans ce processus de repousse. Bien que le modèle murin ne reproduise pas entièrement le lymphœdème humain, ces résultats ouvrent la voie à des traitements futurs combinant des échafaudages de biomatériaux et un contrôle ciblé des signaux immunitaires pour favoriser une réparation lymphatique durable après chirurgie ou blessure.
Citation: Razavi, M.S., Lei, PJ., Amoozgar, Z. et al. Macrophages recruited by implanted fibrin gels promote regeneration of injured lymphatic vessels. Sci Rep 16, 14337 (2026). https://doi.org/10.1038/s41598-026-39167-2
Mots-clés: lymphœdème, régénération lymphatique, hydrogel de fibrine, macrophages, réparation tissulaire