Clear Sky Science · nl
Macrofagen die door geïmplanteerde fibrinegels worden aangetrokken bevorderen regeneratie van beschadigde lymfevaten
Waarom beschadigde drainagevaten ertoe doen
Wanneer de lymfevaten van het lichaam beschadigd raken tijdens kankeroperaties, trauma of infectie, kan vocht niet langer goed uit weefsels worden afgevoerd. Het gevolg is lymfoedeem: chronische zwelling, ongemak en een verhoogd infectierisico die een leven lang kunnen aanhouden. Tegenwoordig is er geen goedgekeurd geneesmiddel dat deze vaten betrouwbaar herstelt. Deze studie onderzoekt een eenvoudig idee met grote implicaties: kan een klein plugje van het eigen stolingsmateriaal van het lichaam, fibrine, beschadigde lymfevaten begeleiden om terug te groeien en de stroom te herstellen?
Een tijdelijke brug bouwen voor kapotte leidingen
Het lymfestelsel is een netwerk van vaten dat overtollig vocht, vetten en immuuncellen uit weefsels verzamelt en terugvoert naar de bloedbaan. Grotere “verzamelende” vaten pompen lymfe actief vooruit met ritmische contracties en eenrichtingskleppen. Wanneer deze vaten worden doorgesneden of verwijderd, zoals vaak gebeurt bij het weghalen van lymfeklieren tijdens kankerbehandelingen, verbinden de overgebleven segmenten zich niet altijd vanzelf weer. De auteurs redeneerden dat fibrine, het natuurlijke netwerk dat tijdens de bloedstolling ontstaat, zou kunnen fungeren als een tijdelijke brug over een kloof in een doorgesneden verzamelvat, en zo cellen een structuur bieden om doorheen te groeien terwijl ze de verbinding herbouwen. 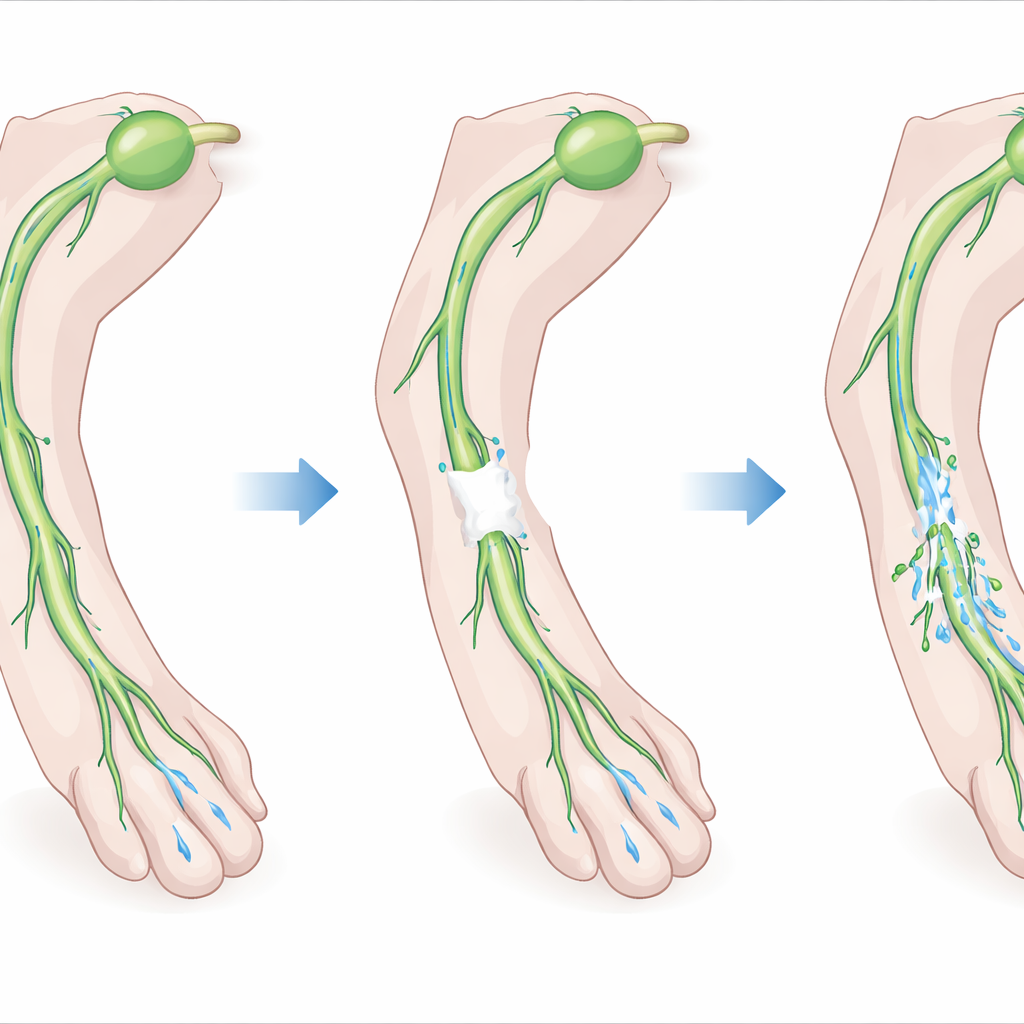
Een gelgids testen in levend weefsel
Om dit idee te testen, kweekten de onderzoekers eerst korte segmenten van muizenverzamelende lymfevaten in driedimensionale fibrinegels. Ze vonden dat de vaten veel dunne uitlopers in de gel stuurden, bestaande uit zowel de bekledende cellen van lymfevaten als hun omliggende spiercellen. De hoeveelheid en het patroon van uitgroei hing sterk af van de concentratie, en daarmee de stijfheid, van de fibrine: een gemiddelde concentratie produceerde de langste en talrijkste uitlopers, terwijl gels die te zacht of te stijf waren de groei beperkten. Dit hielp hen een optimale gelformulering te kiezen om in dieren te implanteren.
Stroom herstellen in beschadigde poten
Het team veroorzaakte vervolgens een gecontroleerde verwonding in de achterpoten van muizen door een segment van 1–2 millimeter van een belangrijk verzamelend lymfevat te verwijderen, terwijl nabijgelegen bloedvaten intact werden gelaten. Bij sommige dieren vulden ze de kloof met de fibrinegel; bij anderen deden ze dat niet. Met behulp van nabij-infrarood beeldvorming om een fluorescerende kleurstof geïnjecteerd in de poot te volgen, toonden ze aan dat zonder gel de lymfestroom naar de belangrijkste afvoerende lymfeklier grotendeels niet herstelde. Met gel groeiden nieuwe lymfeuitlopers vanuit de afgesneden uiteinden van het vat in en door de gel, en werden de gebroken segmenten binnen enkele weken opnieuw verbonden. De pompfunctie stroomopwaarts van de verwonding keerde terug en de kleurstof bereikte opnieuw de oorspronkelijke afvoerende lymfeklier, hoewel een deel van de stroom alternatieve routes volgde—bewijs van zowel herstel als omleiding.
Immuunhelpers en een sleutelsignaalmolecuul
De fibrinepluggen deden meer dan alleen structuur bieden: ze trokken ook immuuncellen aan. Flowcytometrie en microscopie toonden aan dat macrofagen, en in mindere mate neutrofielen, zich in de gel rondom regenererende vaten ophoopten. Toen de onderzoekers lokaal macrofagen uitputten en neutrofielen functioneel uitschakelden met clodronaatgeladen deeltjes, werden lymfeuitgroei en het herstel van pompfunctie grotendeels uitgeschakeld, wat het belang van deze cellen onderstreepte. Een overzicht van weefselsignalerende eiwitten liet zien dat één molecuul, het chemokine CCL5, sterk toenam na verwonding plus gimplantatie. Muizen zonder CCL5 herstelden aanzienlijk minder vaak de juiste vulling van het vat stroomopwaarts van de verwonding, en hun vroege pompactiviteit was verminderd, ook al konden immuuncellen nog steeds het gebied binnendringen. Dit suggereert dat CCL5 helpt regelen hoe deze cellen het herstel ondersteunen, en niet alleen of ze arriveren. 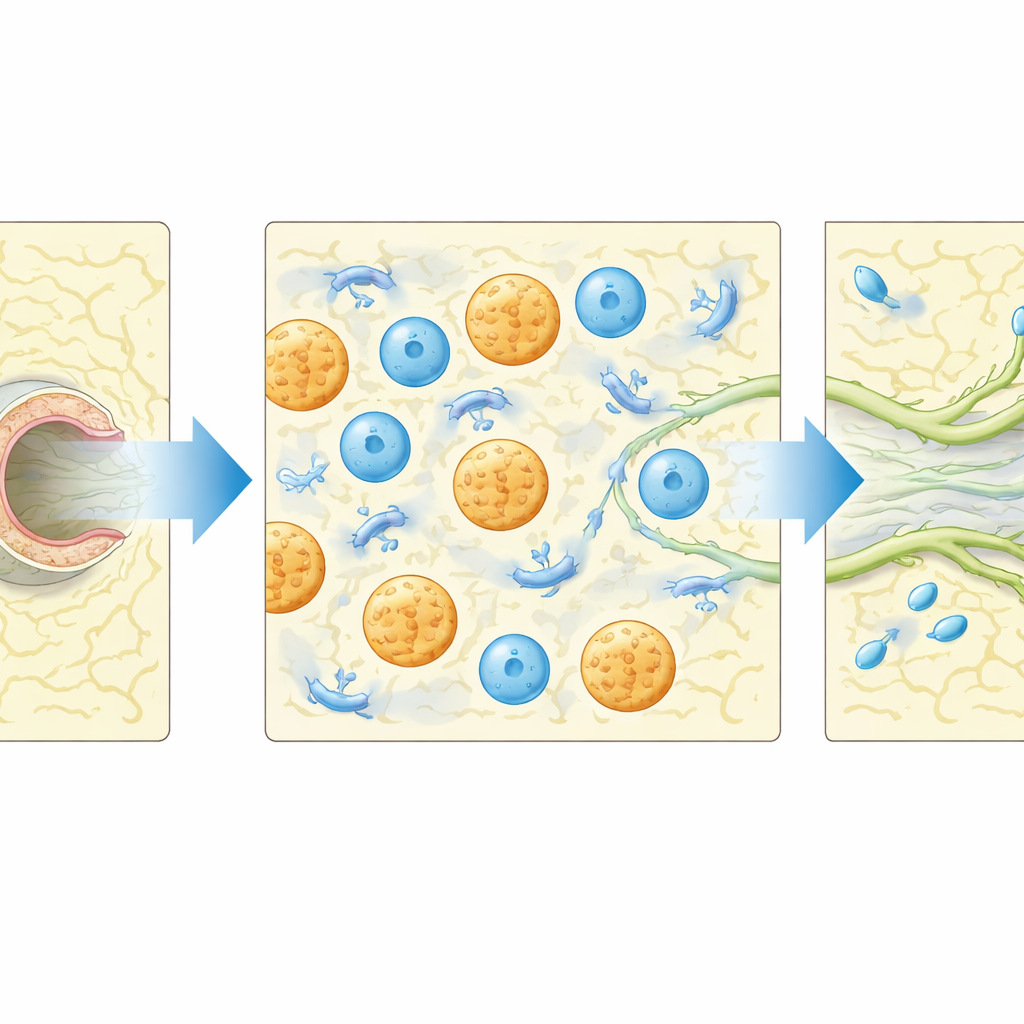
Wat dit kan betekenen voor mensen met zwelling
Al met al laat de studie zien dat een zorgvuldig afgestemde fibrinegel kan fungeren als een geleide reparatieset voor beschadigde lymfevaten, waardoor ze kunnen uitgroeien, opnieuw verbinden en het pompen van vocht naar de juiste lymfeklier kunnen hervatten. Het werk benadrukt ook dat het eigen opruimteam van het lichaam—macrofagen en neutrofielen—en het signaalmolecuul CCL5 centraal staan in dit hergroeiproces. Hoewel het muismodel niet volledig het menselijke lymfoedeem nabootst, wijzen deze resultaten op toekomstige behandelingen die biomaterialen combineren met gerichte aansturing van immuunsignalen om duurzaam herstel van lymfevaten na chirurgie of letsel te bevorderen.
Bronvermelding: Razavi, M.S., Lei, PJ., Amoozgar, Z. et al. Macrophages recruited by implanted fibrin gels promote regeneration of injured lymphatic vessels. Sci Rep 16, 14337 (2026). https://doi.org/10.1038/s41598-026-39167-2
Trefwoorden: lymfoedeem, lymfatische regeneratie, fibrine-hydrogel, macrofagen, weefselherstel