Clear Sky Science · de
Von implantierten Fibrin-Gelen angeworbene Makrophagen fördern die Regeneration verletzter Lymphgefäße
Warum beschädigte Drainagegefäße zählen
Wenn die lymphatischen Gefäße des Körpers bei Krebsoperationen, Verletzungen oder Infektionen beschädigt werden, kann Flüssigkeit nicht mehr richtig aus dem Gewebe abfließen. Das Ergebnis ist ein Lymphödem: chronische Schwellung, Unbehagen und ein dauerhaft erhöhtes Infektionsrisiko. Bisher gibt es kein zugelassenes Medikament, das diese Gefäße zuverlässig repariert. Diese Studie untersucht eine einfache Idee mit großen Folgen: Kann ein winziger Pfropf aus dem körpereigenen Blutgerinnungsmaterial Fibrin beschädigte Lymphgefäße dazu anleiten, wieder zu wachsen und den Fluss wiederherzustellen?
Eine temporäre Brücke für gebrochene Leitungen bauen
Das Lymphsystem ist ein Netzwerk von Gefäßen, das überschüssige Flüssigkeit, Fette und Immunzellen aus dem Gewebe aufnimmt und zurück in den Blutkreislauf führt. Größere „sammelnde“ Gefäße pumpen die Lymphe aktiv vorwärts mithilfe rhythmischer Kontraktionen und Einwegklappen. Werden diese Gefäße durchtrennt oder entfernt, wie das oft beim Entfernen von Lymphknoten während einer Krebstherapie der Fall ist, verbinden sich die verbleibenden Segmente nicht immer von selbst wieder. Die Autorinnen und Autoren vermuteten, dass Fibrin, das natürliche Gerüst, das sich bei der Blutgerinnung bildet, als temporäre Brücke über eine Lücke in einem durchtrennten Sammelgefäß wirken könnte und den Zellen etwas bieten würde, durch das sie wachsen können, während sie die Verbindung wiederherstellen. 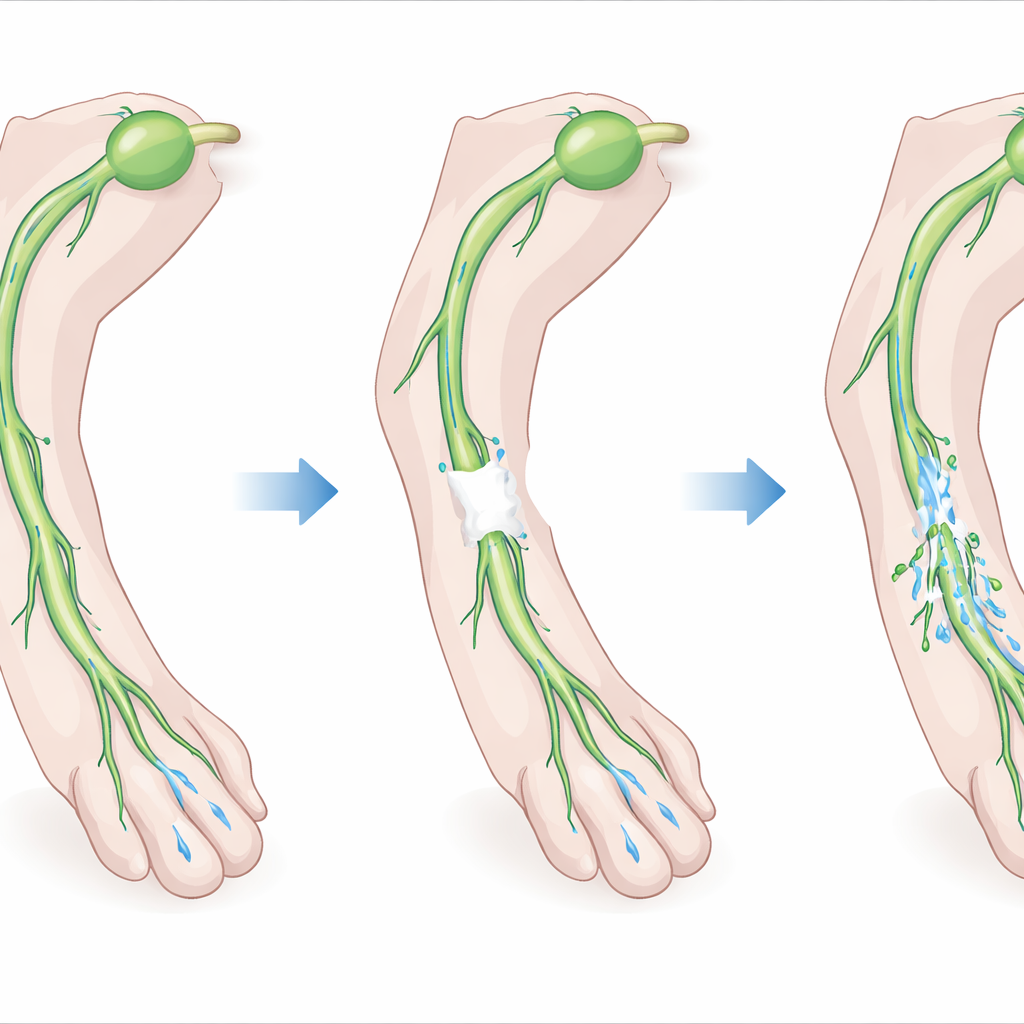
Ein Gel-Leitfaden im lebenden Gewebe testen
Um diese Idee zu prüfen, kultivierten die Forschenden zunächst kurze Abschnitte von Maus-Sammellymphgefäßen in dreidimensionalen Fibrin-Gelen. Sie fanden heraus, dass die Gefäße viele dünne Ausläufer in das Gel aussendeten, die sowohl aus den Auskleidungszellen der Lymphgefäße als auch aus den umgebenden Muskelzellen bestanden. Menge und Muster der Auswüchse hingen stark von der Konzentration und damit von der Steifigkeit des Fibrins ab: Eine mittlere Konzentration erzeugte die längsten und zahlreichsten Ausläufer, während zu weiche oder zu steife Gele das Wachstum einschränkten. Das half ihnen, eine optimale Gel-Formulierung für die Implantation in Tieren auszuwählen.
Den Fluss in verletzten Beinen wiederherstellen
Das Team erzeugte dann eine kontrollierte Verletzung an den Hinterbeinen von Mäusen, indem es ein 1–2 Millimeter langes Segment eines wichtigen Sammel-lymphgefäßes entfernte, während nahegelegene Blutgefäße intakt blieben. In einigen Tieren füllten sie die Lücke mit dem Fibrin-Gel; in anderen taten sie das nicht. Mithilfe von nahinfraroter Bildgebung, um einen in die Pfote injizierten Fluoreszenzfarbstoff zu verfolgen, zeigten sie, dass ohne Gel der Lymphfluss zum hauptsächlichen drainierenden Lymphknoten weitgehend nicht wiederhergestellt wurde. Mit Gel wuchsen neue lymphatische Ausläufer aus den durchtrennten Enden des Gefäßes in das Gel hinein und durch das Gel hindurch und verbanden die gebrochenen Segmente innerhalb weniger Wochen wieder. Die Pumpaktivität stromaufwärts der Verletzung kehrte zurück, und der Farbstoff erreichte wieder den ursprünglichen drainierenden Lymphknoten, obwohl ein Teil des Flusses weiterhin alternative Routen nahm — ein Hinweis auf sowohl Reparatur als auch Umleitungen.
Immunhelfer und ein zentrales Signalmolekül
Die Fibrinpfropfen leisteten mehr als nur Struktur: Sie zogen auch Immunzellen an. Durch Durchflusszytometrie und Mikroskopie zeigte sich, dass Makrophagen und in geringerem Maße Neutrophile sich im Gel um die regenerierenden Gefäße ansammelten. Als die Forschenden lokal Makrophagen entfernten und Neutrophile funktionell mit clodronatbeladenen Partikeln deaktivierten, gingen die lymphatische Aussprossung und die Rückkehr der Pumpfunktion größtenteils verloren, was die Bedeutung dieser Zellen unterstreicht. Eine Übersicht über Gewebesignalmoleküle zeigte, dass ein Molekül, der Chemokin CCL5, nach Verletzung und Gel-Implantation stark anstieg. Mäuse ohne CCL5 erlangten deutlich seltener eine normale Füllung des Gefäßes stromaufwärts der Verletzung zurück, und ihre frühe Pumpaktivität war reduziert, obwohl Immunzellen weiterhin in das Gebiet eindringen konnten. Das legt nahe, dass CCL5 steuert, wie diese Zellen die Reparatur unterstützen, nicht nur, ob sie ankommen. 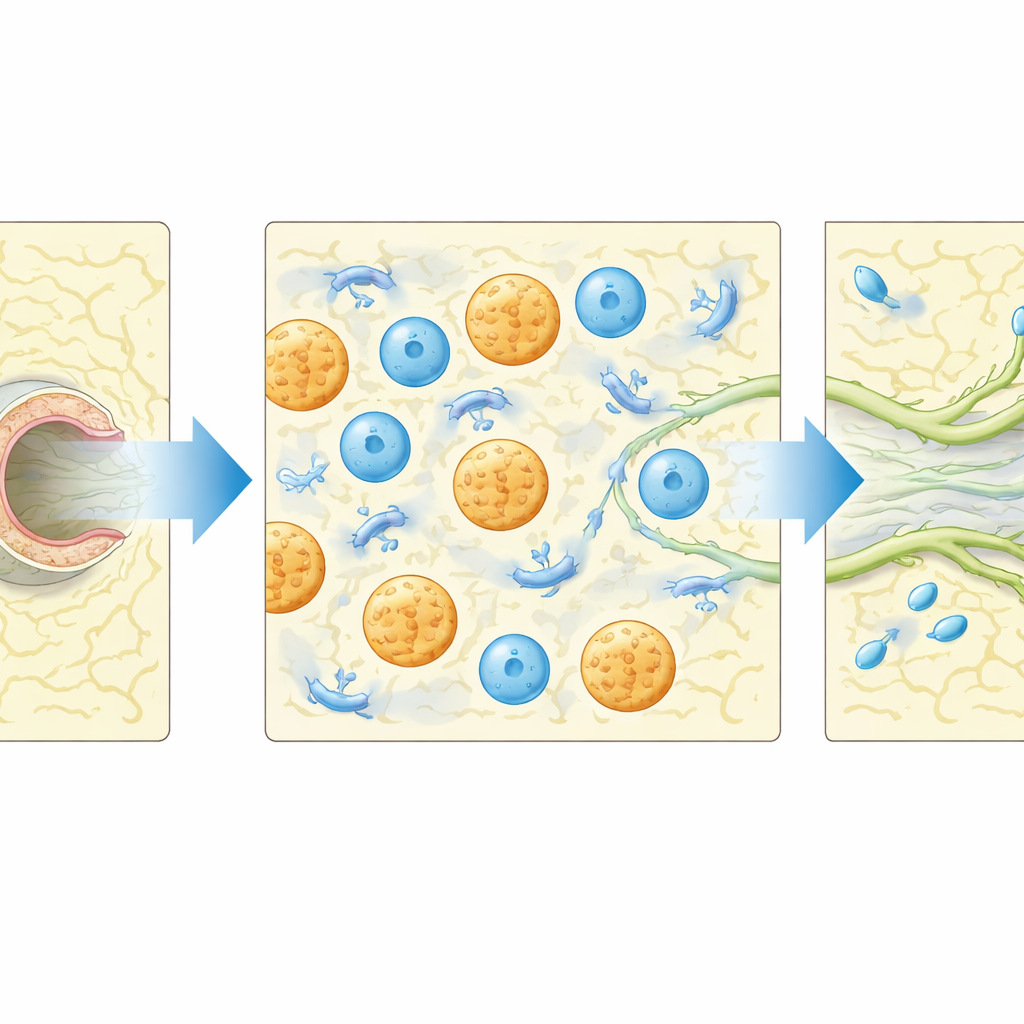
Was das für Menschen mit Schwellungen bedeuten könnte
Insgesamt zeigt die Studie, dass ein sorgfältig abgestimmtes Fibrin-Gel als geführtes Reparaturset für beschädigte Lymphgefäße dienen kann, indem es ihnen ermöglicht, auszutreiben, sich wieder zu verbinden und das Pumpen der Flüssigkeit zum richtigen Lymphknoten wieder aufzunehmen. Die Arbeit betont auch, dass die körpereigene Aufräumtruppe — Makrophagen und Neutrophile — sowie das Signalmolekül CCL5 zentral für diesen Nachwachsprozess sind. Zwar bildet das Mausmodell das menschliche Lymphödem nicht vollständig ab, doch deuten diese Ergebnisse auf mögliche künftige Therapien hin, die Biomaterial-Gerüste mit gezielter Steuerung von Immun-signalen kombinieren, um eine dauerhafte lymphatische Reparatur nach Operationen oder Verletzungen zu fördern.
Zitation: Razavi, M.S., Lei, PJ., Amoozgar, Z. et al. Macrophages recruited by implanted fibrin gels promote regeneration of injured lymphatic vessels. Sci Rep 16, 14337 (2026). https://doi.org/10.1038/s41598-026-39167-2
Schlüsselwörter: Lymphödem, lymphatische Regeneration, Fibrin-Hydrogel, Makrophagen, Gewebereparatur