Clear Sky Science · es
Macrófagos reclutados por geles de fibrina implantados promueven la regeneración de los vasos linfáticos lesionados
Por qué importan los vasos de drenaje dañados
Cuando los vasos linfáticos del cuerpo se lesionan durante una cirugía oncológica, un traumatismo o una infección, el líquido ya no puede drenarse correctamente de los tejidos. El resultado es el linfedema: hinchazón crónica, molestias y un mayor riesgo de infección que pueden perdurar de por vida. Hoy no existe un fármaco aprobado que repare de forma fiable estos vasos. Este estudio explora una idea sencilla con grandes implicaciones: ¿puede un pequeño tapón del propio material de coagulación del cuerpo, la fibrina, orientar a los vasos linfáticos dañados para que vuelvan a crecer y restauren el flujo?
Construir un puente temporal para tuberías rotas
El sistema linfático es una red de vasos que recoge el exceso de líquido, grasas y células inmunitarias de los tejidos y los devuelve al torrente sanguíneo. Los vasos “colectores” más grandes bombean activamente la linfa hacia adelante mediante contracciones rítmicas y válvulas unidireccionales. Cuando estos vasos se cortan o extirpan, como ocurre con frecuencia cuando se quitan ganglios linfáticos durante el tratamiento del cáncer, los segmentos restantes no siempre se reconectan por sí mismos. Los autores plantearon que la fibrina, la estructura natural que se forma durante la coagulación de la sangre, podría actuar como un puente temporal a través de una brecha en un vaso colector seccionado, ofreciendo a las células un andamiaje por el que crecer mientras reconstruyen la conexión. 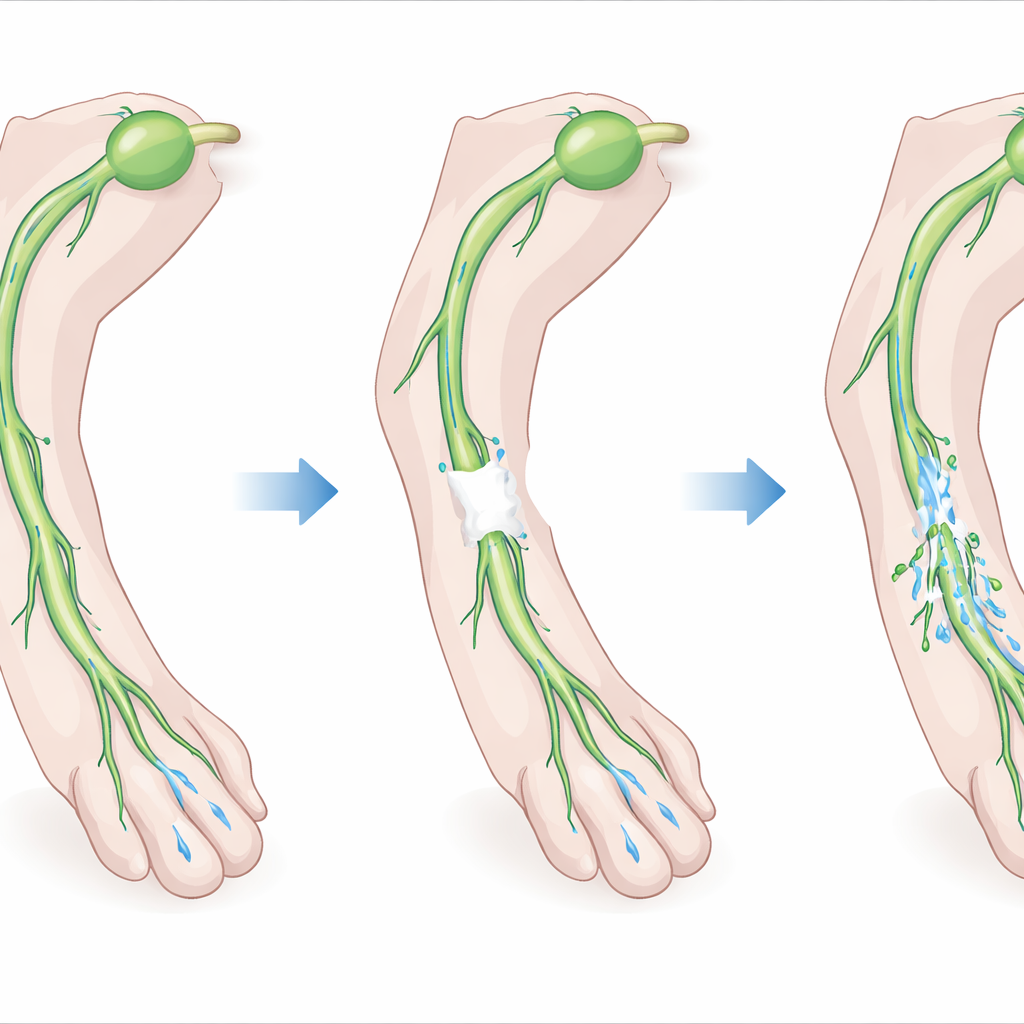
Probar una guía de gel en tejido vivo
Para poner a prueba esta idea, los investigadores primero cultivaron segmentos cortos de vasos linfáticos colectores de ratón dentro de geles tridimensionales de fibrina. Observaron que los vasos emitían numerosos brotes delgados en el gel, formados tanto por las células que recubren los vasos linfáticos como por sus células musculares periféricas. La cantidad y el patrón de brotación dependieron fuertemente de la concentración, y por tanto de la rigidez, de la fibrina: una concentración intermedia produjo los brotes más largos y numerosos, mientras que los geles demasiado blandos o demasiado rígidos limitaron el crecimiento. Esto les permitió elegir una formulación óptima de gel para implantar en animales.
Restaurar el flujo en patas lesionadas
El equipo creó entonces una lesión controlada en las extremidades posteriores de ratones eliminando un segmento de 1–2 milímetros de un vaso linfático colector clave, dejando intactos los vasos sanguíneos cercanos. En algunos animales llenaron la brecha con el gel de fibrina; en otros no lo hicieron. Mediante imagen en el infrarrojo cercano para seguir un tinte fluorescente inyectado en la pata, mostraron que, sin gel, el flujo linfático hacia el ganglio linfático colector principal no se recuperó en gran medida. Con el gel, nuevos brotes linfáticos crecieron desde los extremos cortados del vaso dentro y a través del gel, reconectando los segmentos rotos en unas pocas semanas. La actividad de bombeo aguas arriba de la lesión retornó y el tinte volvió a alcanzar el ganglio linfático colector original, aunque parte del flujo todavía tomó rutas alternativas: evidencia tanto de reparación como de desvío.
Auxiliares inmunitarios y una molécula de señal clave
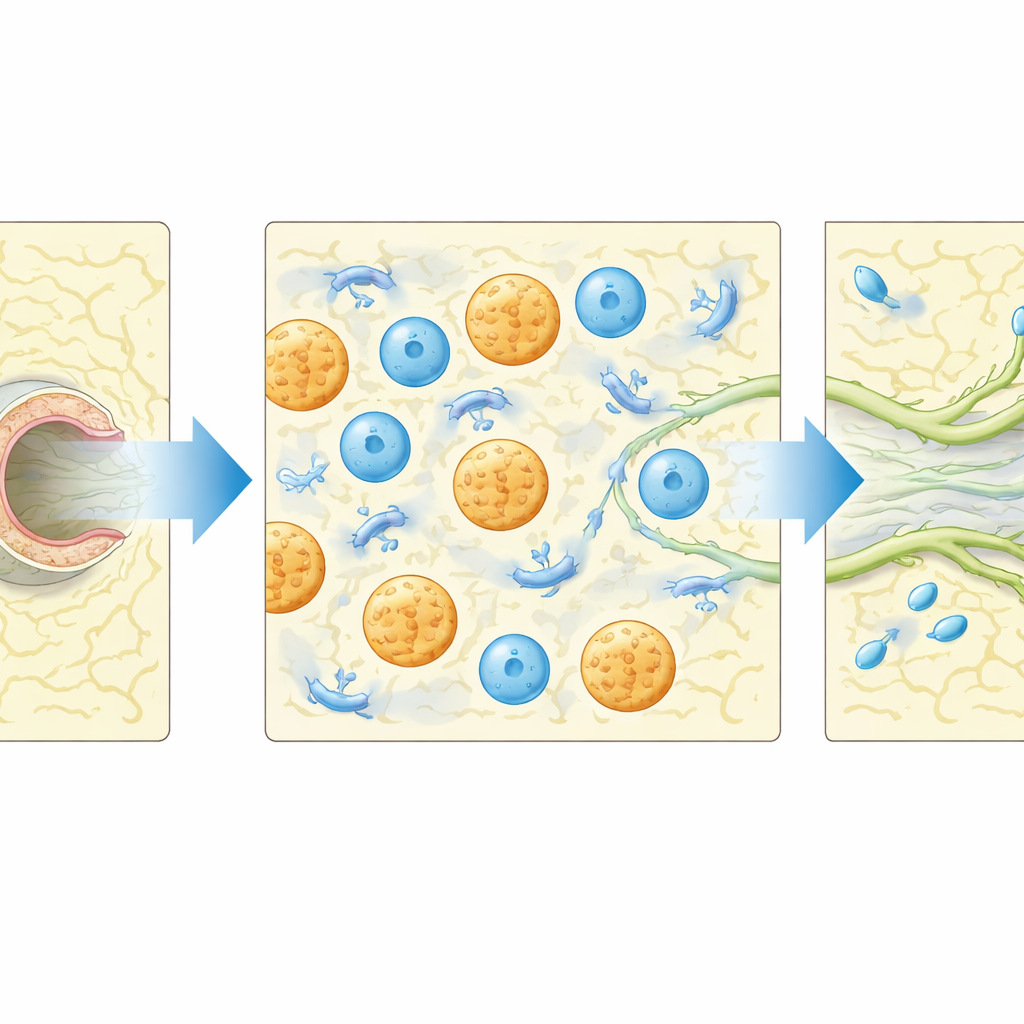
Los tapones de fibrina hicieron más que proporcionar estructura: también atraían células inmunitarias. La citometría de flujo y la microscopía revelaron que macrófagos, y en menor medida neutrófilos, se acumularon en el gel alrededor de los vasos en regeneración. Cuando los investigadores agotaron localmente los macrófagos y desactivaron funcionalmente los neutrófilos usando partículas cargadas con clodronato, la brotación linfática y el retorno del bombeo se vieron en gran parte abolidos, subrayando la importancia de estas células. Un análisis de las proteínas de señalización tisular mostró que una molécula, la quimiocina CCL5, aumentó de forma marcada tras la lesión y la implantación del gel. Los ratones carentes de CCL5 tuvieron una probabilidad significativamente menor de recuperar el llenado adecuado del vaso aguas arriba de la lesión, y su actividad de bombeo temprana se redujo, aunque las células inmunitarias aún podían entrar en la zona. Esto sugiere que CCL5 ayuda a controlar cómo estas células apoyan la reparación, no simplemente si llegan.
Qué podría significar esto para las personas con hinchazón
En conjunto, el estudio muestra que un gel de fibrina cuidadosamente ajustado puede actuar como un kit de reparación guiada para vasos linfáticos dañados, permitiéndoles brotar, reconectarse y reanudar el bombeo de líquido hacia el ganglio linfático correcto. El trabajo también pone de relieve que el propio equipo de limpieza del cuerpo—macrófagos y neutrófilos—y la molécula señal CCL5 son centrales en este proceso de regeneración. Aunque el modelo en ratón no reproduce totalmente el linfedema humano, estos resultados apuntan hacia tratamientos futuros que combinen andamios biomateriales con el control dirigido de señales inmunitarias para favorecer una reparación linfática duradera tras cirugía o lesión.
Cita: Razavi, M.S., Lei, PJ., Amoozgar, Z. et al. Macrophages recruited by implanted fibrin gels promote regeneration of injured lymphatic vessels. Sci Rep 16, 14337 (2026). https://doi.org/10.1038/s41598-026-39167-2
Palabras clave: linfedema, regeneración linfática, hidrogel de fibrina, macrófagos, reparación tisular