Clear Sky Science · zh
心鼻蝠α冠状病毒利用人类CEACAM6进入细胞
为什么蝙蝠病毒与我们息息相关
在COVID-19之后,很多人都在思考下一次大流行可能来自何处。这项研究通过考察生活在蝙蝠体内的不太为人知的冠状病毒,提出了一个简单但关键的问题:其中是否有病毒已经能够进入人类细胞?通过识别这种“预适应”能力的病毒,科学家希望及早发现潜在威胁,从而在疫情爆发之前部署疫苗、药物和监测措施。
在拥挤的病毒宇宙中搜索
α冠状病毒是一个大型病毒群体,大多感染蝙蝠、啮齿动物和家畜,但也有少数已在人类中引起普通感冒。要在实验室中逐一检测所有已知菌株几乎不可能,因此研究人员采用了计算学捷径。他们从2700多条刺突蛋白序列——病毒附着细胞的那一部分——中挑选出40条,最能代表该群体的整体遗传多样性。然后用这些刺突蛋白制成无害的“假病毒”,这些假病毒在成功进入细胞时会发光,从而可以快速检测每种病毒在不同物种中能使用哪些受体。
大多数蝙蝠病毒无法使用我们常见的“门把手”
我们已知的人类冠状病毒,例如引起普通感冒的229E和NL63或SARS-CoV-2,使用一小部分被充分研究的细胞表面分子作为进入点,包括称为ACE2、APN和DPP4的蛋白。当研究组将这40种病毒对多种哺乳动物来源的受体库进行测试时,发现很少有α冠状病毒能够使用这些受体,几乎没有能使用人类版本。这表明在该病毒家族分支中,经典的冠状病毒“门把手”反而是例外。对大多数蝙蝠α冠状病毒来说,必然存在一些其他尚未识别的入胞途径。
一种心鼻蝠病毒找到了新的“人类门把手”
然而有一种病毒脱颖而出。一株名为CcCoV‑KY43的病毒,最初在肯尼亚的心鼻蝠中发现,能够进入两种来源于肺和肠组织的人类细胞系。为弄清其机制,研究人员将该病毒刺突的受体结合域作为诱饵,对759种人类细胞表面蛋白的大型面板进行筛选。出现了三个密切相关的候选者,均来自CEACAM家族——该家族蛋白通常参与细胞粘附,在黏膜表面丰富。后续实验将关键角色缩小到单一成员:CEACAM6。当将通常抵抗感染的人类细胞工程化表达CEACAM6时,这些细胞立即变得可被该蝙蝠病毒刺突感染。阻断或降低CEACAM6表达显著减少了感染量,证实了该蛋白作为病毒“门” 的作用。
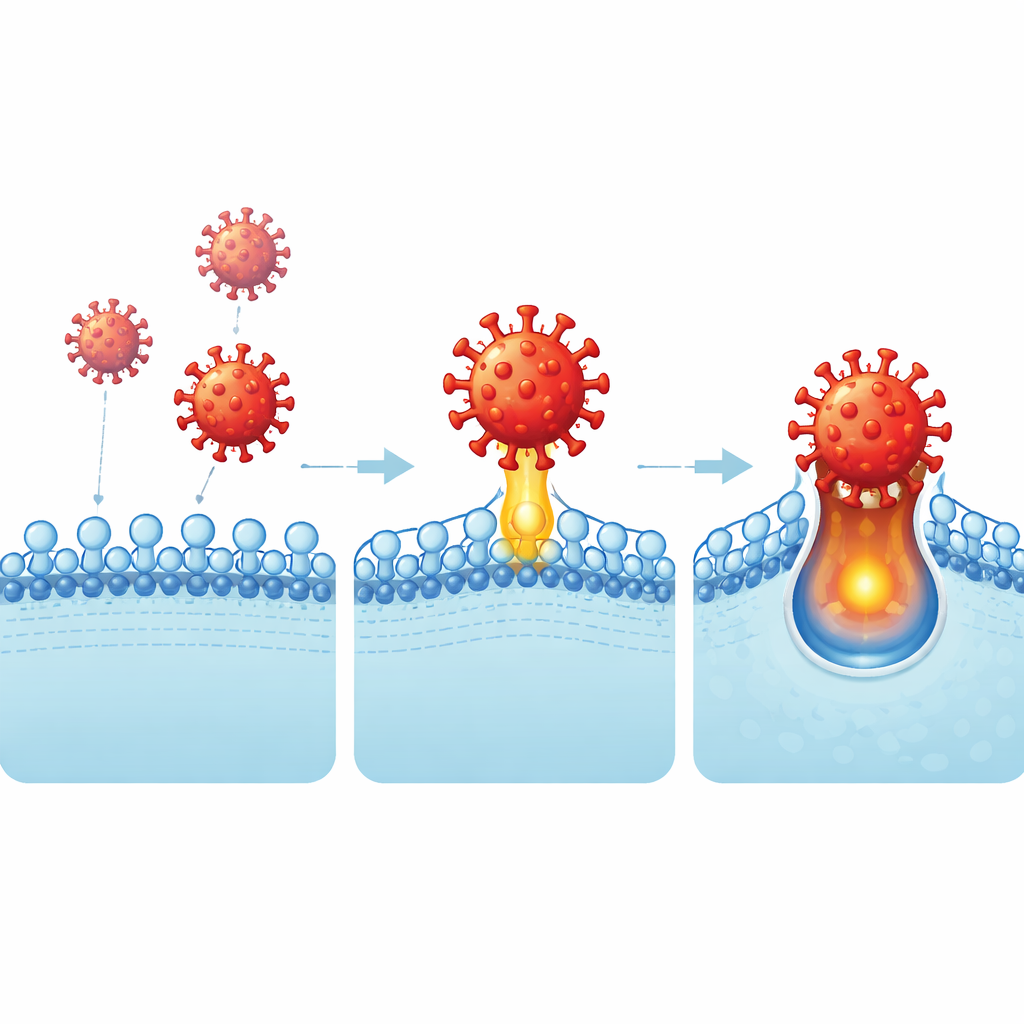
分子结合的样子是什么
为了精确观察这种相互作用,研究团队将蝙蝠病毒的结合域与CEACAM6结晶并解析了其结构。他们发现病毒刺突上的三个微小环状结构扣住了CEACAM6最外层结构的顶端,形成一个由疏水(排斥水)相互作用主导的紧密界面。这正是CEACAM6通常与其配对蛋白接触的区域,表明病毒已进化出模仿或干扰正常细胞间相互作用的策略。界面上仅少数氨基酸的细微变化就足以增强或削弱病毒入侵,这也解释了为何密切相关的CEACAM5结合更弱,不能作为有效受体。
这种危险特性有多普遍?
故事并不止于单一病毒。来自肯尼亚同一蝙蝠物种的另外两种冠状病毒,以及来自中国和俄罗斯铁蹄蝠(horseshoe bats)若干相关病毒,也被发现利用类似CEACAM6的蛋白作为进入通道。有些能够使用人类CEACAM6,有些仅能使用蝙蝠版本,这取决于病毒与宿主序列中微妙的配对细节。通过分析进化树,作者认为利用CEACAM6的能力至少在不同α冠状病毒谱系中独立出现过两次。重要的是,研究者在对数百名居住在肯尼亚蝙蝠栖息地附近人群的血样进行筛查时,仅发现少量针对这些蝙蝠病毒的抗体痕迹,说明目前并无大规模、持续的溢出现象,但不能排除罕见或短暂感染的可能。
这对未来疫情意味着什么
从日常角度看,这项工作表明某些蝙蝠冠状病毒已经具备打开人类肺细胞特定“门”的能力,尽管它们尚未引发被识别的疾病。CEACAM6在人类呼吸道广泛存在,并且似乎被地理分布广泛的一组α冠状病毒使用,尤其是在东非和欧亚部分地区。这种——对我们细胞现成的通路加上野生动物中广泛存在——的组合,使这些病毒成为值得关注的对象。通过确定确切的受体并描绘能够利用它的病毒株,该研究为监测、风险评估以及未来的疫苗或抗病毒药物提供了明确的目标,将大流行准备从猜测转向更系统、基于证据的路径。
引用: Gallo, G., Di Nardo, A., Lugano, D. et al. Heart-nosed bat alphacoronaviruses use human CEACAM6 to enter cells. Nature 653, 180–189 (2026). https://doi.org/10.1038/s41586-026-10394-x
关键词: 蝙蝠冠状病毒, CEACAM6, 人畜共患溢出, 病毒受体, 大流行准备