Clear Sky Science · zh
新辅助帕博昔布联合内分泌治疗与化疗在ER+/HER2-乳腺癌中的比较:一项随机Ⅱ期试验
这项乳腺癌研究为何重要
对于许多激素敏感型乳腺癌患者,首个重大治疗决策是在手术前接受传统化疗还是使用更新的靶向口服药物。化疗可能有效,但常伴随沉重的副作用;而旨在阻断肿瘤生长的口服药物可能更温和,但在这一早期治疗情境中尚未成为常规。本研究提出了一个简单却关键的问题:我们能否安全地用靶向口服药代替化疗,或以不同顺序使用化疗——并且现代肿瘤基因检测能否告诉我们谁真正需要哪种治疗?
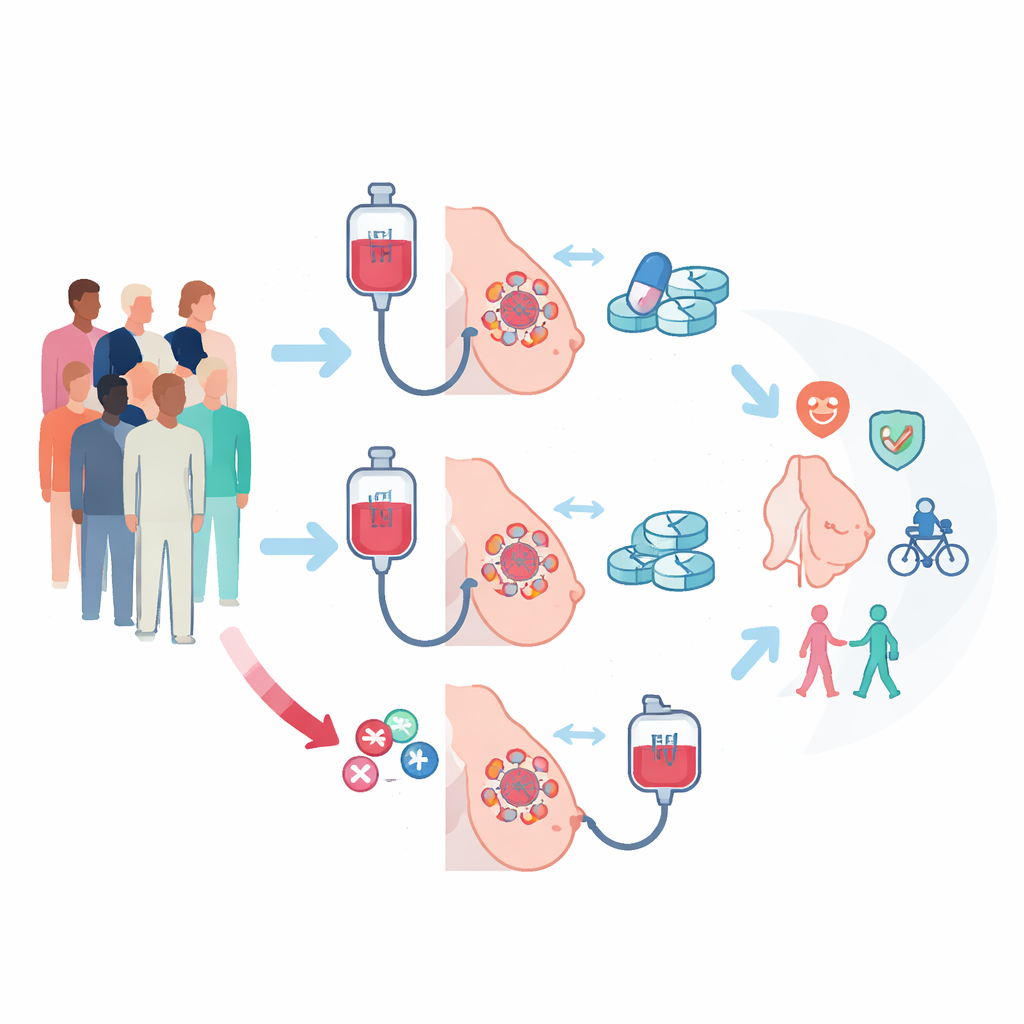
术前的两条不同路径
PREDIX LumB 试验纳入了179名常见的、对雌激素敏感但不出现HER2过表达的乳腺癌患者(ER阳性/HER2阴性)。所有肿瘤体积较大和/或已累及近处淋巴结,因此在手术前缩小肿瘤具有临床意义。参与者被随机分配到两条路径之一。一组先接受标准化疗:每周紫杉醇12周,随后再给予为期12周的口服靶向药帕博昔布联合阻断激素的治疗;另一组顺序相反:先给予帕博昔布加内分泌治疗,然后再进行紫杉醇化疗。经过这24周的术前治疗后,所有人均接受标准手术和按建议的后续治疗。
相似的肿瘤缩小和生存,但日常影响不同
主要指标是前12周后有多少患者在影像学上出现明确的肿瘤缩小。先行化疗的组别有59%的患者出现应答,而先行口服靶向药加内分泌治疗的组别为45%;这一下降未达到研究者通常认为具有统计学显著性的水平。到24周——即所有患者都接受了两种疗法但顺序相反后——两组的应答率都较高且相近。长期结局也大体一致:无事件生存期、术后复发和约四年半随访期内的总生存率无显著差异。副作用方面则表现不同:化疗更常引起手足神经毒性、皮疹和乏力,而帕博昔布常导致白细胞计数下降。患者报告称在口服药物阶段生活质量保持得更好,而在化疗期间下降更明显,尽管大多数指标在术后约一年内恢复到基线水平。
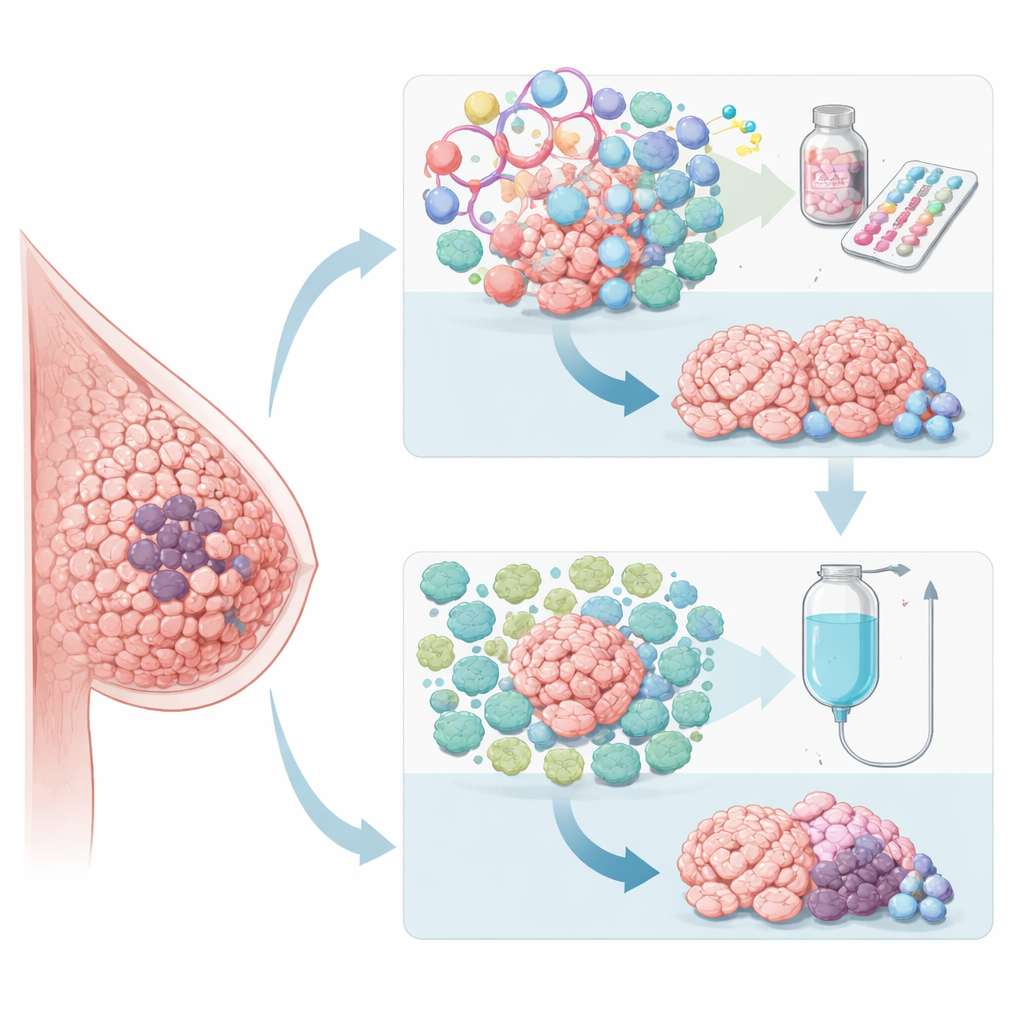
深入肿瘤以寻找隐含线索
由于常规指标如肿瘤分级和常规化验不足以指导先用哪种药物,研究者转向对肿瘤组织的深度分析。他们在治疗前使用全外显子组和RNA测序对数千个基因进行分型,并将这些基因表达模式与对不同治疗的应答相关联。对紫杉醇化疗反应良好的肿瘤通常显示出更强的免疫活性迹象和较弱的雌激素相关信号。相反,对帕博昔布加内分泌治疗反应更好的肿瘤在与细胞分裂和雌激素信号相关的基因上活动性较高,而免疫特征相对低沉。这些观察表明,癌症的生物学“特性”——不仅仅是其大小和分期——决定了其对不同治疗的反应。
一种用于治疗选择的新型基因工具
基于这些模式,研究团队构建了一种名为 CDKPredX 的新型基因工具。它将31个基因归纳为三个简单主题:肿瘤细胞的分裂速度、对雌激素的依赖程度以及局部免疫反应的活跃度。被标记为 CDKPredX 阳性的肿瘤表现为高度增殖、强烈的激素驱动并且免疫活性低。在 PREDIX LumB 试验中,这类肿瘤较少从化疗中获益,但仍对帕博昔布加内分泌治疗有反应。研究者随后在其他临床研究(包括 CORALLEEN 试验)和大型外部数据集中验证了 CDKPredX。在这些独立队列中,CDKPredX 一再识别出那些从化疗中获益甚少但仍对像帕博昔布这样的 CDK4/6 抑制剂敏感的患者。与此同时,该特征并非仅预测总体预后更好的人群;相反,它具体指出哪种治疗类型更有可能奏效。
对乳腺癌患者意味着什么
这项研究表明,对于这种类型的乳腺癌,在术前以不同顺序给予化疗或帕博昔布加内分泌治疗,平均而言会产生相似的肿瘤缩小效果和长期结局。然而,研究也显示肿瘤本身并非同质。通过读取每个肿瘤的基因“指纹”,像 CDKPredX 这样的工具或许能帮助医生识别出可以在不牺牲疗效的情况下安全避免最严酷化疗副作用的患者,及那些确实需要化疗强效打击的患者。尽管 CDKPredX 在成为常规指南前仍需前瞻性测试,但这项工作标志着向更个体化、而非一刀切的激素敏感型乳腺癌治疗迈出的重要一步。
引用: Matikas, A., Tzoras, E., Sarafidis, M. et al. Neoadjuvant palbociclib and endocrine therapy versus chemotherapy in ER + /HER2- breast cancer: a randomized phase II trial. Nat Commun 17, 3403 (2026). https://doi.org/10.1038/s41467-026-71452-6
关键词: 雌激素受体阳性乳腺癌, CDK4/6 抑制剂, 新辅助治疗, 化疗耐药, 肿瘤基因分型