Clear Sky Science · ru
Неоадъювантный палбосциклиб и эндокринная терапия против химиотерапии при ER+/HER2- раке молочной железы: рандомизированное исследование фазы II
Почему это исследование рака молочной железы важно
Для многих людей с гормонально-чувствительным раком молочной железы первым важным лечебным выбором является получение традиционной химиотерапии или новых целевых таблеток до операции. Химиотерапия может быть эффективной, но часто сопровождается тяжелыми побочными эффектами, тогда как препараты в виде таблеток, направленные на блокирование роста опухоли, могут переноситься легче, но пока не стали рутиной в этой ранней ситуации. В этом исследовании задается простой, но важный вопрос: можно ли безопасно применять целевые таблетки вместо химиотерапии или в другом порядке по отношению к ней — и могут ли современные генетические тесты опухоли подсказать, кому действительно какое лечение необходимо?
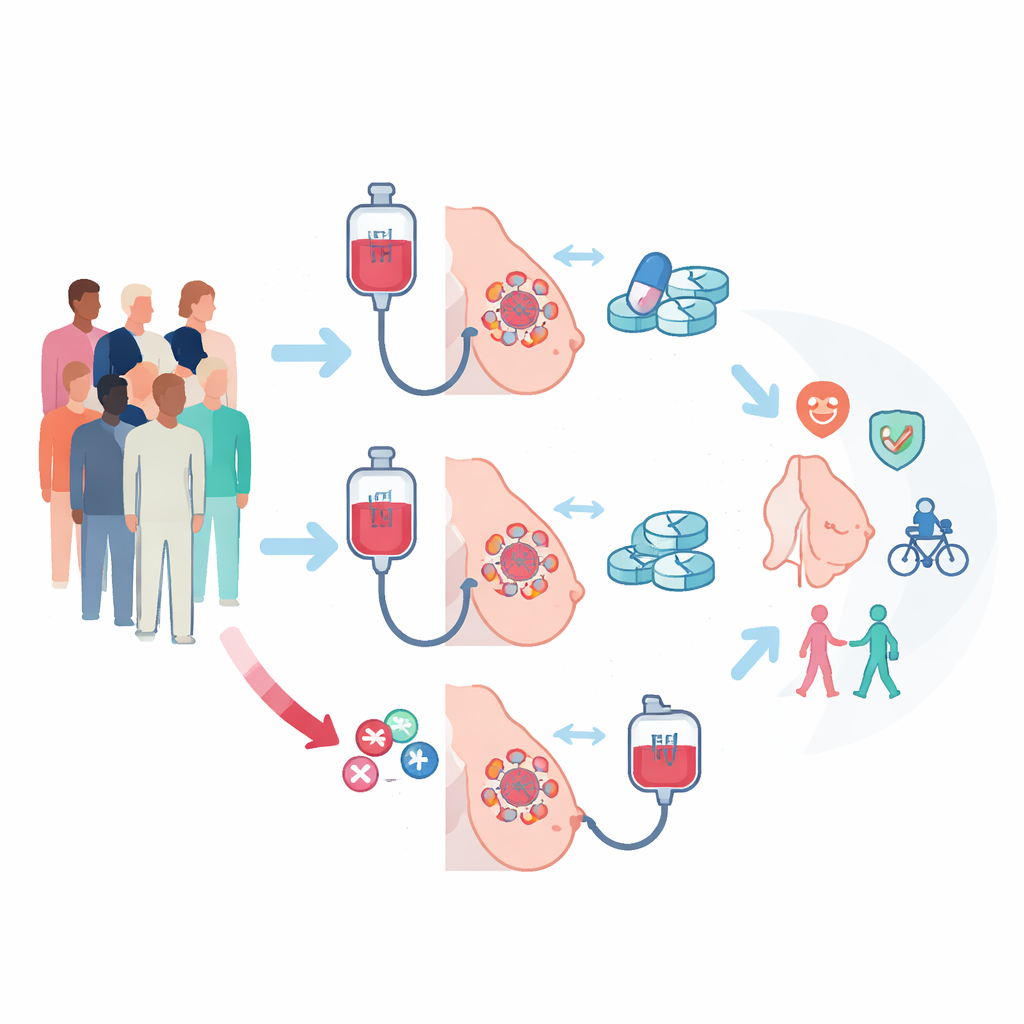
Два разных пути до операции
В исследование PREDIX LumB были включены 179 человек с распространенной формой рака молочной железы, чувствительной к эстрогену, но не сопровождающейся сверхэкспрессией белка HER2 (ER-позитивный/HER2-негативный). Все опухоли были достаточно большими и/или имели поражение близлежащих лимфоузлов, поэтому их уменьшение до операции имело клиническое значение. Участников рандомизировали в одну из двух групп. В одной ветви сначала проводили стандартную химиотерапию — еженедельный паклитаксел в течение 12 недель, затем 12 недель целевого препарата палбосциклиба в сочетании с гормональной блокадой. В другой ветви порядок был обратным: сначала палбосциклиб плюс гормональная терапия, затем паклитаксел. После 24 недель предоперационного лечения все пациенты прошли стандартную операцию и дальнейшую терапию по показаниям.
Схожее уменьшение опухоли и выживаемость, но разный повседневный эффект
Главной мерой была доля пациентов с явным уменьшением опухоли на сканах после первых 12 недель. Химиотерапия первой вызвала ответ у 59% пациентов, тогда как начало с таблетки плюс гормональной терапии дало ответы у 45%; эта разница не достигла уровня, который исследователи считают статистически значимым. К 24 неделям — после того как все получили оба вида лечения в разном порядке — показатели ответа были высокими и сходными в обеих группах. Долгосрочные исходы также совпадали: безрецидивная выживаемость, рецидивы после операции и общая выживаемость примерно за четыре с половиной года были по сути одинаковыми независимо от порядка лечения. Однако побочные эффекты различались по характеру. Химиотерапия чаще вызывала нейропатию рук и ног, сыпь и утомляемость, тогда как палбосциклиб чаще приводил к снижению числа белых кровяных клеток. Пациенты сообщали, что качество жизни лучше сохранялось во время приема таблеток и сильнее падало во время химиотерапии, хотя большинство показателей возвращалось к исходному уровню примерно через год после операции.
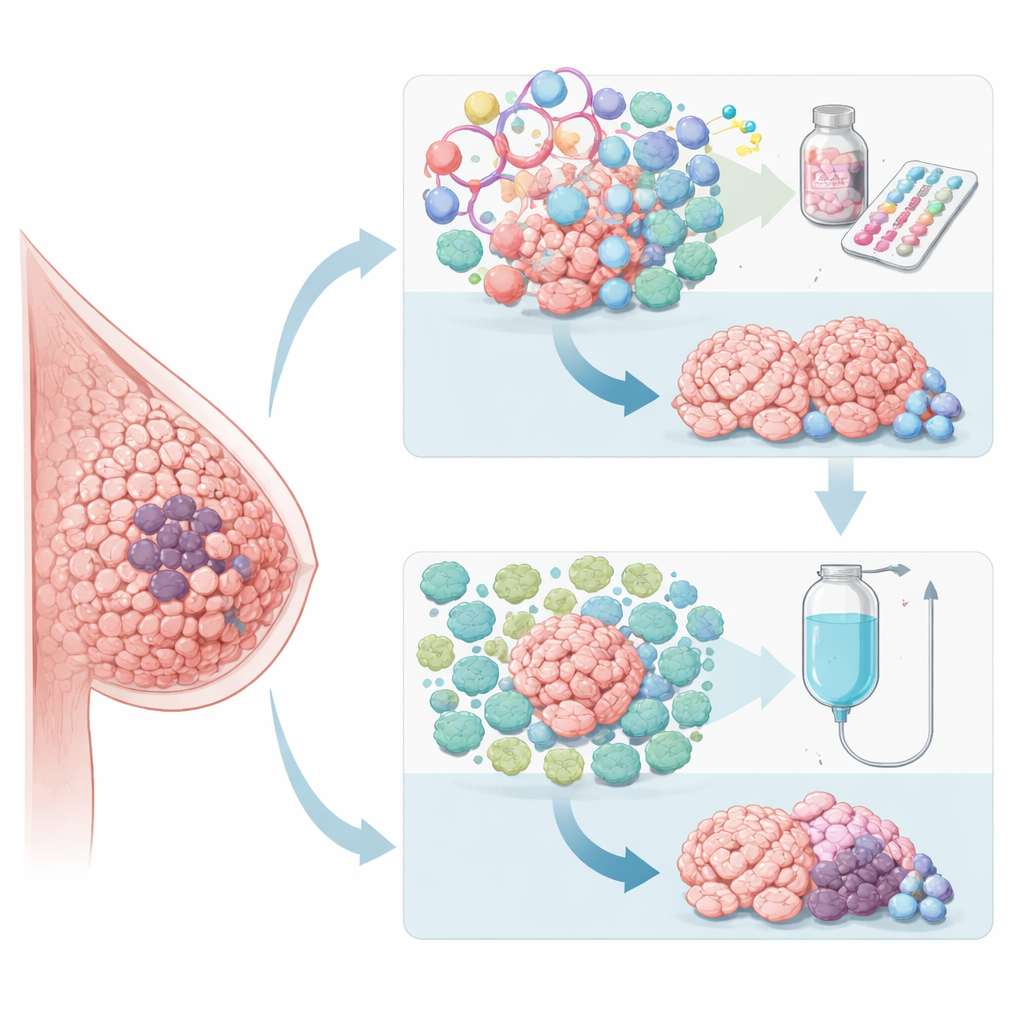
Взгляд внутрь опухолей в поисках скрытых подсказок
Поскольку стандартных показателей, таких как степень злокачественности опухоли и рутинные лабораторные тесты, было недостаточно, чтобы решить, кто должен получить какое лекарство первым, исследователи обратились к глубокому анализу ткани опухоли. Они использовали секвенирование всего экзома и РНК для профилирования тысяч генов до лечения и сопоставляли эти паттерны с ответом на ту или иную терапию. Опухоли, которые лучше отвечали на паклитаксел, чаще демонстрировали более выраженные признаки иммунной активности и слабее выраженные эстроген-зависимые сигналы. Напротив, опухоли, лучше реагировавшие на палбосциклиб в сочетании с гормональной терапией, проявляли высокую активность генов, связанных с делением клеток и эстрогеновым сигналингом, но относительно приглушенные иммунные сигнатуры. Эти наблюдения указывали на то, что биологическая «личность» рака — а не только его размер и стадия — определяет, как он реагирует на разные виды лечения.
Новый генетический ориентир для выбора лечения
Исходя из этих закономерностей, команда создала новый генетический инструмент под названием CDKPredX. Он объединяет 31 ген в три простые темы: скорость деления опухолевых клеток, степень зависимости от эстрогена и активность местного иммунного ответа. Опухоли, помеченные как CDKPredX-положительные, были высокопролиферативными, сильно гормонозависимыми и имели низкую иммунную активность. В исследовании PREDIX LumB эта группа реже извлекала пользу из химиотерапии, но продолжала отвечать на палбосциклиб в сочетании с гормональной терапией. Исследователи затем протестировали CDKPredX в других клинических исследованиях, включая CORALLEEN, и в крупных внешних наборах данных. В этих независимых когортах CDKPredX последовательно выявлял пациентов, которые мало выигрывали от химиотерапии, но оставались чувствительными к ингибиторам CDK4/6, таким как палбосциклиб. При этом сигнатура не просто предсказывала общий более благоприятный прогноз; она конкретно указывала, какой тип лечения с большей вероятностью сработает.
Что это значит для людей с раком молочной железы
Это исследование показывает, что в среднем проведение химиотерапии или целевого лечения палбосциклибом в сочетании с гормональной терапией в разной последовательности до операции приводит к схожему уменьшению опухоли и долгосрочным исходам для этого типа рака молочной железы. Однако оно также демонстрирует, что сами ракy далеко не однородны. Читая генетический «отпечаток» каждой опухоли, инструменты вроде CDKPredX вскоре могут помочь врачам определить пациентов, которые могли бы безопасно избежать самых тяжелых эффектов химиотерапии без потери эффективности, а также тех, кому действительно нужна «ударная» сила химиотерапии. При этом CDKPredX еще требует проспективной проверки, прежде чем он сможет руководить рутинной практикой, но эта работа представляет важный шаг к более персонализированному, а не «один размер для всех» подходу к лечению людей с гормонально-чувствительным раком молочной железы.
Цитирование: Matikas, A., Tzoras, E., Sarafidis, M. et al. Neoadjuvant palbociclib and endocrine therapy versus chemotherapy in ER + /HER2- breast cancer: a randomized phase II trial. Nat Commun 17, 3403 (2026). https://doi.org/10.1038/s41467-026-71452-6
Ключевые слова: ER-позитивный рак молочной железы, ингибиторы CDK4/6, неоадъювантная терапия, резистентность к химиотерапии, генетическое профилирование опухоли