Clear Sky Science · pl
Neoadiuwantowe palbocyklib i terapia hormonalna versus chemioterapia w raku piersi ER + /HER2-: randomizowane badanie fazy II
Dlaczego to badanie raka piersi ma znaczenie
Dla wielu osób z rakiem piersi wrażliwym na hormony pierwszą istotną decyzją terapeutyczną jest, czy otrzymać tradycyjną chemioterapię, czy nowsze doustne terapie celowane przed operacją. Chemioterapia może być skuteczna, ale często wiąże się z obciążającymi skutkami ubocznymi, podczas gdy terapie w formie tabletek, mające na celu blokowanie wzrostu guza, mogą być łagodniejsze, ale nie są jeszcze rutynowo stosowane we wczesnym stadium. Badanie stawia proste, lecz kluczowe pytanie: czy możemy bezpiecznie stosować leki celowane zamiast chemioterapii, lub w innej kolejności — i czy nowoczesne testy genetyczne guza mogą wskazać, kto naprawdę potrzebuje którego leczenia?
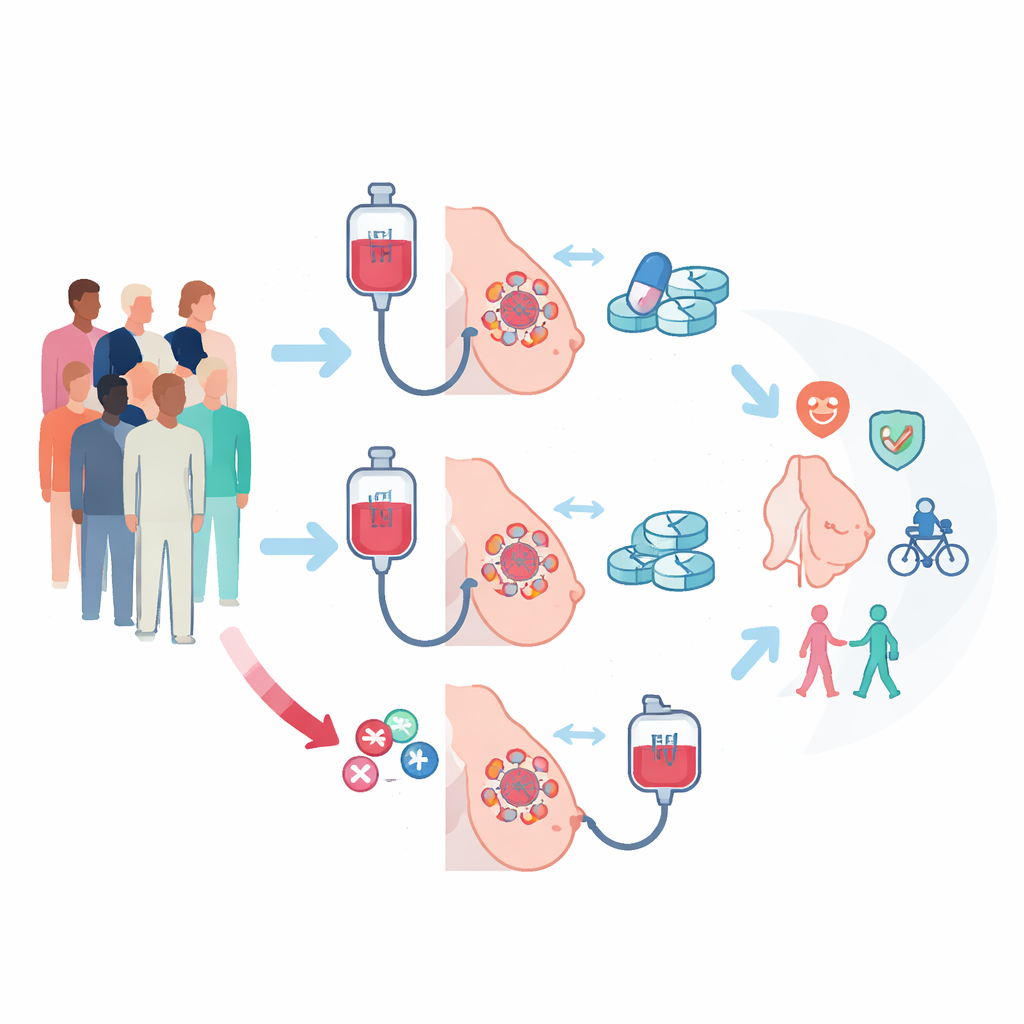
Dwie różne drogi przed operacją
W badaniu PREDIX LumB zapisano 179 osób z powszechną postacią raka piersi wrażliwego na estrogen, ale nienadekspresującego białka HER2 (ER-dodatni/HER2-ujemny). Wszystkie guzy były stosunkowo duże i/lub zajęły pobliskie węzły chłonne, więc ich zmniejszenie przed zabiegiem było medycznie istotne. Uczestnicy zostali losowo przydzieleni do jednej z dwóch ścieżek. W jednej grupie najpierw otrzymali standardową chemioterapię — paklitaksel co tydzień przez 12 tygodni — a następnie przez 12 tygodni palbocyklib w połączeniu z terapią blokującą hormony. W drugiej grupie kolejność była odwrotna: najpierw palbocyklib plus terapia hormonalna, potem paklitaksel. Po tych 24 tygodniach leczenia przedoperacyjnego wszyscy przeszli standardowy zabieg chirurgiczny i dalszą terapię zgodnie z zaleceniami.
Podobne zmniejszenie guza i przeżycia, różny wpływ na codzienne życie
Głównym wskaźnikiem była odsetek pacjentów, u których guzy wyraźnie zmniejszyły się w badaniach obrazowych po pierwszych 12 tygodniach. Rozpoczęcie od chemioterapii dało odpowiedź u 59% pacjentów, podczas gdy rozpoczęcie od leku w połączeniu z terapią hormonalną — u 45%; ta różnica nie osiągnęła poziomu uznawanego przez badaczy za statystycznie istotny. Po 24 tygodniach — gdy wszyscy otrzymali oba typy leczenia w odwrotnej kolejności — wskaźniki odpowiedzi były wysokie i podobne w obu grupach. Wyniki długoterminowe także były zbliżone: przeżycie bez zdarzeń, nawroty po operacji i przeżycie ogólne przez około cztery i pół roku były zasadniczo takie same niezależnie od kolejności leczenia. Skutki uboczne różniły się jednak charakterem. Chemioterapia częściej powodowała uszkodzenia nerwów w dłoniach i stopach, wysypkę oraz zmęczenie, podczas gdy palbocyklib częściej prowadził do spadków liczby białych krwinek. Pacjenci zgłaszali, że jakość życia była lepiej zachowana w fazie leczenia doustnego, a bardziej obniżona podczas chemioterapii, chociaż większość miar wróciła do poziomu wyjściowego około roku po operacji.
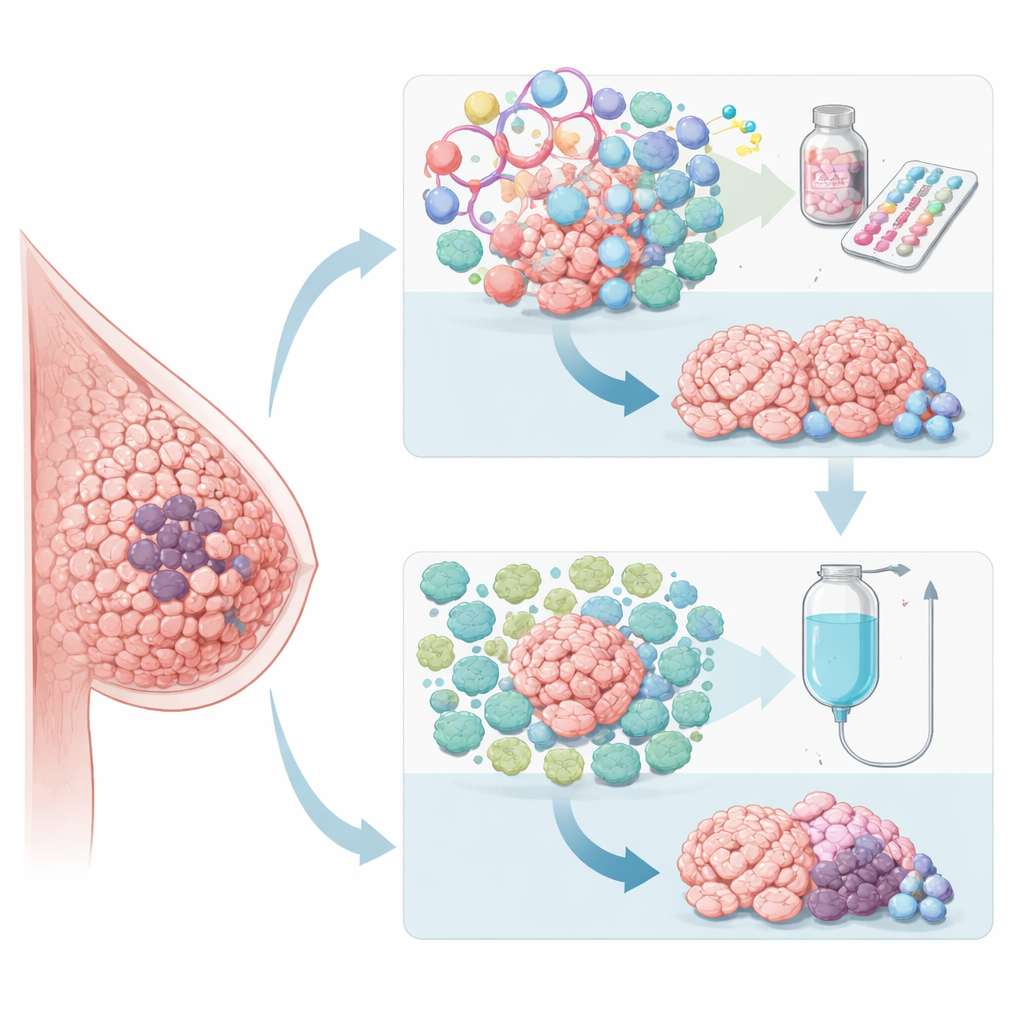
Zajrzeć do wnętrza guzów po ukryte wskazówki
Ponieważ standardowe miary, takie jak stopień złośliwości guza i rutynowe badania laboratoryjne, nie wystarczały do wskazania, kto powinien otrzymać który lek jako pierwszy, badacze sięgnęli po dogłębne analizy tkanek nowotworowych. Wykorzystali sekwencjonowanie całego egzomu i RNA, aby przeanalizować tysiące genów przed leczeniem i powiązać te wzorce z odpowiedzią na poszczególne terapie. Guzy, które dobrze reagowały na chemioterapię paklitakselem, miały tendencję do silniejszych oznak aktywności układu odpornościowego i słabszych sygnałów związanych z estrogenem. Natomiast guzy lepiej reagujące na palbocyklib w połączeniu z terapią hormonalną wykazywały wysoką aktywność genów związanych z podziałem komórek i sygnalizacją estrogenową, ale stosunkowo stłumione sygnatury immunologiczne. Obserwacje te sugerują, że biologiczna „osobowość” nowotworu — nie tylko jego rozmiar i stopień zaawansowania — kształtuje, jak reaguje na różne terapie.
Nowy genetyczny przewodnik wyboru terapii
Na podstawie tych wzorców zespół opracował nowe narzędzie genetyczne nazwane CDKPredX. Łączy ono 31 genów w trzy proste motywy: tempo podziału komórek nowotworowych, stopień zależności od estrogenu oraz aktywność lokalnej odpowiedzi immunologicznej. Guzy oznaczone jako CDKPredX-pozytywne były wysoce proliferacyjne, silnie napędzane hormonami i miały niską aktywność odpornościową. W badaniu PREDIX LumB grupa ta rzadziej korzystała z chemioterapii, ale nadal reagowała na palbocyklib z terapią hormonalną. Badacze następnie przetestowali CDKPredX w innych badaniach klinicznych, w tym w próbie CORALLEEN oraz w dużych zewnętrznych zestawach danych. W tych niezależnych grupach CDKPredX wielokrotnie identyfikował pacjentów, którzy niewiele zyskiwali dzięki chemioterapii, a jednocześnie pozostawali wrażliwi na inhibitory CDK4/6, takie jak palbocyklib. Jednocześnie sygnatura nie była jedynie prognozą ogólnego lepszego przebiegu; specyficznie wskazywała, który typ leczenia był bardziej prawdopodobny, by zadziałać.
Co to oznacza dla osób z rakiem piersi
Badanie pokazuje, że średnio podawanie chemioterapii lub terapii celowanej palbocyklibem w połączeniu z terapią hormonalną w różnych sekwencjach przed operacją prowadzi do podobnego zmniejszenia guza i wyników długoterminowych w tym typie raka piersi. Jednocześnie ujawnia, że nowotwory są dalekie od jednorodności. Czytając genetyczny „odcisk palca” każdego guza, narzędzia takie jak CDKPredX mogą wkrótce pomóc lekarzom zidentyfikować pacjentów, którzy bezpiecznie mogą uniknąć najsurowszych skutków chemioterapii bez utraty skuteczności, oraz tych, którzy rzeczywiście potrzebują uderzenia chemioterapii. Choć CDKPredX wymaga jeszcze prospektywnego przetestowania, zanim będzie mógł kierować rutynową opieką, praca ta stanowi ważny krok w kierunku bardziej spersonalizowanego, mniej jednorodnego leczenia osób z rakiem piersi wrażliwym na hormony.
Cytowanie: Matikas, A., Tzoras, E., Sarafidis, M. et al. Neoadjuvant palbociclib and endocrine therapy versus chemotherapy in ER + /HER2- breast cancer: a randomized phase II trial. Nat Commun 17, 3403 (2026). https://doi.org/10.1038/s41467-026-71452-6
Słowa kluczowe: Rak piersi z receptorami estrogenowymi, Inhibitory CDK4/6, terapia neoadiuwantowa, oporność na chemioterapię, profilowanie genów nowotworu