Clear Sky Science · fr
Palbociclib néo-adjuvant et hormonothérapie vs chimiothérapie dans le cancer du sein ER + /HER2- : un essai randomisé de phase II
Pourquoi cette étude sur le cancer du sein est importante
Pour de nombreuses personnes atteintes d’un cancer du sein hormonosensible, la première décision majeure de traitement consiste à choisir entre une chimiothérapie traditionnelle ou de nouvelles pilules ciblées avant la chirurgie. La chimiothérapie peut être efficace mais s’accompagne souvent d’effets secondaires lourds, tandis que les traitements oraux visant à bloquer la croissance tumorale peuvent être plus doux mais ne sont pas encore routiniers à ce stade précoce. Cette étude pose une question simple mais cruciale : peut‑on utiliser en toute sécurité des pilules ciblées à la place de la chimiothérapie, ou dans un ordre différent — et les tests génétiques modernes sur la tumeur peuvent‑ils nous dire qui a réellement besoin de quel traitement ?
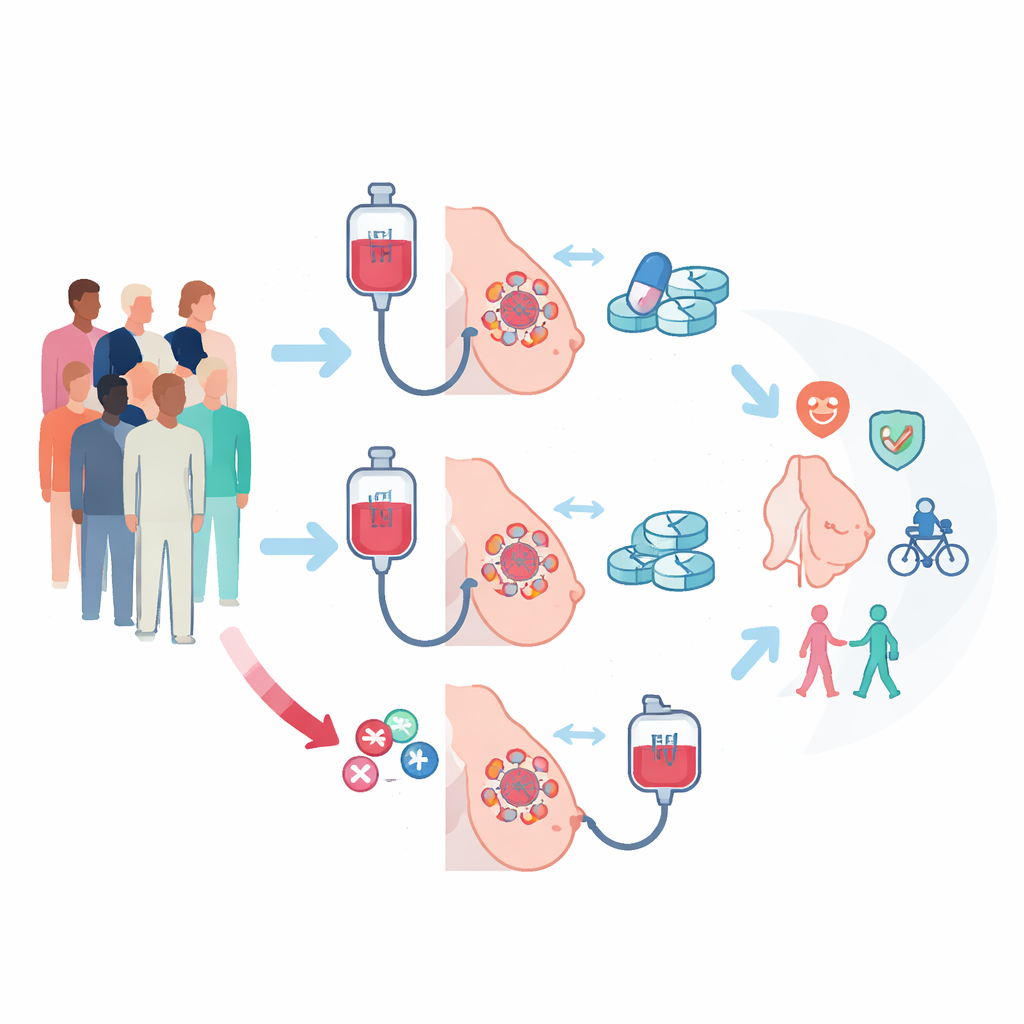
Deux parcours différents avant la chirurgie
L’essai PREDIX LumB a recruté 179 personnes atteintes d’une forme fréquente de cancer du sein sensible aux œstrogènes mais sans surexpression de la protéine HER2 (ER‑positif/HER2‑négatif). Toutes les tumeurs étaient relativement volumineuses et/ou avaient gagné des ganglions lymphatiques voisins, rendant leur réduction avant chirurgie médicalement importante. Les participant·e·s ont été assigné·e·s aléatoirement à l’un des deux parcours. Dans un bras, ils ont d’abord reçu la chimiothérapie standard avec du paclitaxel hebdomadaire pendant 12 semaines, suivie de 12 semaines d’une pilule ciblée appelée palbociclib en association avec une hormonothérapie. Dans l’autre bras, l’ordre était inversé : palbociclib plus hormonothérapie en premier, puis paclitaxel. Après ces 24 semaines de traitement préopératoire, tout le monde a bénéficié de la chirurgie standard et d’un traitement complémentaire selon les recommandations.
Réduction tumorale et survie similaires, impact quotidien différent
Le principal critère était le pourcentage de patient·e·s dont la tumeur avait clairement diminué à l’imagerie après les 12 premières semaines. La chimiothérapie en premier a entraîné des réponses chez 59 % des patient·e·s, tandis que commencer par la pilule plus hormonothérapie a donné des réponses chez 45 % ; cette différence n’a pas atteint le seuil considéré comme statistiquement certain par les chercheurs. À 24 semaines — après que tout le monde a reçu les deux types de traitement en ordre inverse — les taux de réponse étaient élevés et comparables dans les deux groupes. Les résultats à plus long terme étaient également similaires : survie sans événement, récidives après chirurgie et survie globale sur environ quatre ans et demi étaient essentiellement équivalents quel que soit l’ordre des traitements. En revanche, les effets indésirables différaient par leur nature. La chimiothérapie provoquait plus souvent des atteintes nerveuses périphériques (engourdissements, picotements), des éruptions cutanées et de la fatigue, tandis que le palbociclib entraînait fréquemment des baisses des globules blancs. Les patient·e·s ont rapporté une qualité de vie mieux préservée pendant la phase orale et une baisse plus marquée pendant la chimiothérapie, bien que la plupart des paramètres soient revenus au niveau de référence environ un an après la chirurgie.
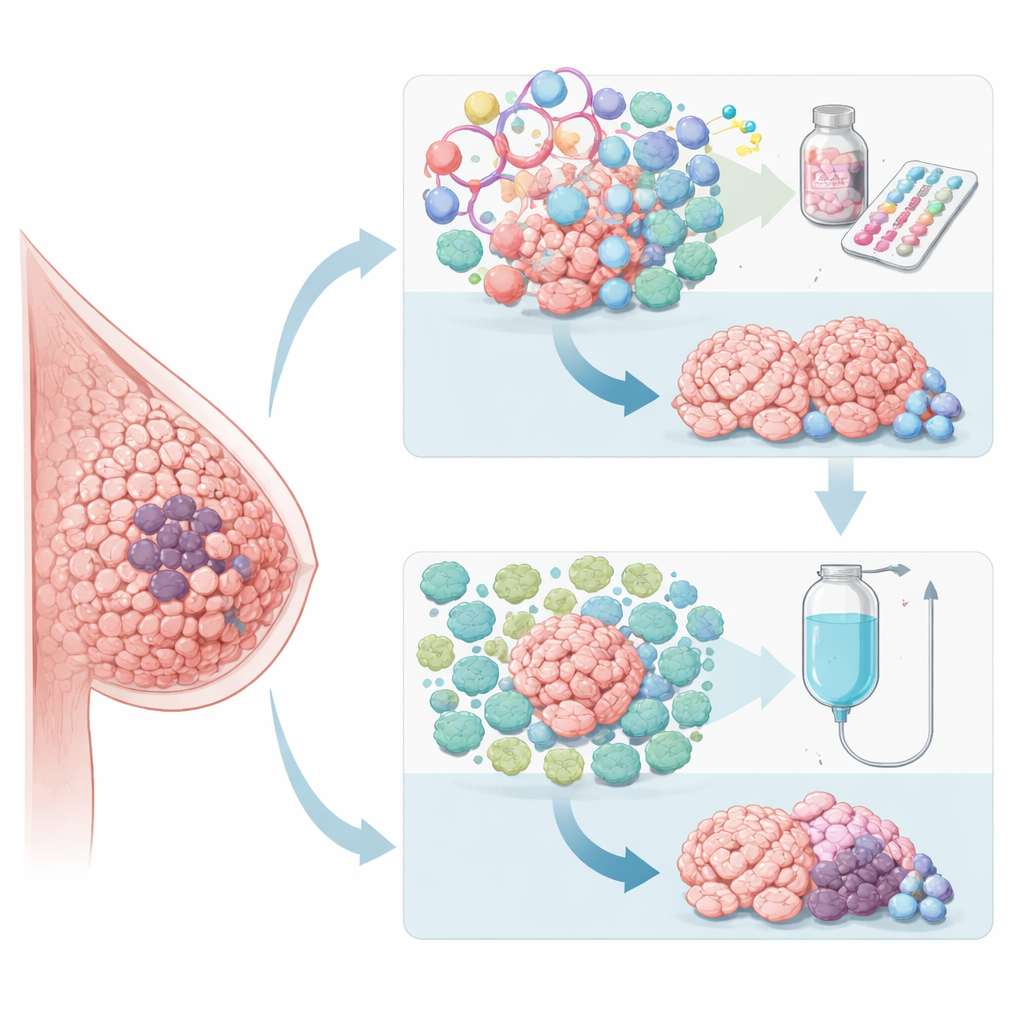
Explorer les tumeurs pour y trouver des indices cachés
Comme les mesures standard — grade tumoral et bilans de routine — ne suffisaient pas à orienter qui devrait recevoir quel médicament en premier, les chercheurs se sont tournés vers des analyses approfondies des tissus tumoraux. Ils ont utilisé le séquençage de l’exome entier et de l’ARN pour profiler des milliers de gènes avant le traitement et ont relié ces profils à la réponse à chaque thérapie. Les tumeurs qui répondaient bien au paclitaxel présentaient en général des signes plus marqués d’activité immunitaire et des signaux œstrogéniques plus faibles. À l’inverse, les tumeurs qui répondaient mieux au palbociclib associé à l’hormonothérapie montraient une forte activité de gènes liés à la division cellulaire et au signalement œstrogénique, mais des signatures immunitaires relativement atténuées. Ces observations suggèrent que la « personnalité » biologique du cancer — pas seulement sa taille et son stade — conditionne sa réaction aux différents traitements.
Un nouvel outil génétique pour guider le choix thérapeutique
À partir de ces schémas, l’équipe a construit un nouvel outil génétique appelé CDKPredX. Il combine 31 gènes en trois thèmes simples : la vitesse de prolifération des cellules tumorales, leur dépendance aux œstrogènes et l’activité de la réponse immunitaire locale. Les tumeurs classées CDKPredX‑positives étaient fortement prolifératives, fortement hormonodépendantes et présentaient une faible activité immunitaire. Dans l’essai PREDIX LumB, ce groupe était moins susceptible de bénéficier de la chimiothérapie mais répondait toujours au palbociclib associé à l’hormonothérapie. Les chercheurs ont ensuite testé CDKPredX dans d’autres études cliniques, dont l’essai CORALLEEN et de grandes bases de données externes. Dans ces cohortes indépendantes, CDKPredX a de manière répétée identifié des patient·e·s qui tiraient peu d’avantage de la chimiothérapie tout en restant sensibles aux inhibiteurs de CDK4/6 comme le palbociclib. Parallèlement, ce profil ne prédisait pas simplement qui irait mieux globalement ; il mettait spécifiquement en évidence quel type de traitement avait le plus de chances de fonctionner.
Ce que cela signifie pour les personnes atteintes d’un cancer du sein
Cette étude montre que, en moyenne, administrer la chimiothérapie ou le palbociclib ciblé associé à l’hormonothérapie dans des séquences différentes avant la chirurgie conduit à une réduction tumorale et à des résultats à long terme similaires pour ce type de cancer du sein. Elle révèle toutefois que les cancers sont loin d’être uniformes. En lisant l’« empreinte » génétique de chaque tumeur, des outils comme CDKPredX pourraient bientôt aider les médecins à identifier des patient·e·s qui pourraient éviter en toute sécurité les effets les plus lourds de la chimiothérapie sans sacrifier l’efficacité, et d’autres qui ont vraiment besoin de la puissance de la chimiothérapie. Bien que CDKPredX doive encore être testé de manière prospective avant de pouvoir orienter les pratiques courantes, ce travail constitue une étape importante vers des traitements plus personnalisés et moins uniformes pour les personnes atteintes d’un cancer du sein hormonosensible.
Citation: Matikas, A., Tzoras, E., Sarafidis, M. et al. Neoadjuvant palbociclib and endocrine therapy versus chemotherapy in ER + /HER2- breast cancer: a randomized phase II trial. Nat Commun 17, 3403 (2026). https://doi.org/10.1038/s41467-026-71452-6
Mots-clés: Cancer du sein ER-positif, Inhibiteurs de CDK4/6, Thérapie néo-adjuvante, Résistance à la chimiothérapie, Profilage génétique des tumeurs