Clear Sky Science · de
Neoadjuvante Palbociclib- und endokrine Therapie versus Chemotherapie bei ER+/HER2- Brustkrebs: eine randomisierte Phase-II-Studie
Warum diese Brustkrebsstudie wichtig ist
Für viele Menschen mit hormonsensitivem Brustkrebs besteht die erste große Therapieentscheidung darin, ob sie vor der Operation eine klassische Chemotherapie oder neuere zielgerichtete Tabletten erhalten sollen. Chemotherapie kann wirksam sein, geht aber oft mit belastenden Nebenwirkungen einher, während tablettenbasierte Behandlungen, die das Tumorwachstum blockieren, schonender sein können, in dieser frühen Situation aber noch nicht routinemäßig eingesetzt werden. Diese Studie stellt eine einfache, aber wesentliche Frage: Können wir gezielte Tabletten sicher anstelle von, oder in anderer Reihenfolge als, Chemotherapie verwenden — und können moderne Gentests am Tumor vorhersagen, wer welche Behandlung wirklich benötigt?
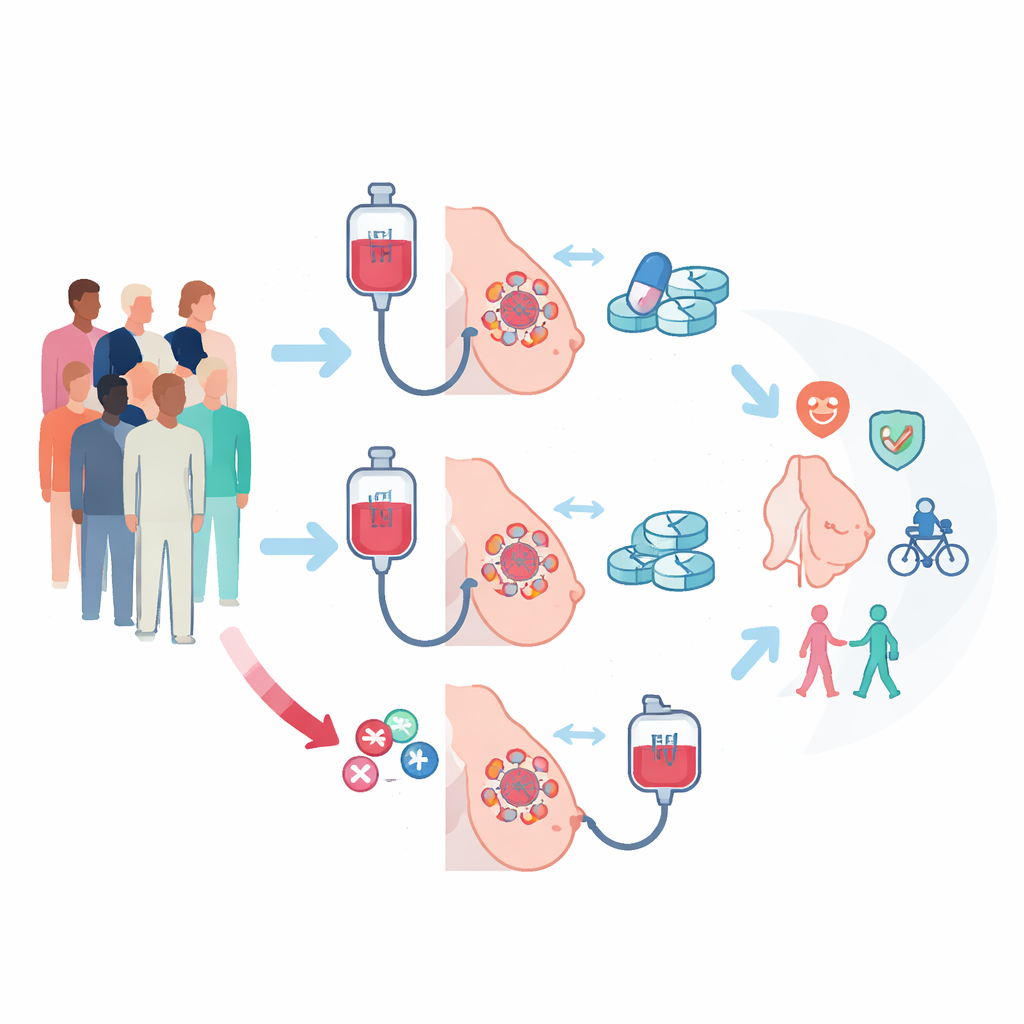
Zwei unterschiedliche Wege vor der Operation
Die PREDIX LumB-Studie rekrutierte 179 Personen mit einer häufigen Form von Brustkrebs, die auf Östrogen anspricht, aber kein HER2-Protein übermäßig produziert (ER-positiv/HER2-negativ). Alle Tumoren waren relativ groß und/oder hatten sich auf nahegelegene Lymphknoten ausgebreitet, sodass eine Verkleinerung vor der Operation medizinisch wichtig war. Die Teilnehmenden wurden zufällig einem von zwei Wegen zugewiesen. In einem Arm erhielten sie zunächst die Standardchemotherapie mit wöchentlichem Paclitaxel über 12 Wochen, gefolgt von 12 Wochen eines zielgerichteten Medikaments namens Palbociclib in Kombination mit einer hormonblockierenden Therapie. Im anderen Arm war die Reihenfolge umgekehrt: Zuerst Palbociclib plus Hormontherapie, dann Paclitaxel. Nach diesen 24 Wochen der präoperativen Behandlung unterzogen sich alle der Standardoperation und der empfohlenen Nachbehandlung.
Ähnliche Tumorverkleinerung und Überleben, unterschiedlicher Alltagsimpact
Der wichtigste Maßstab war, wie viele Patientinnen und Patienten nach den ersten 12 Wochen in bildgebenden Verfahren eine deutliche Tumorverkleinerung zeigten. Eine Chemotherapie zuerst führte zu Ansprechen bei 59 % der Betroffenen, während der Beginn mit Tabletten plus Hormontherapie bei 45 % zu Ansprechen führte; dieser Unterschied erreichte nicht das statistische Signifikanzniveau, das die Forschenden als belastbar betrachten. Nach 24 Wochen — nachdem alle beide Behandlungsarten in umgekehrter Reihenfolge erhalten hatten — waren die Ansprechraten in beiden Gruppen hoch und ähnlich. Auch die langfristigen Ergebnisse waren vergleichbar: ereignisfreies Überleben, Rückfälle nach der Operation und das Gesamtüberleben über etwa viereinhalb Jahre waren im Wesentlichen gleich, unabhängig davon, welche Therapie zuerst gegeben wurde. Die Nebenwirkungen unterschieden sich jedoch in der Art. Die Chemotherapie verursachte häufiger Nervenschäden in Händen und Füßen, Hautausschlag und Müdigkeit, während Palbociclib häufig zu Abfällen der weißen Blutkörperchen führte. Patientinnen und Patienten berichteten, dass ihre Lebensqualität während der tablettenbasierten Phase besser erhalten blieb und während der Chemotherapie stärker abfiel, wobei sich die meisten Messwerte etwa ein Jahr nach der Operation wieder dem Ausgangswert annäherten.
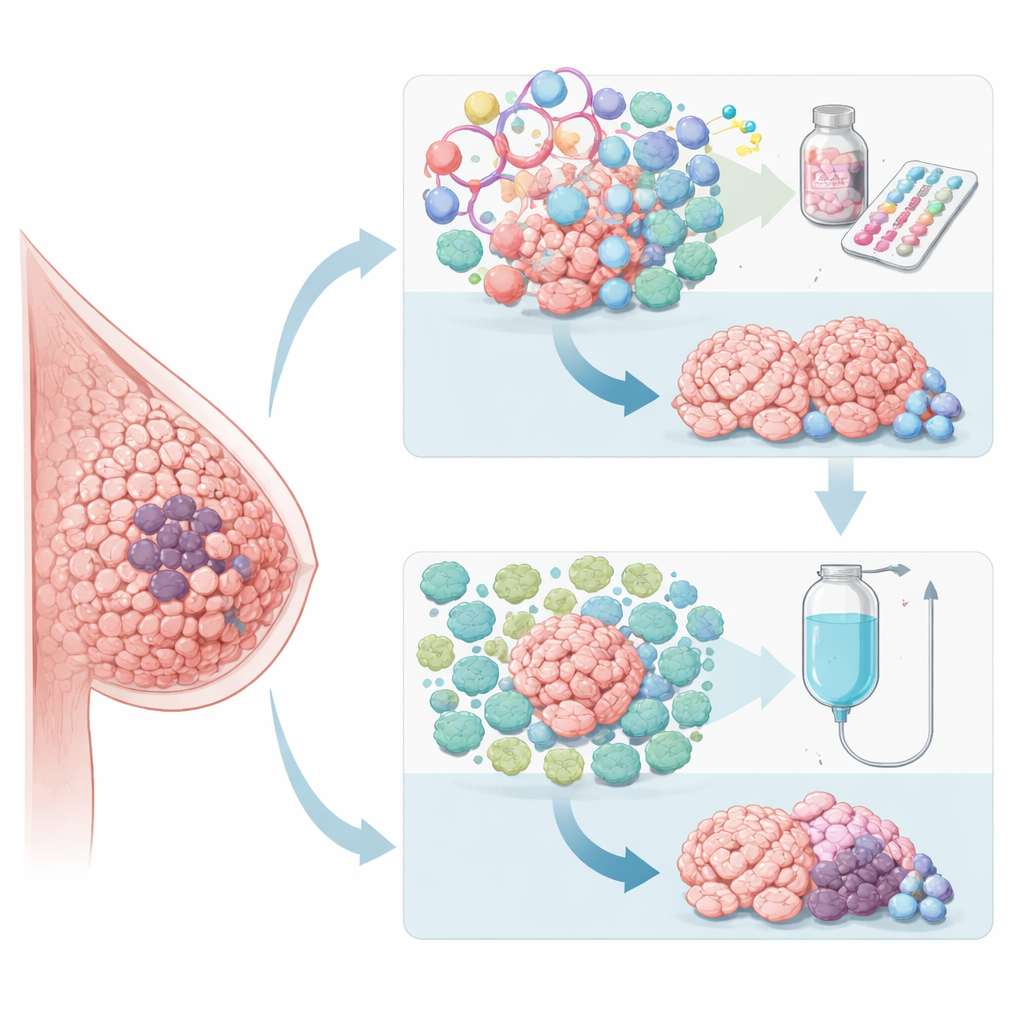
Im Tumor nach verborgenen Hinweisen suchen
Da Standardmaße wie Tumorgrad und Routine-Labortests nicht ausreichten, um zu entscheiden, wer welches Medikament zuerst erhalten sollte, wandten sich die Forschenden tiefgehenden Analysen des Tumorgewebes zu. Sie nutzten Whole-Exome- und RNA-Sequenzierung, um Tausende von Genen vor der Behandlung zu charakterisieren und diese Muster mit dem Ansprechen auf die jeweiligen Therapien zu verknüpfen. Tumoren, die gut auf die Paclitaxel-Chemotherapie reagierten, zeigten tendenziell stärkere Hinweise auf Immunaktivität und schwächere östrogenbezogene Signale. Im Gegensatz dazu wiesen Tumoren, die besser auf Palbociclib plus Hormontherapie ansprachen, eine hohe Aktivität in Genen auf, die mit Zellteilung und Östrogen-Signalgebung verbunden sind, aber relativ zurückhaltende Immunprofile. Diese Beobachtungen deuten darauf hin, dass die biologische „Persönlichkeit“ des Krebses — nicht nur seine Größe und sein Stadium — bestimmt, wie er auf verschiedene Behandlungen reagiert.
Ein neuer genetischer Leitfaden für die Therapieauswahl
Auf Basis dieser Muster entwickelte das Team ein neues genetisches Instrument namens CDKPredX. Es fasst 31 Gene zu drei einfachen Themen zusammen: wie schnell sich die Tumorzellen teilen, wie stark sie vom Östrogen abhängig sind und wie aktiv die lokale Immunantwort ist. Als CDKPredX-positiv klassifizierte Tumoren waren hoch proliferativ, stark hormongetrieben und wiesen eine geringe Immunaktivität auf. In der PREDIX LumB-Studie profitierte diese Gruppe weniger von der Chemotherapie, sprach aber weiterhin auf Palbociclib plus Hormontherapie an. Die Forschenden testeten CDKPredX anschließend in anderen klinischen Studien, darunter der CORALLEEN-Studie, sowie in großen externen Datensätzen. Über diese unabhängigen Kohorten hinweg identifizierte CDKPredX wiederholt Patientinnen und Patienten, die wenig von Chemotherapie profitierten, aber gegenüber CDK4/6-Inhibitoren wie Palbociclib empfindlich blieben. Gleichzeitig sagte die Signatur nicht einfach voraus, wer insgesamt besser abschneiden würde; vielmehr hob sie spezifisch hervor, welche Behandlungsart mit höherer Wahrscheinlichkeit wirksam ist.
Was das für Menschen mit Brustkrebs bedeutet
Diese Studie zeigt, dass das Verabreichen von Chemotherapie oder zielgerichteter Palbociclib- plus Hormontherapie in unterschiedlicher Reihenfolge vor der Operation im Mittel zu ähnlicher Tumorverkleinerung und langfristigen Ergebnissen für diese Form des Brustkrebses führt. Sie macht aber auch deutlich, dass die Tumoren alles andere als einheitlich sind. Indem man den genetischen „Fingerabdruck“ jedes Tumors liest, könnten Werkzeuge wie CDKPredX Ärztinnen und Ärzten bald helfen, Patientinnen und Patienten zu identifizieren, die die stärksten Nebenwirkungen der Chemotherapie sicher vermeiden können, ohne an Wirksamkeit einzubüßen, und andere, die tatsächlich die stärkere Wirkung der Chemotherapie benötigen. Obwohl CDKPredX noch prospektiv getestet werden muss, bevor es die Routineentscheidung leiten kann, stellt diese Arbeit einen wichtigen Schritt in Richtung einer personalisierteren, weniger uniformen Behandlung für Menschen mit hormonsensitivem Brustkrebs dar.
Zitation: Matikas, A., Tzoras, E., Sarafidis, M. et al. Neoadjuvant palbociclib and endocrine therapy versus chemotherapy in ER + /HER2- breast cancer: a randomized phase II trial. Nat Commun 17, 3403 (2026). https://doi.org/10.1038/s41467-026-71452-6
Schlüsselwörter: ER-positiver Brustkrebs, CDK4/6-Inhibitoren, neoadjuvante Therapie, Chemotherapie-Resistenz, Tumor-Genprofilierung