Clear Sky Science · zh
DC-CD4 双特异性耐受性纳米囊泡诱导抗原特异性调节性T细胞并改善小鼠胶原诱导性关节炎
教免疫系统何时不应进攻
自身免疫性疾病发生在机体的防御系统错误地攻击自身组织时,引发慢性疼痛和损伤。科学家们正在寻找比广泛抑制免疫更精确的办法,以重新训练这些防御系统,使其对特定的无害靶标视而不见,同时仍能对真正的威胁作出反应。这项小鼠研究描述了一个微小的工程化载体,旨在实现这一目标,为将来治疗类风湿性关节炎等疾病提供更精确的思路。 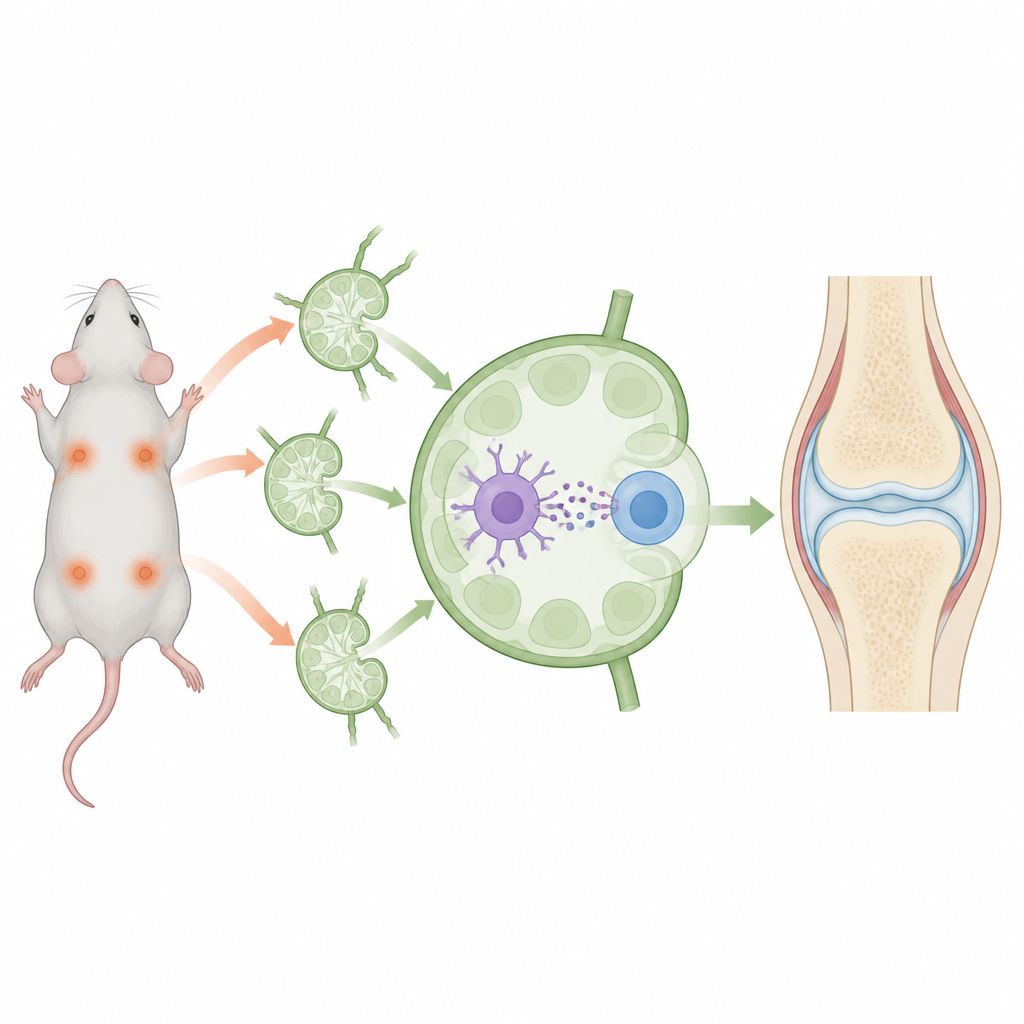
为何有选择地压低特定细胞很重要
健康的免疫系统能区分“自身”与“入侵者”,这种平衡被称为免疫耐受。一类特殊的白细胞——调节性T细胞,像维护和平的角色,在有害反应失控前将其平息。临床上曾尝试通过体外扩增后回输这些细胞,或使用促进其体内生长的药物来增强它们,两种方法都有缺点,包括细胞处理复杂以及可能过度抑制免疫。目标是仅增加那些识别与特定疾病相关的有问题自我分子的调节性细胞。
设计微小的维持和平囊泡
研究者构建了纳米级的囊泡,取自具有镇静特性的免疫细胞外膜。这些囊泡被装载两种关键成分:一段短的胶原片段(关节中在关节炎中被靶向的蛋白)和促进耐受性状态的药物雷帕霉素。随后对囊泡进行“装饰”,使其能在淋巴结中同时依附两类不同的伙伴:展示抗原的树突状细胞和可分化为攻击性或调节性角色的CD4 T细胞。通过在同一胶原片段和药物周围将这两类细胞物理性地聚集在一起,囊泡被设计为将细胞间的交流引导向耐受而非攻击。
将免疫流量引导到正确位置
注射入小鼠皮下后,纳米囊泡流入邻近的淋巴结——免疫决策的枢纽。在那里,它们牢固地附着于树突状细胞和CD4 T细胞,有效地充当两者之间的桥梁。与游离药物和胶原相比,囊泡将更多物质送入树突状细胞,并显著增强这些细胞展示胶原片段的能力。与此同时,它们使树突状细胞和CD4 T细胞趋向更安静、更具调节性的表型,炎性信号减少,而像TGF-β和IL-10等抑炎因子增加。这种环境有利于胶原特异性调节性T细胞的扩增,这些细胞随后能够识别并抑制针对关节的免疫攻击。
在关节炎模型中保护关节
为检验这种免疫再教育在疾病中的意义,研究团队采用了标准的胶原诱导关节炎小鼠模型,它模拟了许多人类类风湿性关节炎的特征。接受胶原装载纳米囊泡治疗的小鼠出现的关节肿胀明显较轻,活动能力保持较好,体重损失也更少。影像学和组织切片显示,治疗组关节侵蚀更少、活动性炎症迹象减少、瘢痕形成减轻。重要的是,调节性T细胞不仅在淋巴结和脾脏中增加,在关节衬里内也有所升高,同时有害的炎性分子下降。缺乏正确抗原的囊泡或不能有效桥接两类细胞的囊泡保护作用较弱,强调了抗原选择与细胞间联结的重要性。 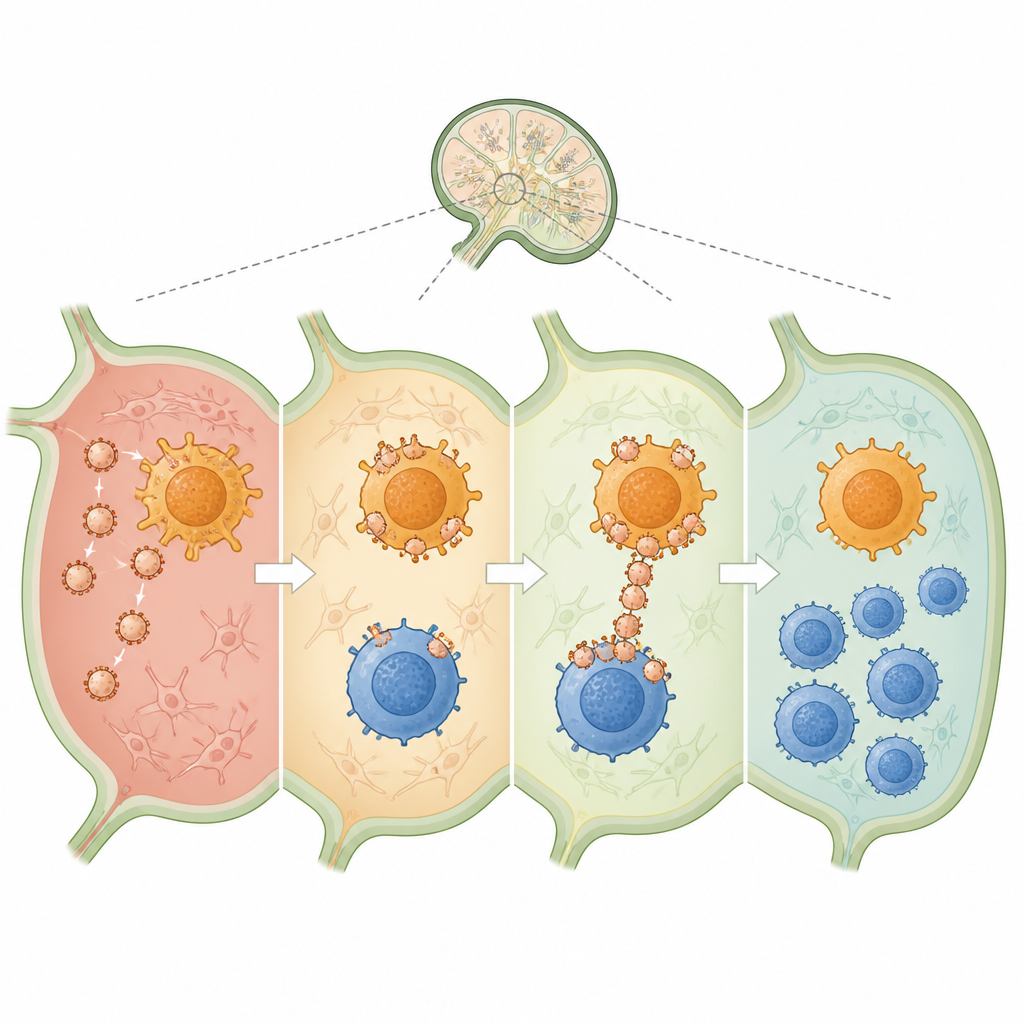
持久的平静及下一步方向
研究者进一步证明,这些纳米囊泡诱导的调节性T细胞可以转移保护效果到其他小鼠,并帮助抵抗随后发生的关节炎复发,表明免疫系统“记住”了这次教导。虽然相关工作仍限于小鼠和单一关节炎模型,但它指向一种灵活的平台,可以替换进不同疾病相关的自我片段,以重新训练不同自身免疫病中的免疫反应。对患者而言,这种方法的目标不是完全沉默免疫系统,而是教会它仅在对机体有害之处退让。
引用: Zhao, L., Gao, Z., Yuan, Z. et al. DC-CD4 bispecific tolerogenic nanovesicles induce antigen-specific regulatory T cells and ameliorate collagen-induced arthritis in mice. Nat Commun 17, 4170 (2026). https://doi.org/10.1038/s41467-026-70898-y
关键词: 自身免疫耐受, 调节性T细胞, 纳米囊泡, 类风湿性关节炎, 免疫治疗