Clear Sky Science · de
DC-CD4 bispezifische tolerogene Nanovesikel induzieren antigenspezifische regulatorische T‑Zellen und bessern kollageninduzierte Arthritis bei Mäusen
Dem Immunsystem beibringen, wann es nicht angreifen soll
Autoimmunerkrankungen entstehen, wenn das Abwehrsystem des Körpers irrtümlich eigenes Gewebe angreift und dadurch chronische Schmerzen und Schäden verursacht. Anstatt das Immunsystem breit zu unterdrücken, suchen Wissenschaftler nach Wegen, diese Abwehrkräfte so umzuschulen, dass sie harmlose, körpereigene Ziele ignorieren, während sie weiterhin echte Bedrohungen bekämpfen. Diese Studie an Mäusen beschreibt ein winziges, konstruiertes Paket, das genau das anstrebt und auf präzisere Behandlungen für Erkrankungen wie rheumatoide Arthritis in der Zukunft hindeutet. 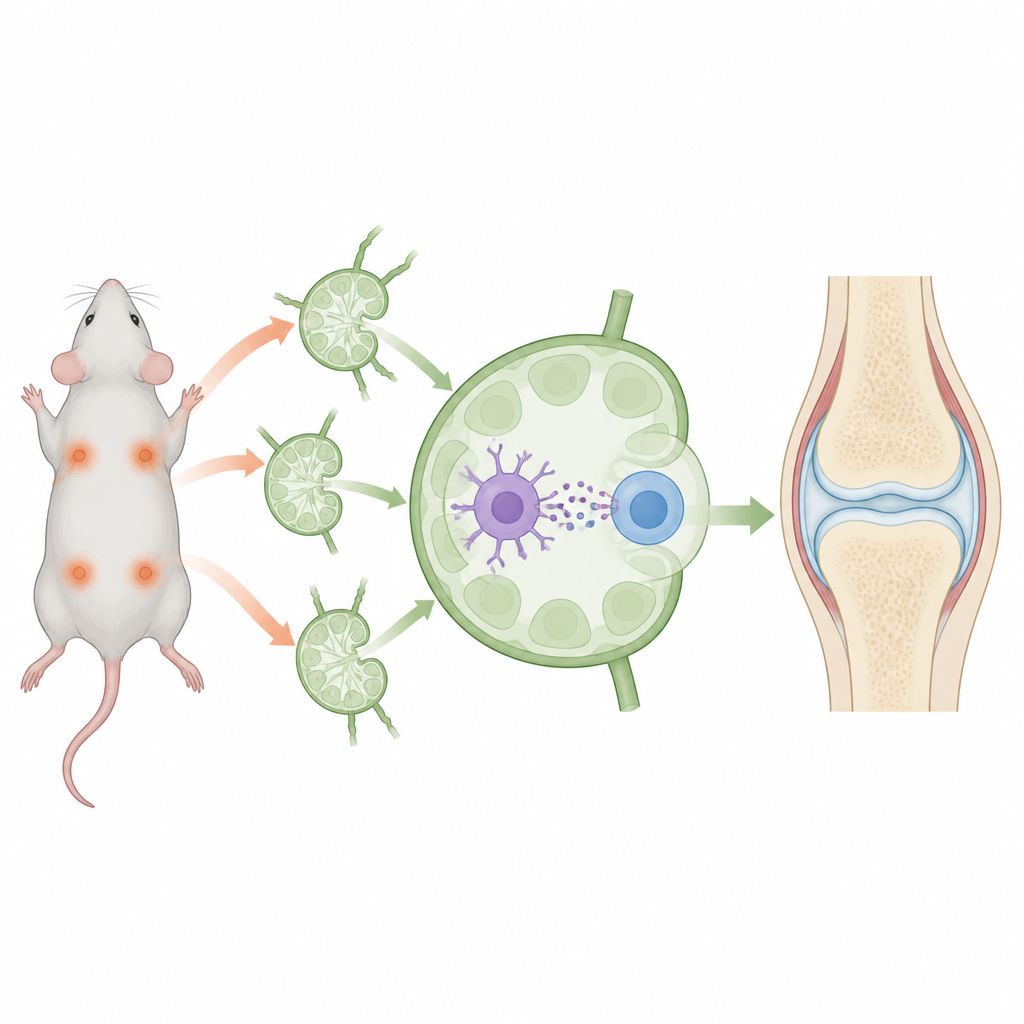
Warum es wichtig ist, die richtigen Zellen herunterzufahren
Ein gesundes Immunsystem kann zwischen „selbst“ und „Fremd“ unterscheiden — ein Gleichgewicht, das als immunologische Toleranz bezeichnet wird. Spezielle weiße Blutkörperchen, die regulatorischen T‑Zellen, fungieren als Friedenswächter und dämpfen schädliche Reaktionen, bevor sie zur Krankheit eskalieren. Ärzt*innen haben versucht, diese Zellen zu stärken, indem man sie außerhalb des Körpers vermehrt und zurückinfundiert oder indem man Medikamente einsetzt, die ihr Wachstum im Körper begünstigen. Beide Ansätze haben Nachteile, etwa aufwändige Zellmanipulationen und das Risiko, die Immunabwehr zu stark abzuschwächen. Das Ziel ist, nur jene regulatorischen Zellen zu erhöhen, die die störenden Selbst‑Moleküle erkennen, die mit einer bestimmten Erkrankung verbunden sind.
Entwurf winziger Friedenspakete
Die Forschenden bauten nanoskalige Bläschen, sogenannte Nanovesikel, aus den äußeren Membranen von Immunzellen, die bereits beruhigende Eigenschaften haben. Diese Vesikel wurden mit zwei Schlüsselinhalten beladen: einem kurzen Kollagenfragment, einem in Gelenken vorkommenden Protein, das bei Arthritis angegriffen wird, und dem Medikament Rapamycin, das einen toleranteren immunologischen Zustand fördert. Die Nanovesikel wurden dann „geschmückt“, damit sie sich an zwei verschiedene Partner in Lymphknoten anheften können: dendritische Zellen, die Antigene präsentieren, und CD4‑T‑Zellen, die sich entweder zu aggressiven Kämpfern oder zu regulatorischen Friedensstiftern entwickeln können. Indem diese beiden Zelltypen physisch um dasselbe Kollagenfragment und das Medikament zusammengebracht wurden, sollten die Vesikel das Gespräch in Richtung Toleranz statt Angriff lenken.
Immunsystem gezielt an den richtigen Ort lenken
Nach Injektion in die Haut der Mäuse flossen die Nanovesikel in nahegelegene Lymphknoten, die Schaltzentralen, in denen immunologische Entscheidungen getroffen werden. Dort hefteten sie sich stark an sowohl dendritische Zellen als auch CD4‑T‑Zellen und dienten effektiv als Brücken zwischen ihnen. Im Vergleich zu freiem Medikament und freiem Kollagen lieferten die Vesikel deutlich mehr Material in dendritische Zellen und steigerten stark, wie gut diese Zellen das Kollagenfragment präsentierten. Gleichzeitig verschoben sie sowohl dendritische Zellen als auch CD4‑T‑Zellen hin zu einem ruhigeren, stärker regulatorischen Profil, mit weniger entzündlichen Signalen und mehr beruhigenden Faktoren wie TGF‑beta und IL‑10. Dieses Milieu begünstigte die Entstehung kollagenspezifischer regulatorischer T‑Zellen, die später Immunangriffe auf Gelenke erkennen und einschränken würden.
Gelenkschutz in einem Arthritismodell
Um zu prüfen, ob diese Immun‑Umschulung im Krankheitsverlauf eine Rolle spielt, verwendete das Team ein etabliertes Mausmodell der kollageninduzierten Arthritis, das viele Merkmale der menschlichen rheumatoiden Arthritis nachbildet. Mäuse, die mit kollagenbeladenen Nanovesikeln behandelt wurden, entwickelten deutlich mildere Gelenkschwellungen, behielten eine normalere Beweglichkeit und verloren weniger Gewicht als unbehandelte Tiere. Detaillierte Bildgebung und Gewebeschnitte zeigten weniger Gelenkzerstörung, weniger Anzeichen aktiver Entzündung und reduzierte Vernarbung bei den behandelten Mäusen. Wichtig ist, dass regulatorische T‑Zellen nicht nur in Lymphknoten und Milz zunahmen, sondern auch in der Gelenkschleimhaut selbst, während schädliche entzündliche Moleküle zurückgingen. Varianten der Nanovesikel, denen das korrekte Antigen fehlte oder die nicht beide Zelltypen effektiv überbrücken konnten, boten schwächeren Schutz, was die Bedeutung sowohl der Antigenauswahl als auch der Zell‑zu‑Zell‑Verbindung unterstreicht. 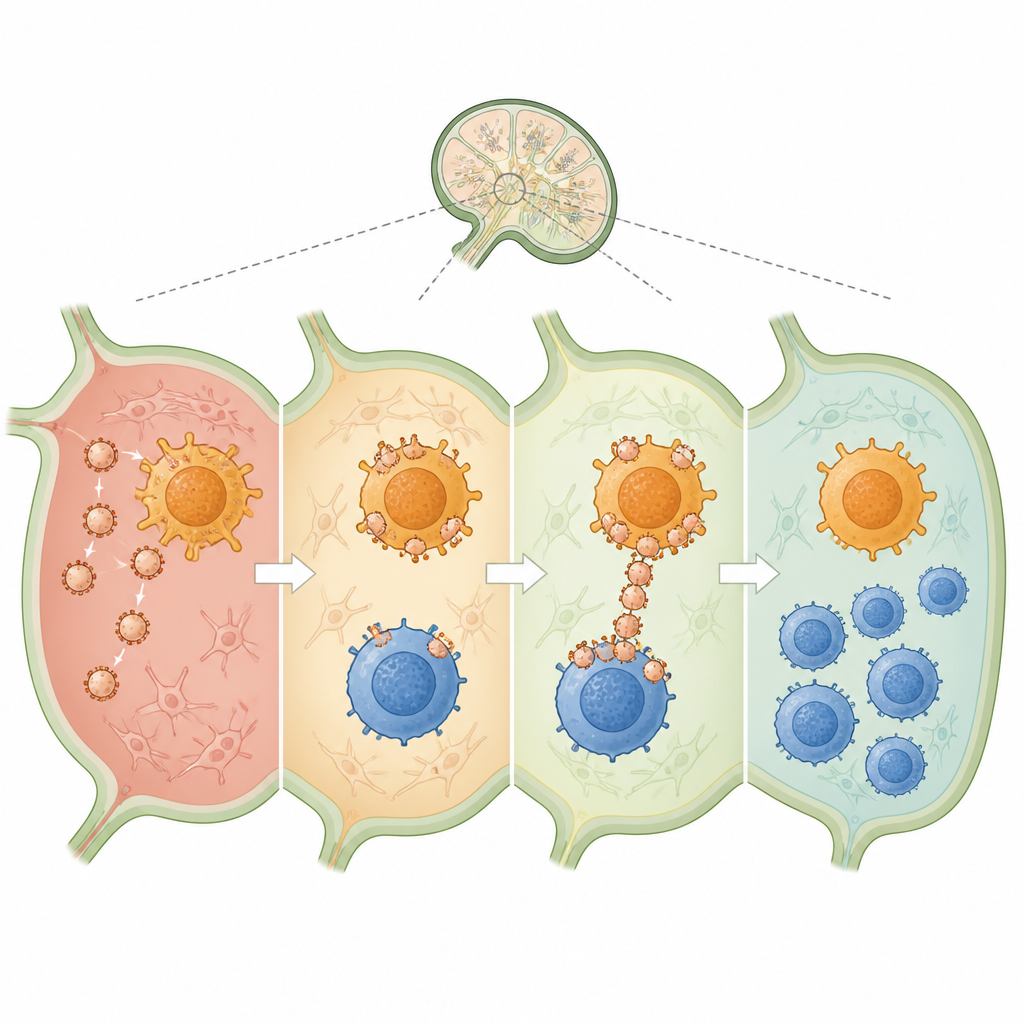
Dauerhafte Beruhigung und Ausblick
Die Forschenden zeigten außerdem, dass die durch diese Nanovesikel ausgelösten regulatorischen T‑Zellen Schutz auf andere Mäuse übertragen und einem späteren Arthritis‑Schub widerstehen konnten, was darauf hindeutet, dass das Immunsystem die Lektion „merkt“. Obwohl die Arbeit bisher auf Mäuse und ein Arthritismodell beschränkt ist, deutet sie auf eine flexible Plattform hin, in der krankheitsspezifische Selbst‑Fragmente ausgetauscht werden könnten, um die Immunantwort bei unterschiedlichen Autoimmunerkrankungen umzuschulen. Für Patient*innen zielt dieser Ansatz nicht darauf ab, das Immunsystem vollständig stummzuschalten, sondern ihm beizubringen, nur dort zurückzutreten, wo es Schaden anrichtet.
Zitation: Zhao, L., Gao, Z., Yuan, Z. et al. DC-CD4 bispecific tolerogenic nanovesicles induce antigen-specific regulatory T cells and ameliorate collagen-induced arthritis in mice. Nat Commun 17, 4170 (2026). https://doi.org/10.1038/s41467-026-70898-y
Schlüsselwörter: autoimmune Toleranz, regulatorische T‑Zellen, Nanovesikel, rheumatoide Arthritis, Immuntherapie