Clear Sky Science · es
Nanovesículas tolerogénicas bispecíficas DC-CD4 inducen células T reguladoras específicas de antígeno y mejoran la artritis inducida por colágeno en ratones
Enseñar al sistema inmunitario cuándo no atacar
Las enfermedades autoinmunes se producen cuando el sistema de defensa del organismo se vuelve contra sus propios tejidos, provocando dolor crónico y daño. En lugar de apagar la inmunidad de forma general, los científicos buscan maneras de reentrenar estas defensas para que ignoren objetivos inofensivos concretos mientras siguen combatiendo las amenazas reales. Este estudio en ratones describe un pequeño paquete diseñado con ese propósito, que apunta a tratamientos más precisos para afecciones como la artritis reumatoide en el futuro. 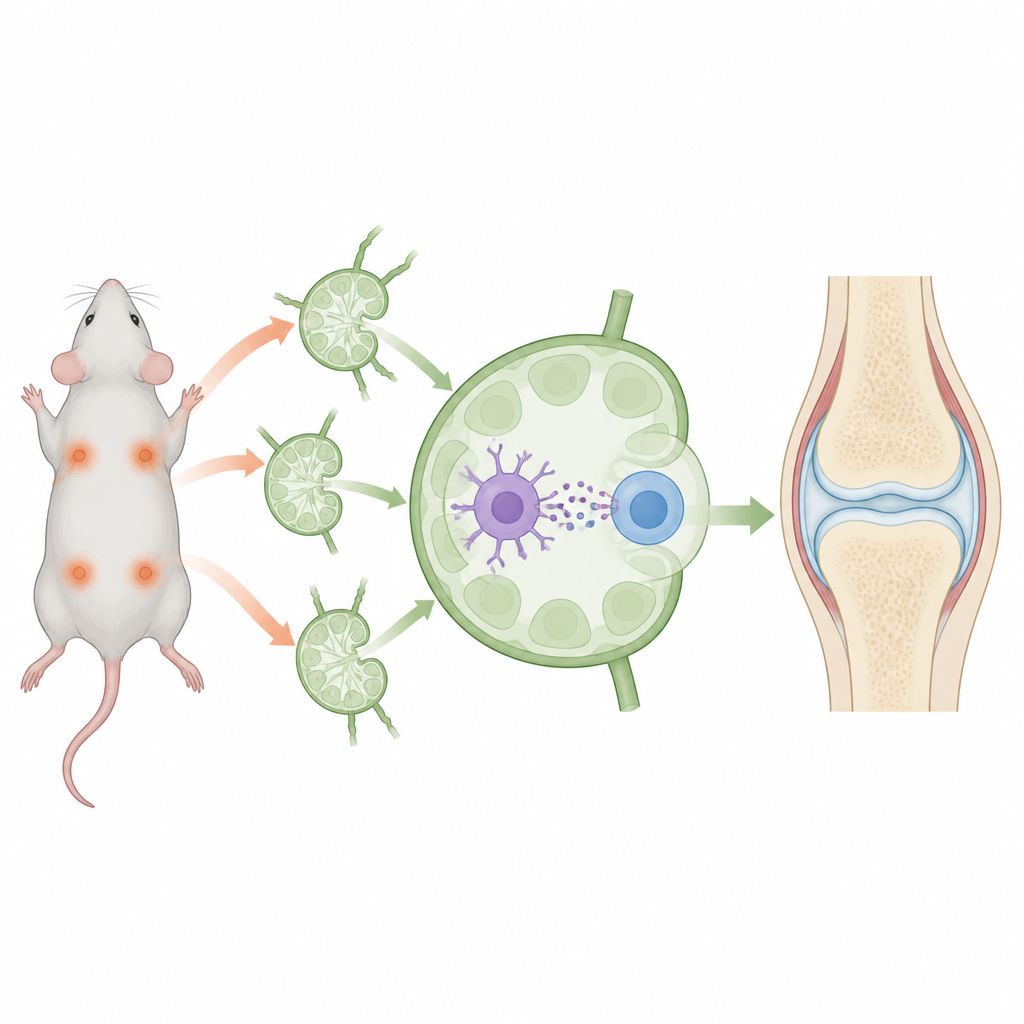
Por qué importa apagar las células correctas
Un sistema inmunitario sano distingue entre lo “propio” y lo “foráneo”, un equilibrio conocido como tolerancia inmunitaria. Ciertas células blancas llamadas células T reguladoras actúan como pacificadoras, calmando reacciones dañinas antes de que deriven en enfermedad. Los médicos han intentado aumentar estas células ya sea cultivándolas fuera del cuerpo para reinyectarlas, o usando fármacos que favorecen su expansión in vivo. Ambos enfoques tienen inconvenientes, incluidos procedimientos celulares complejos y el riesgo de debilitar la inmunidad de forma demasiado amplia. El objetivo es incrementar únicamente aquellas células reguladoras que reconocen las moléculas propias problemáticas asociadas a una enfermedad concreta.
Diseñando pequeños paquetes pacificadores
Los investigadores construyeron burbujas de tamaño nanométrico, o nanovesículas, a partir de las membranas externas de células inmunitarias que ya poseen rasgos calmantes. Estas vesículas se cargaron con dos ingredientes clave: un fragmento corto de colágeno, una proteína articular atacada en la artritis, y el fármaco rapamicina, que fomenta un estado inmunitario más tolerante. A las nanovesículas se las “decoró” para que pudieran unirse a dos socios distintos en los ganglios linfáticos: las células dendríticas, que presentan antígenos, y las células T CD4, que pueden convertirse en luchadoras agresivas o en pacificadoras reguladoras. Al reunir físicamente estos dos tipos celulares alrededor del mismo fragmento de colágeno y del fármaco, las vesículas estaban diseñadas para inclinar la interacción hacia la tolerancia en lugar de la respuesta agresiva.
Guiando el tráfico inmune al lugar adecuado
Cuando se inyectaron en la piel de ratones, las nanovesículas drenaron hacia los ganglios linfáticos cercanos, los centros donde se toman las decisiones inmunitarias. Allí, se unieron con fuerza tanto a las células dendríticas como a las células T CD4, actuando efectivamente como puentes entre ellas. En comparación con el fármaco y el colágeno libres, las vesículas entregaron mucho más material a las células dendríticas y aumentaron notablemente la presentación del fragmento de colágeno por parte de estas células. Al mismo tiempo, desplazaron tanto a las células dendríticas como a las células T CD4 hacia un perfil más silencioso y regulador, con menos señales inflamatorias y más señales calmantes como TGF-beta e IL-10. Este entorno favoreció el crecimiento de células T reguladoras específicas para el colágeno que posteriormente reconocerían y contenerían los ataques inmunitarios dirigidos a las articulaciones.
Protegiendo las articulaciones en un modelo de artritis
Para evaluar si esta reeducación inmune tenía impacto en la enfermedad, el equipo utilizó un modelo estándar de ratón de artritis inducida por colágeno, que imita muchas características de la artritis reumatoide humana. Los ratones tratados con nanovesículas cargadas de colágeno desarrollaron inflamación articular mucho más leve, conservaron una movilidad más normal y perdieron menos peso que los animales no tratados. Imágenes detalladas y cortes tisulares mostraron menos erosión articular, menos signos de inflamación activa y una reducción de la fibrosis en los ratones tratados. De forma importante, las células T reguladoras aumentaron no solo en los ganglios linfáticos y el bazo, sino también en el revestimiento de la articulación, mientras que las moléculas inflamatorias dañinas descendieron. Versiones de las nanovesículas que carecían del antígeno correcto, o que no podían conectar eficazmente ambos tipos celulares, ofrecieron una protección menor, subrayando la importancia tanto de la elección del antígeno como del enlace célula a célula. 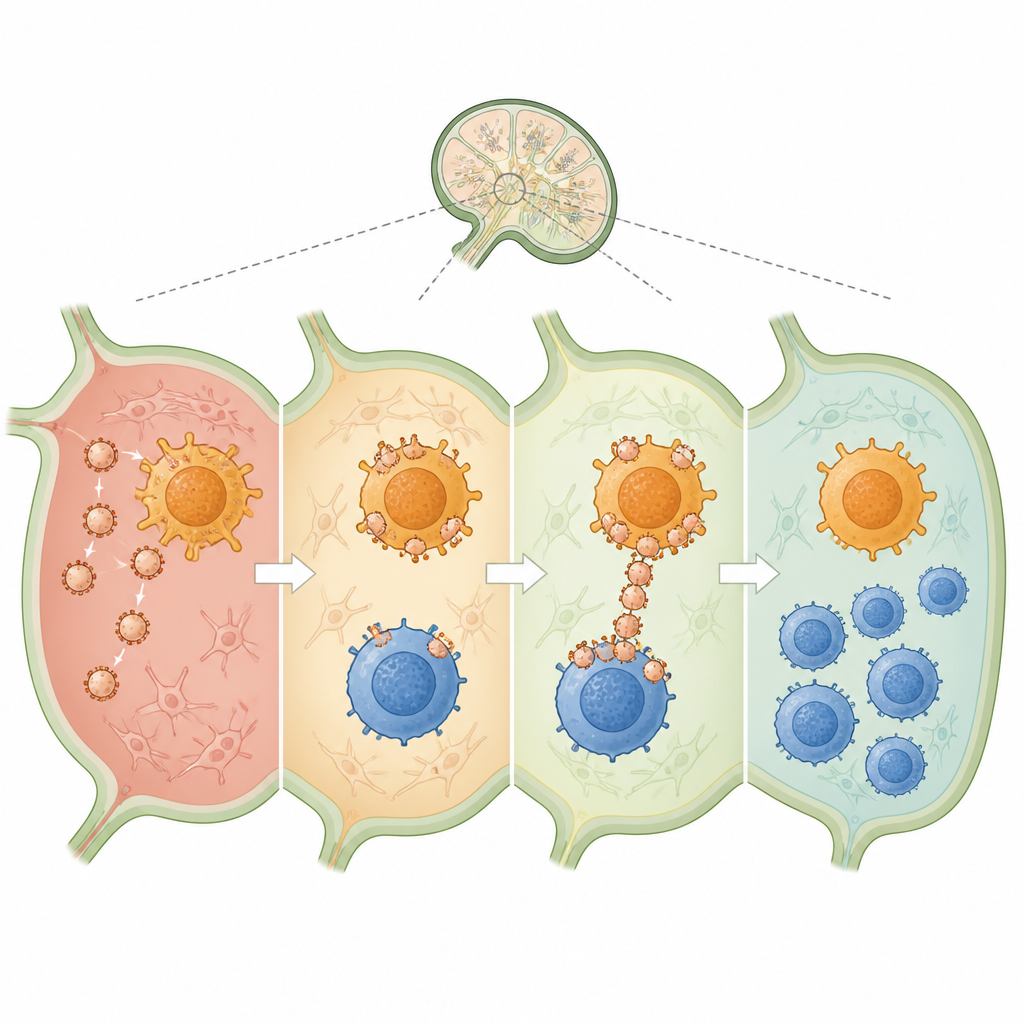
Calma duradera y qué sigue
Los investigadores demostraron además que las células T reguladoras inducidas por estas nanovesículas podían transferir protección a otros ratones y ayudar a resistir un posterior brote de artritis, lo que sugiere que el sistema inmunitario “recuerda” la lección. Aunque el trabajo sigue limitado a ratones y a un único modelo de artritis, apunta hacia una plataforma flexible en la que se podrían intercambiar fragmentos propios específicos de la enfermedad para reentrenar la inmunidad en distintas afecciones autoinmunes. Para los pacientes, este enfoque no pretende silenciar por completo el sistema inmunitario, sino enseñarle a retirarse únicamente donde está causando daño.
Cita: Zhao, L., Gao, Z., Yuan, Z. et al. DC-CD4 bispecific tolerogenic nanovesicles induce antigen-specific regulatory T cells and ameliorate collagen-induced arthritis in mice. Nat Commun 17, 4170 (2026). https://doi.org/10.1038/s41467-026-70898-y
Palabras clave: tolerancia autoinmune, células T reguladoras, nanovesículas, artritis reumatoide, terapia inmunológica